アルツハイマー病の新規病態と遺伝子治療法の発見 (2018)
アルツハイマー病のモデルマウスを用いて、アルツハイマー病超早期に生じる SRRM2 タンパク質リン酸化の病的意義を明らかにしました。SRRM2 リン酸化は核内部の SRRM2 減少につながり、更にRNA スプライシング関連タンパク質(特に発達障害原因タンパク質 PQBP1)の減少、シナプス関連タンパク質の発現低下、さらにシナプス障害を引き起こし、最終的に認知症状を引き起こしていることを明らかにしました。この研究は、当分野の博士課程学生・田中ひかり、同・近藤和、助教・藤田慶大らが主に行ったもので、平成26年度から始まった文部科学省『革新的技術による脳機能ネットワークの全容解明プロジェクト』(平成27年度から日本医療研究開発機構:AMED へ移管)で実施されました。また、一部は、脳科学研究戦略推進プログラム課題 E、新学術領域研究『シナプス・ニューロサーキットパソロジーの創成』の支援を受けました。その研究成果は、国際科学誌 Molecular Psychiatry(モレキュラー・サイキアトリー)2に、2018年10月3日にオンライン版で発表されました。
アルツハイマー病、前頭側頭葉変性症、レヴィー小体型認知症の3大認知症は、高齢化社会の日本で大きな社会問題となっています。アルツハイマー病は、2025年には高齢者の5人に1人が罹患すると言われています。 これらの3大認知症については、根本的な治療法(病態修飾治療法: Disease Modifying Therapy: DMTとも言う)は確立されていません。また、遺伝子変異によって引き起こされる病態についても、多くの知識が蓄積されてきているものの、どの時期からどのような病態が生じているのか、いつからどのような病態を標的に治療をすれば良いのか、については明確になっていません。例えば、アルツハイマー病では欧米の巨大製薬企業を中心にアミロイド凝集除去を目的としてアミロイド抗体を用いた多くの国際的臨床試験(日本を含む)が行われてきましたが、アミロイド除去には成功したものの、臨床症状の改善には至っていません。これらの事例は、症状としての発症以前、さらにはアミロイド凝集体出現以前(凝集前)の『超早期病態』を解明する必要性を示しています。
先行研究において、私達はアルツハイマー病モデルマウス4種類から、発症前・アミロイド凝集前の時期から発症時期までの期間に脳サンプルを採取し、これを網羅的リン酸化プロテオーム解析にかけました。 これにより、発症前・アミロイド凝集前にリン酸化を受けるタンパク質が3つあることを発見しました。その1つは、細胞膜形状の制御に関わる分子MARCKSであり、発症前・アミロイド凝集前のMARCKSリン酸化がシナプス変性・神経突起変性につながることを報告しました(Fujita et al, Sci Rep 2016; 平成28年8月25日プレス発表)。しかしながら、残りの2つのタンパク質(SRRM2、Marcksl1)のリン酸化のアルツハイマー病態における意義は十分に解明されていませんでした。
本研究において私達は、超早期アルツハイマー病態(発症前・アミロイド凝集前)におけるSRRM2タンパク質リン酸化の病的意義を明らかにしました。まず、発症前・アミロイド凝集前に観察されたSer1068のリン酸化はSRRM2のTCP1alphaに対する結合を弱めることを発見しました。TCP1alphaはタンパク質の折りたたみを助けるシャペロンタンパク質のひとつですが、細胞質内の小胞体で作られたSRRM2と結合して、SRRM2の折りたたみを助けて正しい3次構造にする役割があると考えられます。Ser1068でリン酸化されたSRRM2は正しい3次構造を取ることができず、その後に核へ輸送されにくくなり、核内の量が減少します。SRRM2タンパク質は細胞の核内部で多くのRNA関連タンパク質と結合して、結合相手を安定化するスカフォールドタンパク質と考えられており、実際、アルツハイマー病態では、SC35, PQBP1などのRNA関連タンパク質が核内部で減少していることがわかりました。
アルツハイマー病、前頭側頭葉変性症、レヴィー小体型認知症の3大認知症は、高齢化社会の日本で大きな社会問題となっています。アルツハイマー病は、2025年には高齢者の5人に1人が罹患すると言われています。 これらの3大認知症については、根本的な治療法(病態修飾治療法: Disease Modifying Therapy: DMTとも言う)は確立されていません。また、遺伝子変異によって引き起こされる病態についても、多くの知識が蓄積されてきているものの、どの時期からどのような病態が生じているのか、いつからどのような病態を標的に治療をすれば良いのか、については明確になっていません。例えば、アルツハイマー病では欧米の巨大製薬企業を中心にアミロイド凝集除去を目的としてアミロイド抗体を用いた多くの国際的臨床試験(日本を含む)が行われてきましたが、アミロイド除去には成功したものの、臨床症状の改善には至っていません。これらの事例は、症状としての発症以前、さらにはアミロイド凝集体出現以前(凝集前)の『超早期病態』を解明する必要性を示しています。
先行研究において、私達はアルツハイマー病モデルマウス4種類から、発症前・アミロイド凝集前の時期から発症時期までの期間に脳サンプルを採取し、これを網羅的リン酸化プロテオーム解析にかけました。 これにより、発症前・アミロイド凝集前にリン酸化を受けるタンパク質が3つあることを発見しました。その1つは、細胞膜形状の制御に関わる分子MARCKSであり、発症前・アミロイド凝集前のMARCKSリン酸化がシナプス変性・神経突起変性につながることを報告しました(Fujita et al, Sci Rep 2016; 平成28年8月25日プレス発表)。しかしながら、残りの2つのタンパク質(SRRM2、Marcksl1)のリン酸化のアルツハイマー病態における意義は十分に解明されていませんでした。
本研究において私達は、超早期アルツハイマー病態(発症前・アミロイド凝集前)におけるSRRM2タンパク質リン酸化の病的意義を明らかにしました。まず、発症前・アミロイド凝集前に観察されたSer1068のリン酸化はSRRM2のTCP1alphaに対する結合を弱めることを発見しました。TCP1alphaはタンパク質の折りたたみを助けるシャペロンタンパク質のひとつですが、細胞質内の小胞体で作られたSRRM2と結合して、SRRM2の折りたたみを助けて正しい3次構造にする役割があると考えられます。Ser1068でリン酸化されたSRRM2は正しい3次構造を取ることができず、その後に核へ輸送されにくくなり、核内の量が減少します。SRRM2タンパク質は細胞の核内部で多くのRNA関連タンパク質と結合して、結合相手を安定化するスカフォールドタンパク質と考えられており、実際、アルツハイマー病態では、SC35, PQBP1などのRNA関連タンパク質が核内部で減少していることがわかりました。
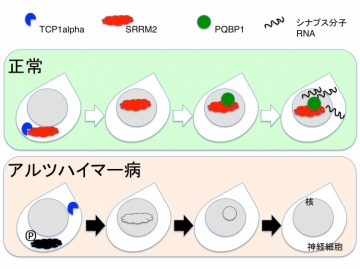
【左図】正常状態では、SRRM2はTCP1alphaと結合し、正常な折りたたみをすることが出来て、核に移行します。核では、PQBP1などのRNAスプライシング関連因子を安定化して(タンパク質寿命を延ばして)、RNA成熟を介して、シナプス形成に必要なタンパク質を増やします。ところが、アルツハイマー病態ではSRRM2はSer1068でリン酸化してTCP1alphaと結合できなくなり、核への移行が減少し、PQBP1タンパク質も減少します。図中のPはリン酸化を示す。 この結果、RNAスプライシングの効率が低下し、シナプス形成に必要な分子のRNAが作れなくなります。 この現象はヒトでも生じていると考えられ、実際、アルツハイマー病のヒト脳においてもSRRM2リン酸化、PQBP1タンパク質減少が確認されました。
この中で、PQBP1はレンペニング症候群、ゴラビ・伊藤・ホール症候群など、多くの発達障害症候群の原因遺伝子であることが知られています。そこで私達は、新たにPQBP1が成熟神経細胞にのみ欠損している遺伝子組み換えマウス(PQBP1-Synapsin-Cre-cKOマウス)を作成して、アルツハイマー病モデルマウス(5xFADマウス)とのシナプス異常と遺伝子発現における共通性を検討しました。 この結果、PQBP1-Syn-cKOマウスと5xFADマウスは、共通してシナプス形態に異常があり、シナプス関連遺伝子のRNAスプライシングが変化していること、さらに5xFADマウスにおけるRNAスプライシング変化はPQBP1の補充(PQBP1遺伝子治療によって回復すること、PQBP1遺伝子治療は、5xFADマウスとヒトAPPノックインマウスにおいて、シナプス形態を回復し、記銘力テストの成績を顕著に回復させることも示されました。
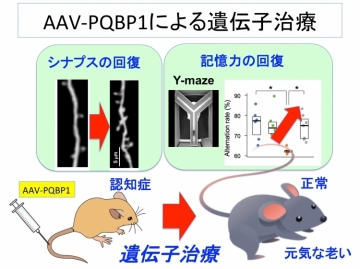
【右図】2種類のアルツハイマー病モデルマウスにPQBP1遺伝子治療(AAV-PQBP1)を用いることで、発症後であっても神経回路の伝達を改善し、記憶力を回復できました。ヒトでも同様な治療の可能性が開けてきました。
また、本研究ではSRRM2リン酸化に至る、上流シグナルについても検討を行い、種々の解析の結果、Erk1, Erk2という酵素がSer1068でSRRM2をリン酸化すると考えられました。発症前・アミロイド凝集前の時期には、モデルマウスの脳内で細胞内のアミロイドが蓄積している状態が存在しており、これがERストレスなど何らかのシグナル経路を通じてErk1/2の過度な活性化状態を来しているものと想定されます。
アルツハイマー病は認知症の最も頻度の高い原因です。本研究において、私達は、アルツハイマー病の超早期(発症前・アミロイド凝集前)に生じる新しい病態メカニズムを明らかにし、この新規病態をターゲットにすることで治療が可能であることを示しました。アルツハイマー病においては、多くの臨床試験が失敗し、従来の仮説とは異なる病態仮説に基づいた新規治療法の開発が求められています。
本研究は、現在の認知症研究の焦点となっている超早期病態解明と、超早期病態で主要な役割を果たす、新たな標的分子を用いた遺伝子治療法を示した点でも、大きな意義を持つと考えられます。
アルツハイマー病は認知症の最も頻度の高い原因です。本研究において、私達は、アルツハイマー病の超早期(発症前・アミロイド凝集前)に生じる新しい病態メカニズムを明らかにし、この新規病態をターゲットにすることで治療が可能であることを示しました。アルツハイマー病においては、多くの臨床試験が失敗し、従来の仮説とは異なる病態仮説に基づいた新規治療法の開発が求められています。
本研究は、現在の認知症研究の焦点となっている超早期病態解明と、超早期病態で主要な役割を果たす、新たな標的分子を用いた遺伝子治療法を示した点でも、大きな意義を持つと考えられます。
発表論文
Tanaka, H., Kondo, K., Chen, X., Homma, H., Tagawa, K., Kerever, A., Aoki, S., Saito, T., Saido, T., Muramatsu, S., Fujita, K. & Okazawa, H. (2018)
The intellectual disability gene PQBP1 rescues Alzheimer’s disease pathology.
Mol. Psychiatry 1. doi: 10.1038/s41380-018-0253-8
The intellectual disability gene PQBP1 rescues Alzheimer’s disease pathology.
Mol. Psychiatry 1. doi: 10.1038/s41380-018-0253-8

