「 インターフェロン応答を制御する経時的なアイソフォームスイッチングの役割 」【高地雄太 教授】
― 選択的スプライシングの遺伝子機能への影響を探る ―
ポイント
- 長鎖RNAシーケンス※1を用いて、インターフェロン※2刺激を受けたB細胞※3において転写物アイソフォーム※4を詳細に同定しました。
- アイソフォームの変化が、翻訳効率やタンパク質の構造に影響を与え、遺伝子の機能を変化させることを明らかにしました。
- インターフェロン応答初期では、完全な機能を持つアイソフォームが優勢となり、後期では機能を欠くアイソフォームの割合が増加することを発見しました。
- 特定のアイソフォームの発現比率が、自己免疫疾患や感染症のリスクに関連することを明らかにしました。
研究の背景
そのため、IFN-I応答がどのように制御されているのかを理解することは、感染症から自己免疫疾患に至る幅広い病態の解明や新たな治療法の開発において非常に重要です。しかし、これまでのIFN-I応答に関する研究の多くは、技術的な限界からIFN-I刺激時にのみ発現するアイソフォームが十分に同定されておらず、遺伝子レベルでの発現に焦点が当てられてきました。
研究成果の概要
本研究では、高精度な長鎖RNAシークエンシングが可能なPacBio Iso-SeqII/IIeプラットフォームを用いて、IFN-I非刺激・刺激状態のヒトB細胞の転写物アイソフォームの詳細なプロファイリングを行い、11万以上の転写物の配列カタログ「isoforms of Interferon-Stimulated Genes(isoISG)」を作成しました。このisoISGの約60%は、従来のデータベースに未登録の新規アイソフォームであることが明らかになりました。
このisoISGを用いて、IFN-I刺激を受けたヒトB細胞におけるアイソフォームの発現変化を詳細に解析しました。その結果、IFN応答遺伝子で、従来の遺伝子レベルの解析ではわからなかった、“主要なアイソフォームが別のアイソフォームに切り替わる現象(アイソフォーム・スイッチング)”が起きていることが明らかになりました(下図中)。IFN-I初期応答(6時間)では、IFN-I刺激前に発現していた、“機能が欠損し翻訳効率が低い”アイソフォームが、刺激後は“機能的なドメインを持ち翻訳効率も高い”アイソフォームにスイッチすることが分かりました。これにより、初期応答において適切なIFN-I応答が促進されると考えられます。一方、IFN-I後期応答(24時間~)では、イントロン保持※5が見られるアイソフォームの割合が増加することが明らかになりました。イントロンが保持されたアイソフォームは、mRNAが分解されやすくなり、翻訳効率も低下するため、遺伝子の全体としての機能が低下すると考えられます。特に、IFN-I応答の中心的な役割を担う転写因子で、イントロン保持アイソフォームの割合が時間とともに増加することから、IFN-I応答が収束に向かうメカニズムが示唆されました。また、SRSF6やSRSF8などのスプライシングに関与する遺伝子がイントロン保持アイソフォームの発現と強く関連し、精密に調節していることも明らかになりました。
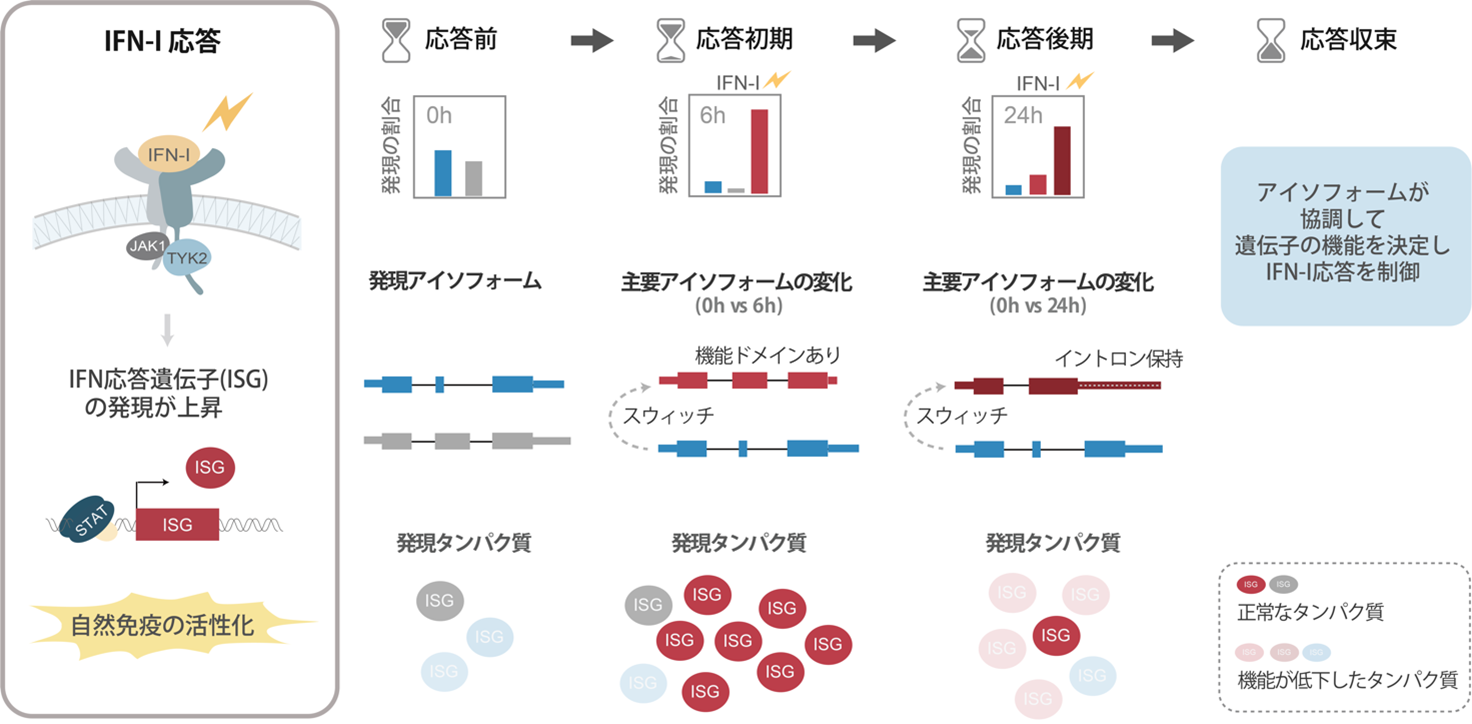
図. I型インターフェロン応答を制御する経時的なアイソフォームスイッチングの役割
I型インターフェロン(IFN-I)刺激を受けたヒトB細胞におけるアイソフォームスイッチングの経時的変化を示す。IFN応答の初期段階(6時間)では、機能的ドメインを持つアイソフォームの割合が優勢となり、遺伝子の機能が向上し、IFN-I応答の正のフィードバックが促進される。一方、後期段階(24時間以降)では、イントロン保持アイソフォームの割合が増加し、mRNAの分解、翻訳効率の低下、ドメイン欠失等により遺伝子の機能が低下する。これにより、負のフィードバックが働くことで免疫応答が収束すると考えられる。
さらに、isoISGを用いて、疾患リスクに関連する新たなアイソフォームを同定しました。例えば、STAT6(喘息)やTYK2(1型糖尿病、SLE※6など)などの疾患に関連するアイソフォームは、いずれもイントロン保持によって機能が欠損しており、リスクアレルを持つ人ではこれらのアイソフォームの発現割合が低いことが確認されました。これらの結果は、リスクアレルを持つ人ではIFN-I応答の収束が適切に行われない可能性が示唆されます。興味深いことに、TYK2の機能欠失アイソフォームはCOVID-19の重症化リスクとも関連していることが分かりましたが、逆に、このアイソフォームの割合が高いことが重症化リスクを高めることが示唆されました。これにより、感染症の重症化リスクにおいて、この機能欠失アイソフォームがIFN-I応答を弱め、ウイルスの排除が不十分になる可能性があります。
研究成果の意義
用語解説
※1 長鎖RNAシーケンス: 遺伝子から転写されたRNA(転写物)を、従来の方法よりも長い断片として読み取る技術。特にPacBioシーケンスは、高精度な配列を得ることができ、複雑な遺伝子の転写物の解析に適している。
※2 インターフェロン: 免疫細胞の活動を調節するサイトカインというタンパク質の一種。特にI型インターフェロンは、ウイルス感染時に自然免疫システムを一早く活性化する。
※3 B細胞: 免疫細胞の一種で、主に抗体を産生することで知られるが、自然免疫の一環としてウイルスや細菌への初期応答にも重要な役割を果たす。
※4 転写物アイソフォーム: 遺伝子がRNAに転写されると、エクソン(必要な部分)とイントロン(不要な部分)を含むRNAが作られる。選択的スプライシングという過程でイントロンが取り除かれ、エクソンが異なる組み合わせでつなぎ合わされることで、同じ遺伝子からでも異なる構造や機能を持つRNA(アイソフォーム)が生成される。
※5 イントロン保持: 通常、スプライシングで取り除かれるイントロンがそのまま残る現象。
※6 SLE: 全身性エリテマトーデス。代表的な自己免疫疾患で、皮膚、関節、腎臓、脳などに多様な症状を引き起こす。
論文情報
掲載誌:Cell Genomics
論文タイトル:Functional and dynamic profiling of transcript isoforms reveals essential roles of alternative splicing in interferon response
DOI:https://doi.org/10.1016/j.xgen.2024.100654
研究者プロフィール

上田 真保子 (ウエダ マホコ) Ueda Mahoko
東京医科歯科大学 難治疾患研究所
ゲノム機能多様性分野 助教
・研究領域
ゲノム科学、比較オミクス

東京医科歯科大学 難治疾患研究所
ゲノム機能多様性分野 教授
・研究領域
ゲノム医学、膠原病内科学
問い合わせ先
<研究に関すること>
東京医科歯科大学 難治疾患研究所
ゲノム機能多様性分野
〒113-8510 東京都文京区湯島1-5-45
E-mail:y-kochi.gfd[@]mri.tmd.ac.jp
<報道に関すること>
東京医科歯科大学 総務部総務秘書課広報係
〒113-8510 東京都文京区湯島1-5-45
E-mail:kouhou.adm[@]tmd.ac.jp
※E-mailは上記アドレス[@]の部分を@に変えてください。

