「 ビッグデータを用いた時系列トータルシミュレーションによって新しい病態・バイオマーカーを発見 」【岡澤均 教授】
新しい病態・バイオマーカーを発見 」
―脊髄小脳失調症では超早期から脳炎症につながる分子的変化が起きている―
ポイント
- ビッグデータ解析は、神経変性疾患の先端的研究において主流になりつつあります。
- しかし、全分子の関係性を表現する「分子ネットワーク」の“時間的変化を因果関係に基づいて解析する手法”は存在しませんでした。
- 今回新たに開発した因果関係に基づく時系列分子ネットワーク解析法(iMAD)を用いて、脊髄小脳失調症1型のiPS細胞から小脳細胞への分化過程、さらには、マウスモデルの発症期までの病態進行の詳細を解析しました。
- その結果、発症のはるか以前(超早期)から、脳炎症に将来的に進行する病態 (ISG15などcytokine関連遺伝子を中心とする分子ネットワーク変化)が生じていることを発見しました。
- なかでもISG15につながる初期病態は重要であり、同時にISG15は脊髄小脳失調症の新たなバイオマーカーとなる可能性を示しました。
研究の背景
最近では、アルツハイマー病に対する複数の抗体医薬品が承認されたことで話題を呼びましたが、これらは基本的に異常タンパク質の沈着凝集の除去を作用基盤としているため、異常タンパク質凝集前の超早期病態には効果がないことが想定され、凝集後の病態を抑制するのみでは効果は限定的になると予想されます。
岡澤教授の研究グループでは、アルツハイマー病、前頭側頭葉変性症、ハンチントン病、脊髄小脳失調症の病態に対する網羅的なタンパク質解析(プロテオーム解析)、遺伝子発現解析(トランスクリプトーム解析)を20年前から開始し(Tagawa et al, J Neurochem 2004; Tagawa et al, J Neurosci 2007; Qi et al, Nature Cell Biol 2007; Enokido et al, J Cell Biol 2010など)、さらに2010年度-2015年度・新学術領域「シナプス・ニューロサーキットパソロジーの創成」および2010年度-2015年度・脳科学研究戦略推進プログラム課題Eにおいて、これらの疾患での異常タンパク質凝集前の『超早期病態』を世界に先駆けて提唱し、その本体を研究してきました(Tagawa et al, Hum Mol Genet 2015; Fujita et al, Sci Rep 2016; Tanaka et al, Nature Commun 2020; Homma et al, Life Sci Alliance 2021など)。
これらの研究は、生後1ヶ月以後の疾患モデルマウスあるいはヒト死後脳をサンプルに用いた解析でしたが、今回の研究では、さらに時間的に繰り上げて、受精直後のES細胞に相当するiPS細胞から解析を始め、受精から発生段階、誕生から発症、そして個体死に至る全過程を解析(トータルシミュレーション)しようと試みました。そして、研究対象とする疾患として、岡澤グループがこれまでも研究をしてきた、また希少疾患でもある、脊髄小脳失調症1型に定めました。その結果、予想外の早期にサイトカイン関連分子のネットワーク変化が認められ、中でもISG15の上昇はアタキシン1の凝集病態のトリガーになりうること、そして血液バイオマーカーにもなりうることが明らかになりました。
このシミュレーションのメソッドは、アルツハイマー病など、患者数の多いコモン疾患にも応用が可能です。また、今回はスパコンを用いた一定のアルゴリズムによる探索的研究でしたが、次の段階でAIと組み合わせることで、予測的研究へと強化することが可能です。
研究成果の概要
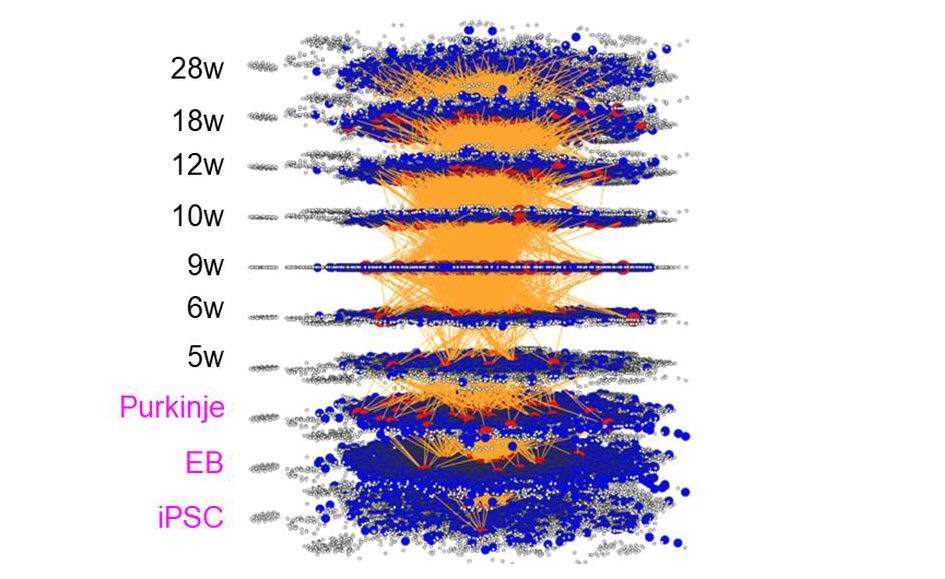
図1: 今回開発した、因果関係に基づく「分子ネットワークの時間的変化」のシミュレーション。IPS細胞の時期に起こった遺伝子発現変化が、発症さらにその後の病態進展につながっていくことが可視化できる。
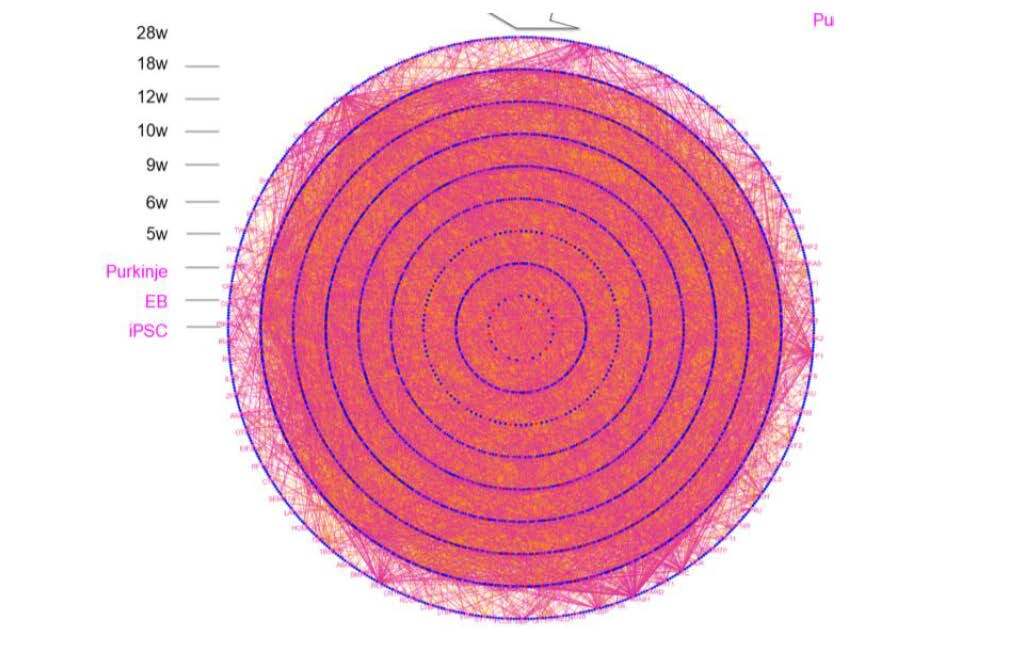
図2: 因果関係を持ってiPS細胞の時期から18週まで途絶えずに繋がっていくcytokineに関わる分子ネットワークを紫色のラインで示している。
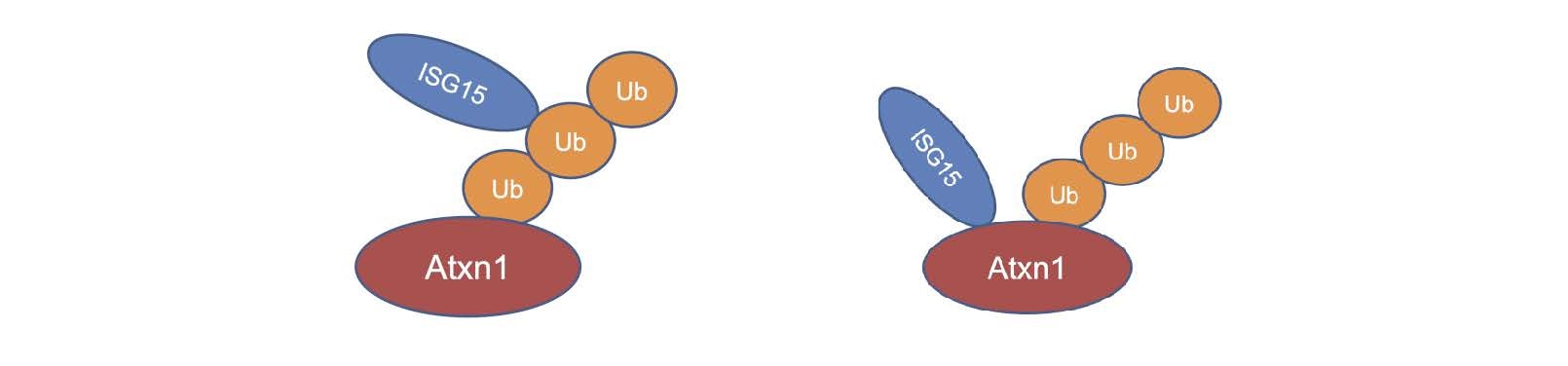
図3: ISG15はAtaxin-1タンパク質のユビキチン鎖に直接結合する(左)か、もしくはユビキチン化したAtaxin-1タンパク質の別な部位に結合して(右)、Ataxin-1タンパク質の分解を阻害すると考えられる。
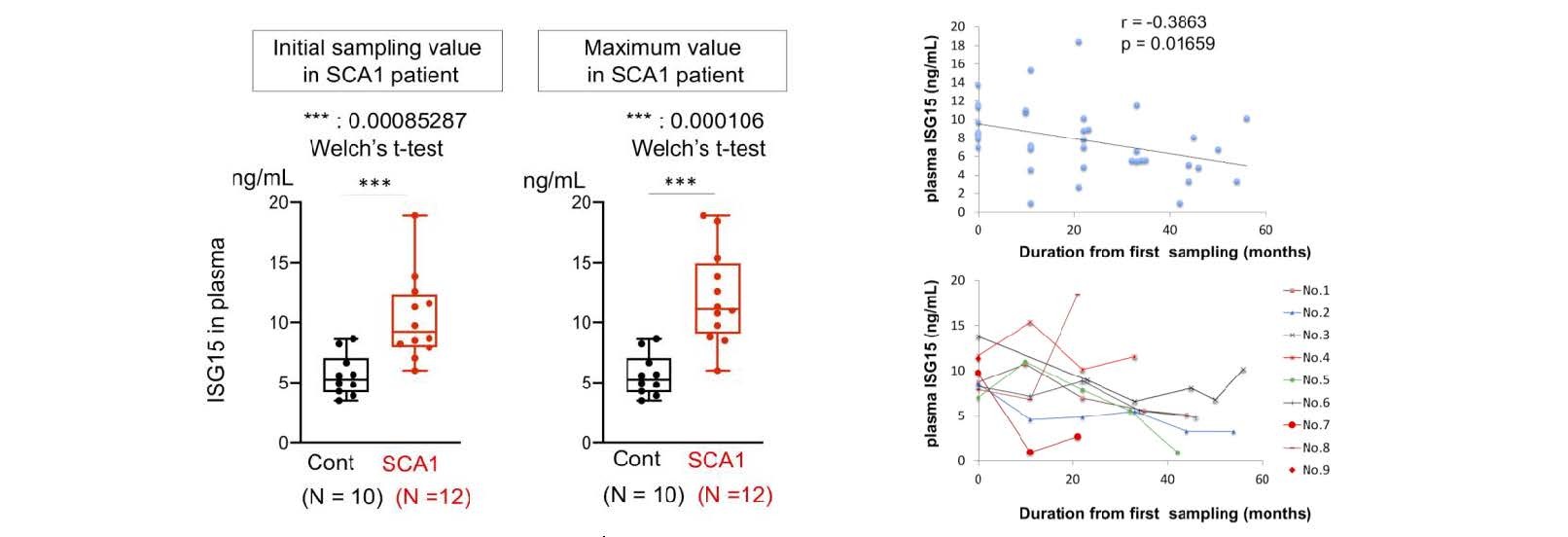
図4: 血漿中のISG15を正常者および脊髄小脳失調症1型患者で測定した(左)。患者群では有意に上昇している。一方、ISG15は発症後の病態進行に伴い徐々に低下する傾向にあった(右)。
研究成果の意義
このシミュレーションのメソッドは、アルツハイマー病など、患者数の多いコモン疾患にも応用が可能です。また、今回はスパコンを用いた一定のアルゴリズムによる探索的研究でしたが、次の段階でAIと組み合わせることで、予測的研究へと強化することが可能です。
また、今回の研究は、超早期病態が予想を超えて早い時期から起きている可能性を示しましたが、この結果は患者さんにとって失望するようなことではなく、どの時期にどのような分子を標的に治療をすれば大きな治療効果を得られるかの予測を示すことになり、治療開発につながります。さらには、どのような分子をどの時期に標的にすれば、将来の発症を抑えるあるいは遅らせることができるかを予測することにもつながります。
岡澤教授のグループでは、約10年前から代表者のアイデアで研究を開始しましたが、ラボのマンパワーあるいは研究資金の不足のため、国際的競争相手に追いつかれています。日本の生物学・医学研究では横並びに平均化することが優先されがちですが、先端的な研究を突出させる必要があると考えています。
用語解説
※1 超早期病態
アルツハイマー病などでは、発症前に既にアミロイド(同病の異常タンパク質)が脳の細胞外に沈着することが知られてる。これらの時期をprodoromalもしくはpreclinicalと国際的には呼称している。最近、日本国内では、これを「超早期病態」と呼ぶことがあるが、これは厳密には間違った使い方であり、超早期病態は異常タンパク質凝集前の分子変化・形態変化を呼ぶものである。
※2 時系列分子ネットワーク解析法(iMAD)
AIの基本となるベイズ解析の考え方に基づき、ある時点においてコントロール群と疾患群の比較において有意に変化するタンパク質について、そのタンパク質がタンパク質間相互作用データから結合関係を持つ全てのタンパク質のうち、次の時点でコントロール群と疾患群の比較において有意に変化したものの割合(有意変化率)と、全タンパクの有意変化率(背景的有意変化率)に対して比較し、前者の有意変化率が後者の背景的変化率に対して統計的な差を持って高い場合に、その結合関係が因果関係にあると判断し、線(エッジ)でタンパク質の点(ノード)を結ぶ方法。
論文情報
掲載誌: Communications Biology
論文タイトル: Dynamic molecular network analysis of iPSC differentiation to Purkinje cells delineates the role of ISG15 in temporal regulation of SCA1 pathology at the earliest stage
DOI: https://doi.org/10.1038/s42003-024-06066-z
研究者プロフィール

岡澤 均(オカザワ ヒトシ) Hitoshi Okazawa
東京医科歯科大学 難治疾患研究所
神経病理学分野 教授
研究領域
神経内科学、神経科学、神経病理学、分子生物学

本間 秀典(ホンマ ヒデノリ) Hidenori Homma
東京医科歯科大学 難治疾患研究所
神経病理学分野 特任准教授
研究領域
数理情報学
問い合わせ先
<研究に関すること>
東京医科歯科大学 難治疾患研究所
神経病理学分野 岡澤 均(オカザワ ヒトシ)
E-mail:okazawa.npat[@]mri.tmd.ac.jp
<報道に関すること>
東京医科歯科大学 総務部総務秘書課広報係
〒113-8510 東京都文京区湯島1-5-45
E-mail:kouhou.adm[@]tmd.ac.jp
※E-mailは上記アドレス[@]の部分を@に変えてください。

