「LRBA複合体はリサイクリングエンドソームにおいてAQP2を活性化し尿量を調節する」【安藤史顕 助教】
― 様々なタンパク質のリサイクルを司るLRBAの詳細な役割を解明 ―
ポイント
- 本研究ではマウス腎臓の細胞内小胞※1を精製するために新たな密度勾配遠心法※2を確立し、超解像顕微鏡や近接ライゲーションアッセイといった最新の手法を組み合わせることで、生体内のタンパク質の細胞内局在を今までにない微細なレベルで定量的に解析しました。
- 研究グループは、腎臓において尿量の調節に関わるAQP2水チャネルとLRBAが普段はリサイクリングエンドソーム※3と呼ばれる細胞内小胞に待機し、いざ私たちの体が脱水に陥るとLRBAが瞬時にAQP2の機能をONに切り替え、脱水の進行を防ぐために尿量を減少させることを明らかにしました。
- LRBAはAQP2以外にも細胞内小胞から細胞膜へ輸送される様々なタンパク質の活性を制御することが知られており、腎臓におけるLRBAの局在や役割の詳細を解明することで、腎外組織におけるLRBA機能の解明にもつながることが期待されます。
研究の背景
研究成果の概要
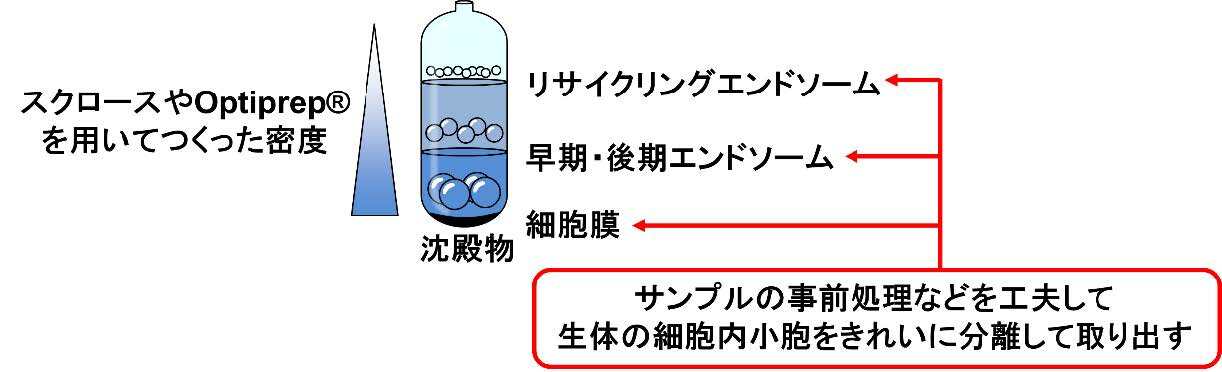
(図1) 細胞内小胞の分離のイメージ
サンプルの事前処理を工夫して、様々な細胞内小胞をきれいに分離して取り出す。
次に、LRBA欠損マウスにおけるAQP2の局在を検討しました。その結果、バゾプレシン刺激下においてもAQP2は細胞膜に移動することができず、リサイクリングエンドソームに留まることがわかりました(図2右)。これはLRBA-PKA複合体がAQP2のリサイクリングエンドソームから細胞膜への移動に必須であることを示しています。
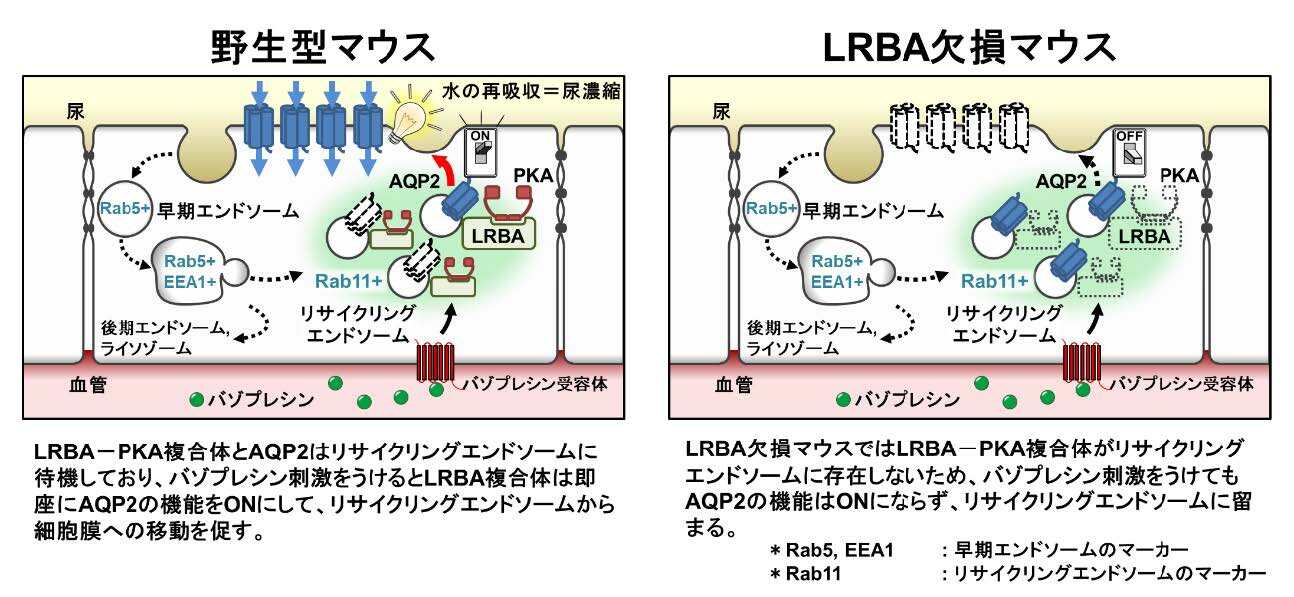
(図2) 腎臓集合管でのLRBA複合体の役割
LRBA複合体とAQP2はリサイクリングエンドソームで近接して待機しており、体内が水分不足になると直ちにLRBA複合体がAQP2の機能をONにすることで体内の水恒常性を厳密に維持している。
研究成果の意義
AQP2研究の歴史は古く、AQP2やその制御分子の局在はin vitro(培養細胞を用いた実験)であきらかにされてきましたが、in vivo(生体を用いた実験)でのAQP2の正確な局在は示されてきませんでした。本研究では、密度勾配遠心法・超解像顕微鏡・免疫電子顕微鏡・近接ライゲーションアッセイを組み合わせることで、はじめてマウス腎臓におけるAQP2とLRBAの詳細な局在を明らかにすると共に、LRBAがもつAQP2の新たな制御機構を解明しました。今回用いた手法は様々な臓器や組織の研究に用いることができ、AQP2やLRBA以外のタンパク質の局在解析にも応用が可能です。LRBAは免疫チェックポイント分子であるCTLA-4などの重要なタンパク質の輸送にも関わっており、腎臓におけるLRBAの詳細な役割が明らかになったことで、LRBA研究のさらなる発展につながることが期待されます。
用語解説
※1 細胞内小胞・・・細胞の中にある膜に包まれた袋状の構造。小胞は細胞膜などの他の構造と融合や分離をすることで膜タンパクや小胞内の物質を輸送することができる。
※2 密度勾配遠心法・・・異なる濃度のスクロースなどの溶媒を積み重ねて用いることで、異なる大きさや形の粒子を分離する方法。
※3 リサイクリングエンドソーム・・・細胞膜上の膜タンパク質が細胞に取り込まれ、また再び細胞の表面にもどされることをリサイクルという。リサイクリングエンドソームは様々な細胞内小胞のうちリサイクルに重要な役割を持つ。
※4腎臓集合管・・・腎臓ではまず原尿とよばれる非常に薄い尿がつくられ、原尿は尿細管とよばれる管を通る間に水などが再吸収されて最終的に濃い尿となる。集合管は尿細管の最後の部分であり、バゾプレシンに応答して最終的な尿量を決定する。
※5LRBAとプロテインキナーゼA(PKA)・・・PKAは他のタンパク質をリン酸化するタンパク質の一種であり、リン酸化されたタンパクのもつ機能をONにしたりOFFにしたりする役割をもつ。LRBAはPKAと結合しており、足場タンパク質としてPKAをAQP2の近くに近接して配置する役割がある。
論文情報
掲載誌:The Journal of Physiology
論文タイトル:LRBA signalosomes activate vasopressin-induced AQP2 trafficking at recycling endosomes
DOI:https://doi.org/10.1113/JP285188
研究者プロフィール

原 悠 (ハラ ユウ) Yu Hara
東京医科歯科大学病院 血液浄化療法部
特任助教
・研究領域
腎臓 水・電解質輸送

東京医科歯科大学 大学院医歯学総合研究科
腎臓内科学分野 大学院生
・研究領域
腎臓 水・電解質輸送

東京医科歯科大学 大学院医歯学総合研究科
腎臓内科学分野 助教
・研究領域
腎臓 水・電解質輸送

東京医科歯科大学 大学院医歯学総合研究科
腎臓内科学分野 教授
・研究領域
腎臓 水・電解質輸送
問い合わせ先
<研究に関すること>
東京医科歯科大学大学院医歯学総合研究科
腎臓内科学分野 氏名 安藤 史顕(アンドウ フミアキ)
E-mail:fandkidc[at]tmd.ac.jp
<報道に関すること>
東京医科歯科大学 総務部総務秘書課広報係
〒113-8510 東京都文京区湯島1-5-45
E-mail:kouhou.adm[at]tmd.ac.jp
※E-mailは上記アドレス[at]の部分を@に変えてください。

