「HBVカプシドタンパク質をターゲットとした抗HBV剤の創製」【玉村啓和 教授】
公開日:2023.8.24
「HBVカプシドタンパク質をターゲットとした抗HBV剤の創製」
― B型肝炎に対する新たな治療薬の可能性 ―
― B型肝炎に対する新たな治療薬の可能性 ―

ポイント
- B型肝炎ウイルス(HBV)※1の複製サイクルを阻害する新規の抗HBV化合物を創製しました。
- in silicoスクリーニング※2によりHBVのカプシドタンパク質(HBc)※3の4量体の疎水性ポケットに入り込む抗HBV化合物Cpd4 (1)を見出しました。また、Cpd4の高活性誘導体を創製しました。
- B型肝炎の有望な治療薬※4開発への応用が期待できます。
東京医科歯科大学 生体材料工学研究所 メディシナルケミストリー分野の玉村啓和教授の研究グループは、熊本大学大学院生命科学研究部血液・膠原病・感染症内科学講座の松岡雅雄教授(現生命科学研究部シニア教授)、天野将之特任助教(現ヒトレトロウイルス学共同研究センター臨床レトロウイルス学分野)との共同研究で、HBVの複製サイクルを阻害する新規の抗HBV化合物を創製しました。この研究は日本学術振興会科学研究費補助金、AMED創薬等ライフサイエンス研究支援基盤事業(BINDS)の支援のもとで行われたもので、その研究成果は、国際科学誌RSC Medicinal Chemistryに、2023年8月24日にオンライン版で発表されました。
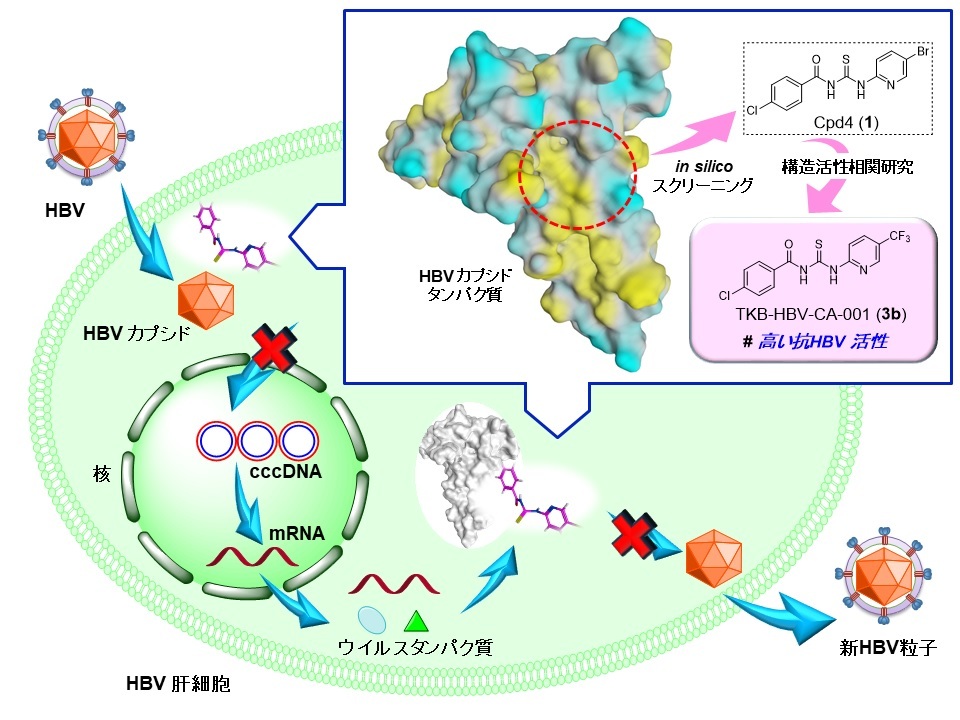
図 抗HBV化合物Cpd4 (1)とその高活性誘導体TKB-HBV-CA-001 (3b)の創出とHBV複製の阻害
研究の背景
B型肝炎の治療の最終目標はHBVを肝臓から排除し、肝炎の再発のない状態を維持することです。そのためには、HBVの排除および増殖過程で感染肝細胞核内に形成されるcccDNA※5の排除が必要です。これまでに、既存のB型肝炎治療薬として、核酸アナログ型逆転写酵素阻害剤、免疫賦活作用を有するPEG化インターフェロンが用いられていますが、これらの薬剤はHBVが増殖する際に肝細胞核内で生じるcccDNAを排除できず、子孫ウイルスの増殖を完全に抑制できないため、HBVの根絶が困難な状況にあります。そのため、既存薬とは異なる新規作用機序を有する治療薬の創製が強く求められているのが現状です。
研究成果の概要
HBcはHBVのDNAを包み込むカプシドを形成するタンパク質であり、cccDNAの転写調節に関わっています。本研究グループは、HBcはB型肝炎の根治に向けた魅力的な標的となりうると考え、研究に着手しました。まず、in silicoスクリーニングによって、HBcの4量体の疎水性ポケットに入り込み、カプシド形成を阻害すると予測される低分子化合物Cpd4 (1)を見出しました。Cpd4 (1)の合成・活性評価の結果、Cpd4 (1)はHBVの増殖の指標となるHBVコア関連抗原 (HBcrAg)を減少させたことに加え、cccDNA量と相関しているHBV 表面抗原 (HBsAg)を減少させました。そこで、Cpd4 (1)をリード化合物として構造活性相関研究を行い、高活性誘導体TKB-HBV-CA-001 (3b)の創出に成功しました。また、活性評価試験等の結果から、高活性なCpd4 (1)誘導体の特徴を明らかにしました。
研究成果の意義
玉村研究グループが創出した新規抗HBV化合物であるCpd4 (1)およびその高活性誘導体TKB-HBV-CA-001 (3b)は、cccDNAの転写調節に関わっているカプシドタンパク質HBcをターゲットとしています。従って、既存のB型肝炎治療薬と違った作用機序を有しており、B型肝炎を根治できる可能性が示唆される有望な治療薬を創出できる可能性があります。また、今回得られた知見を基に、さらに化合物プロフィールが向上した抗HBV剤を創出できる可能性があり、B型肝炎の根治に向けた新薬創製の一助になることが期待されます。
用語解説
※1 B型肝炎ウイルス(HBV): B型肝炎ウイルス(HBV)は、DNAウイルスであり、ヘパドナウイルス科オルトヘパドナウイルス属に属する。また、B型肝炎を起こす原因ウイルスである。
※2 in silicoスクリーニング: 実際の化合物を用いてスクリーニングするのではなく、化合物の構造情報と生物活性の情報をもとにして、化合物の構造式(仮想化合物)だけを用いてコンピュータ上で仮想実験を行い,薬理効果や薬物動態などを予測し,化合物を選別する手法。バーチャルスクリーニングともいう。
※3 HBVカプシドタンパク質(HBc): HBVのDNAを包み込むカプシドを形成するタンパク質であり、カプシドは、HBc の2量体が自己集合することで形成される。HBc の自己集合を改変することにより間接的にHBV ゲノムの合成を阻害することが可能になる。それに加え、HBcはcccDNAの転写調節に関わっていることや、核内へウイルスDNAが侵入するのを阻害する働きをする可能性があるため、HBcを標的とすることで増殖過程の複数のステップを阻害できる可能性がある。また、HBcを形成するアミノ酸配列はゲノムタイプ間で高度に保存されているため、HBcはB型肝炎根治に向けた魅力的な標的になると考えられる。
※4 B型肝炎の有望な治療薬: これまでに、既存のB型肝炎治療薬として、核酸アナログ型逆転写酵素阻害剤、免疫賦活作用を有するPEG化インターフェロンが用いられているが、これらの薬剤はHBVが増殖する際に肝細胞核内で生じるcccDNAを排除できず、子孫ウイルスの増殖を完全に抑制できないため、HBVの根絶が困難である。HBVの排除および増殖過程で感染肝細胞核内に形成されるcccDNAの排除が可能な薬剤が、B型肝炎の根治に向けた有望な治療薬となりうると考えられる。
※5 cccDNA: 肝細胞内に侵入したHBVは、肝細胞核内でDNA修復を受け、不完全な2本鎖DNAから、熱力学的に安定な完全二重鎖DNA(covalently closed circular DNA: cccDNA)を形成する。このcccDNAは核内で安定的に維持され、ウイルス複製の鋳型となる。
※2 in silicoスクリーニング: 実際の化合物を用いてスクリーニングするのではなく、化合物の構造情報と生物活性の情報をもとにして、化合物の構造式(仮想化合物)だけを用いてコンピュータ上で仮想実験を行い,薬理効果や薬物動態などを予測し,化合物を選別する手法。バーチャルスクリーニングともいう。
※3 HBVカプシドタンパク質(HBc): HBVのDNAを包み込むカプシドを形成するタンパク質であり、カプシドは、HBc の2量体が自己集合することで形成される。HBc の自己集合を改変することにより間接的にHBV ゲノムの合成を阻害することが可能になる。それに加え、HBcはcccDNAの転写調節に関わっていることや、核内へウイルスDNAが侵入するのを阻害する働きをする可能性があるため、HBcを標的とすることで増殖過程の複数のステップを阻害できる可能性がある。また、HBcを形成するアミノ酸配列はゲノムタイプ間で高度に保存されているため、HBcはB型肝炎根治に向けた魅力的な標的になると考えられる。
※4 B型肝炎の有望な治療薬: これまでに、既存のB型肝炎治療薬として、核酸アナログ型逆転写酵素阻害剤、免疫賦活作用を有するPEG化インターフェロンが用いられているが、これらの薬剤はHBVが増殖する際に肝細胞核内で生じるcccDNAを排除できず、子孫ウイルスの増殖を完全に抑制できないため、HBVの根絶が困難である。HBVの排除および増殖過程で感染肝細胞核内に形成されるcccDNAの排除が可能な薬剤が、B型肝炎の根治に向けた有望な治療薬となりうると考えられる。
※5 cccDNA: 肝細胞内に侵入したHBVは、肝細胞核内でDNA修復を受け、不完全な2本鎖DNAから、熱力学的に安定な完全二重鎖DNA(covalently closed circular DNA: cccDNA)を形成する。このcccDNAは核内で安定的に維持され、ウイルス複製の鋳型となる。
論文情報
掲載誌:RSC Medicinal Chemistry
論文タイトル: Development of Anti-HBV Agents Targeting HBV Capsid Proteins
DOI:https://doi.org/10.1039/D3MD00258F
論文タイトル: Development of Anti-HBV Agents Targeting HBV Capsid Proteins
DOI:https://doi.org/10.1039/D3MD00258F
研究者プロフィール

玉村 啓和 (タマムラ ヒロカズ) Tamamura, Hirokazu
東京医科歯科大学 生体材料工学研究所
メディシナルケミストリー分野 教授
・研究領域
創薬化学、ペプチド化学、ケミカルバイオロジー、有機化学
問い合わせ先
<研究に関すること>
東京医科歯科大学 生体材料工学研究所
メディシナルケミストリー分野 玉村啓和(タマムラヒロカズ)
E-mail:tamamura.mr[@]tmd.ac.jp
<報道に関すること>
東京医科歯科大学 総務部総務秘書課広報係
〒113-8510 東京都文京区湯島1-5-45
E-mail:kouhou.adm[@]tmd.ac.jp
※E-mailは上記アドレス[@]の部分を@に変えてください。

