東京医科歯科大学は、2024年10月に東京工業大学と統合し、東京科学大学(Science Tokyo)となりました。本サイトの情報は、順次、Science Tokyoのサイトに移行していきます。公開されているページは東京科学大学の情報として有効なものです。
「 非ウイルス性肝細胞がんの特異的予後予測因子SFXN1の同定と脂肪毒性に対する耐性機序の解明 」【田中真二 教授、島田周 助教】
「 非ウイルス性肝細胞がんの特異的予後予測因子SFXN1の同定と
脂肪毒性に対する耐性機序の解明 」
― 非ウイルス性肝細胞がん予防治療への応用に期待 ―
ポイント
- 近年、メタボリックシンドロームを背景因子とする非ウイルス性肝細胞がんが増加していますが、その予後予測因子は不明であり、発症メカニズムも解明されていません。
- 本研究では大規模遺伝子発現解析を行い、非ウイルス性肝細胞がんの特異的予後予測因子として、ミトコンドリア内膜トランスポーターSFXN1を同定しました。
- SFXN1の不活性化は脂肪負荷時における脂肪の取り込み・活性酸素種の産生を抑制し、脂肪毒性を軽減し、生体内における脂肪負荷耐性に寄与することを明らかにしました。
- SFXN1は非ウイルス性肝細胞がんの予後予測だけでなく、発症メカニズムの解明により予防治療などへの応用に役立つ可能性があります。
東京医科歯科大学 大学院医歯学総合研究科 分子腫瘍医学分野の田中真二教授、島田周助教、秋山好光講師、波多野恵助教、八木宏平大学院生の研究グループは、同肝胆膵外科学分野の田邉稔教授との共同研究で、非ウイルス性肝細胞がんの特異的予後予測因子としてミトコンドリア内膜トランスポーターSFXN1を同定し、SFXN1の不活性化が脂肪負荷時における脂肪の取り込み・活性酸素種(ROS)の産生を抑制して、脂肪毒性(lipotoxicity)を軽減し、生体内の脂肪負荷耐性に寄与することを明らかにしました。この研究は文部科学省科学研究費補助金、国立研究開発法人日本医療研究開発機構(AMED)「肝炎等克服実用化研究事業」ならびに高松宮妃癌研究基金助成金の支援のもとでおこなわれたもので、その研究成果は、国際科学誌Scientific Reportsに、2023年6月9日にオンライン版で発表されました。
研究の背景
肝細胞がんはB型肝炎ウイルスやC型肝炎ウイルスの感染、アルコール多飲、メタボリックシンドロームなど様々な病因を背景とする複雑な疾患です。B型肝炎ウイルスワクチンの普及とC型肝炎ウイルス治療薬の開発によりウイルス性肝細胞がんは減少してきていますが、糖尿病や肥満などのメタボリックシンドローム、非アルコール性脂肪性肝疾患(NAFLD)や非アルコール性脂肪性肝炎(NASH)を原因とする非ウイルス性肝細胞がんはむしろ増加傾向となっています。しかし、非ウイルス性肝細胞がんの予後予測因子は報告されておらず、発症メカニズムもその詳細は解明されていません。そこで、本研究グループはCancer Genome Atlas Research Network(TCGA)から提供されている遺伝子発現公開データベースを用いて、非ウイルス性肝細胞がん患者の予後と相関し、腫瘍部分で発現低下している遺伝子を探索し、非ウイルス性肝細胞がん発症における役割を解析しました。
研究成果の概要
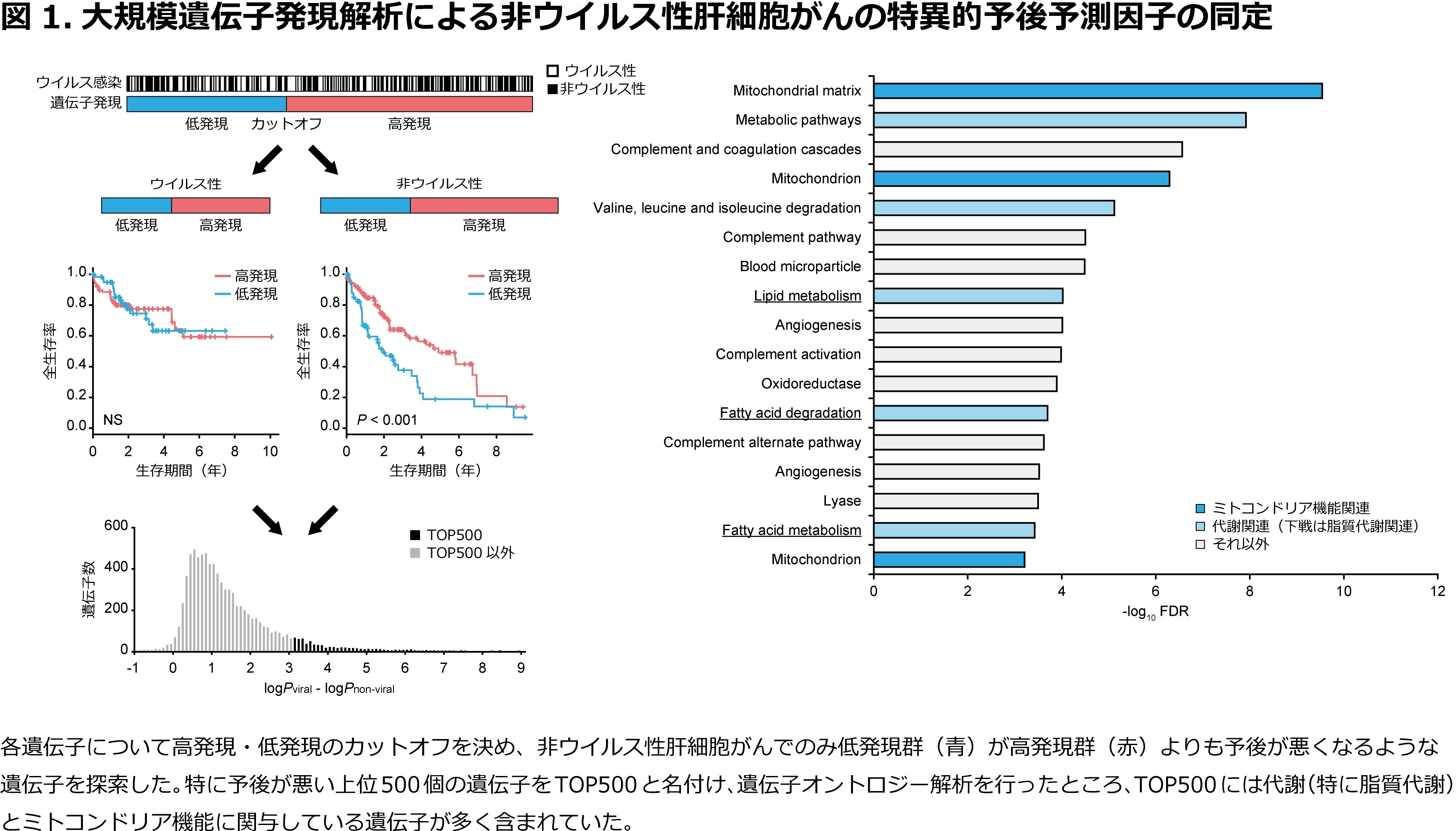
TCGAデータを用いて、370名の肝細胞がん患者(ウイルス性153名、非ウイルス性217名)の20,531個の遺伝子について大規模遺伝子発現解析を行いました。非ウイルス性肝細胞がんにおいてのみ発現低下群が予後不良となるような8,190個の遺伝子を抽出し、予後との相関が強い上位500個の遺伝子をTOP500と名付けました。遺伝子オントロジー解析※1を行ったところ、TOP500は脂質代謝とミトコンドリア機能に関与していることを見出しました。そこで、TOP500に含まれるミトコンドリア内膜関連遺伝子の中で最も予後との相関が強い遺伝子SFXN1に注目しました(図1)。
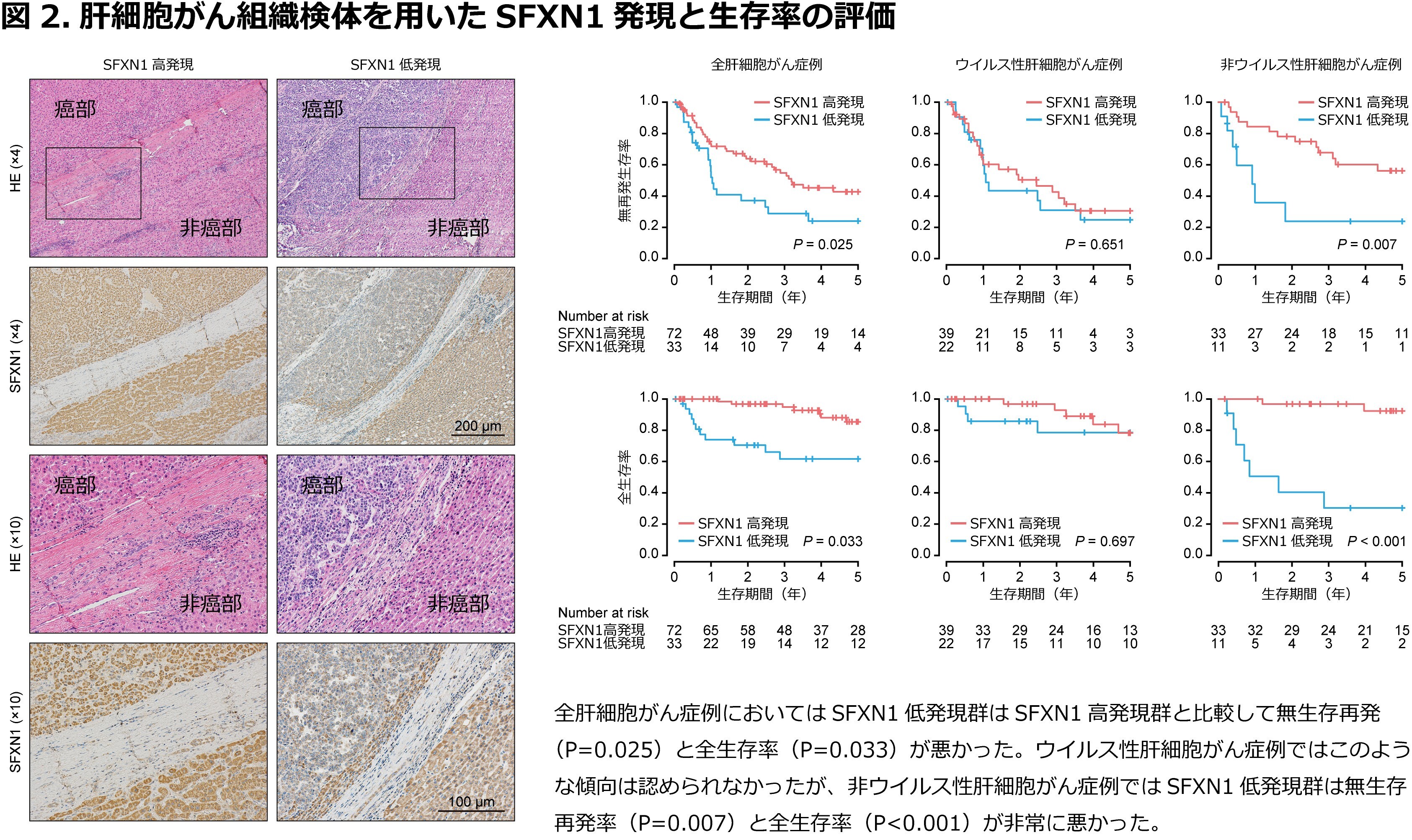
本学で切除された肝細胞がん組織検体105症例について免疫染色を行ったところ、33症例においてSFXN1蛋白質の発現低下が認められました。全肝細胞がん症例において、SFXN1低発現群はSFXN1高発現群と比較して無再発生存率(P=0.025)と全生存率(P=0.033)が悪いことがわかりました。サブ解析によりウイルス性肝細胞がんではこのような傾向は認められませんでしたが、非ウイルス性肝細胞がんではSFXN1低発現群は無再発生存率(P=0.007)と全生存率(P<0.001)が非常に悪いこともわかりました(図2)。
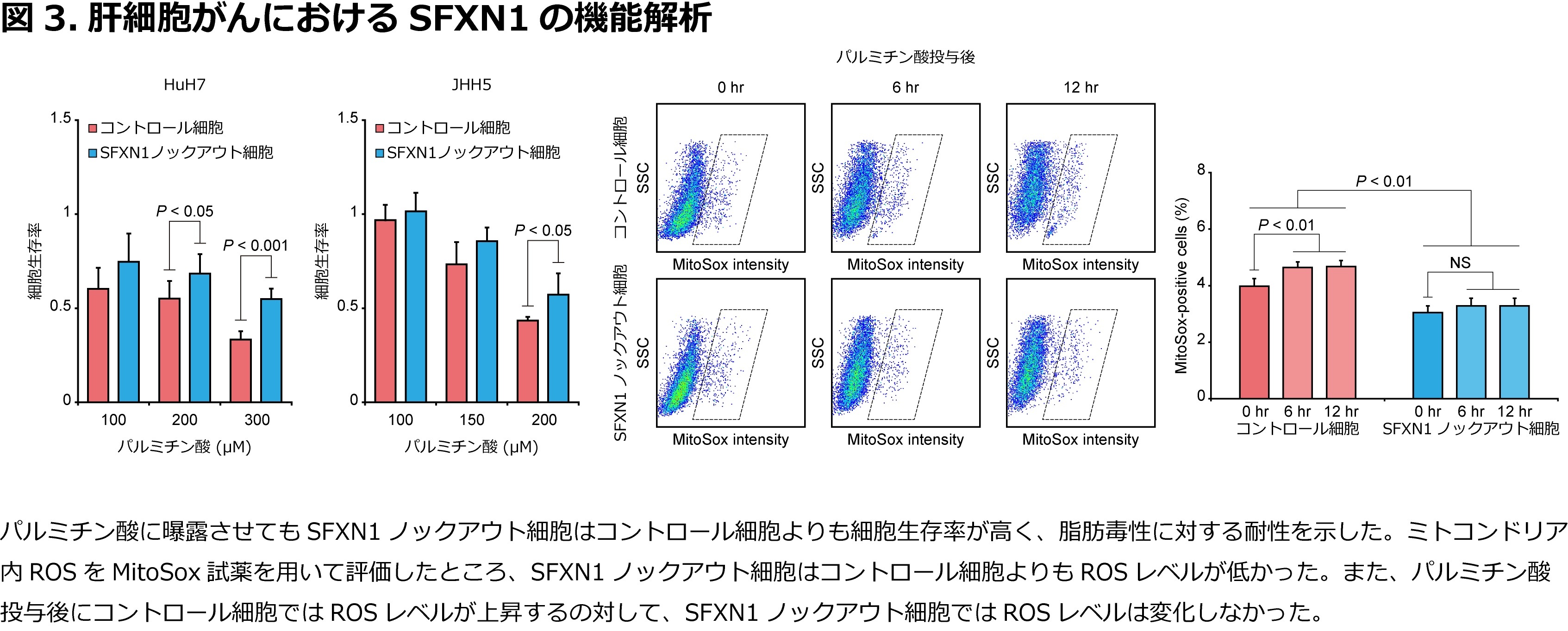
次にCRISPR/Cas9システム※2を用いてヒト肝細胞がん株においてSFXN1をノックアウトしました。SFXN1ノックアウト細胞はコントロール細胞と比較しても細胞増殖能に差はありませんでした。しかし、飽和脂肪酸であるパルミチン酸に曝露させると、SFXN1ノックアウト細胞はコントロール細胞よりも生存率が高いことがわかりました。パルミチン酸投与後にオイルレッド染色※3を行ったところ、SFXN1ノックアウト細胞はコントロール細胞よりも脂肪の取り込みが少ないことがわかりました。パルミチン酸投与後にミトコンドリア内ROSを評価したところ、SFXN1ノックアウト細胞はROSレベルが低いこともわかりました(図3)。以上より、SFXN1の不活性化により、脂肪を負荷しても細胞は脂肪を取り込みにくくなり、ミトコンドリア内ROS産生も抑制し、脂肪毒性の影響を受けにくくなることがわかりました。
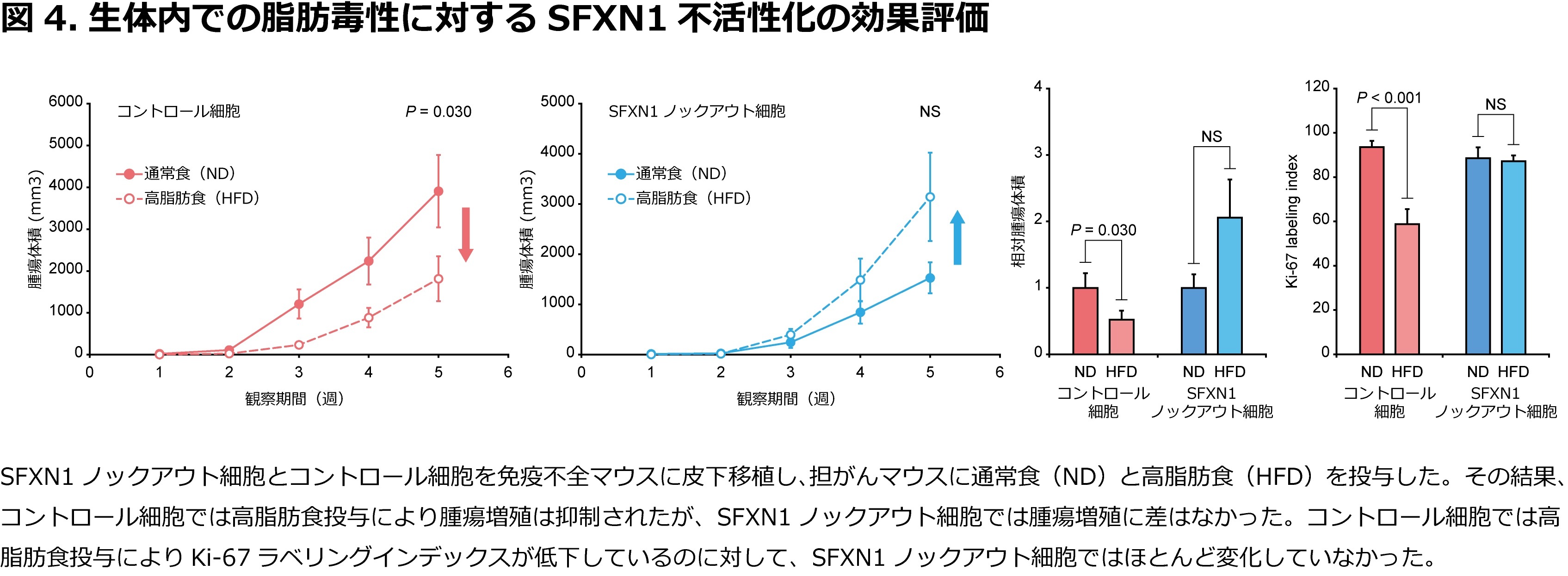
生体内での脂肪毒性を評価するためにSFXN1ノックアウト細胞とコントロール細胞を免疫不全マウスに皮下移植し、担がんマウスに通常食と高脂肪食を投与しました。その結果、コントロール細胞では高脂肪食投与群は通常食投与群よりも腫瘍が小さくなりましたが、SFXN1ノックアウト細胞ではこのような現象は認められませんでした(図4)。腫瘍組織について免疫染色を行ったところ、コントロール細胞では高脂肪食投与によりKi-67ラベリングインデックス※4が低下しているのに対して、SFXN1ノックアウト細胞ではほとんど変化せず、SFXN1ノックアウト細胞では脂肪負荷による細胞増殖抑制が誘導されていないと考えられました。以上より、SFXN1の不活性化は生体内でも脂肪毒性の軽減に寄与していることが示唆されました。
研究成果の意義
SFXN1はアミノ酸であるセリンをミトコンドリア内膜に輸送するトランスポーターであり、セリンワンカーボン代謝経路※5において重要な役割を果たしている遺伝子です。SFXN1は肝臓で高発現しており、肝臓ではセリンワンカーボン代謝経路からNADPHを産生し脂肪酸を合成していることが報告されています。実際、マウスにおいてセリンワンカーボン代謝経路を阻害すると肝臓での脂肪酸合成が減少し、脂肪肝が改善することもわかっています。また、SFXN1は細胞質内の鉄をミトコンドリアに供給し、ミトコンドリア内ROS産生とフェロトーシスに関与していることも知られています。フェロトーシスは細胞内ROSが増加すると鉄を触媒として過酸化膜脂質を生成し、細胞死を誘導するという最近発見されたプログラム細胞死の一つであり、肝障害に対する治療標的の一つとして注目されています。SFXN1はROS産生・脂質代謝・鉄代謝に関与する遺伝子であるので、SFXN1の不活性化はフェロトーシスを阻害することでメタボリックシンドローム・脂肪肝という環境下においてもがん細胞が生存・増殖するのを可能にしていると考えられます。
以上のように、SFXN1に関する本研究は非ウイルス性肝細胞がんの予後予測だけでなく、発症メカニズムの解明により予防治療などへの応用に役立つ可能性があります。
用語解説
※1遺伝子オントロジー解析
遺伝子個々に注目するのではなく、遺伝子群に共通する分子機能・細胞構成・生体反応に注目し、メカニズムを明らかにする方法。
※2CRISPR/Cas9システム
ゲノム中で任意の領域を切断できる遺伝子改変システム。遺伝子内の標的配列に相補的な配列を含むguide RNAとCas9蛋白質を細胞内で発現させ、遺伝子内の標的配列が切断、非相同末端結合により修復されるときにフレームシフト変異が生じ、遺伝子が機能喪失する。
※3オイルレッド染色
細胞内の脂肪を染色する方法。オイルレッドは無極性・脂溶性であるため、細胞内の脂肪に溶け込み、赤色を呈する。
※4Ki-67ラベリングインデックス
Ki-67は細胞増殖時に核内に発現する蛋白質であり、腫瘍組織中のKi-67陽性細胞の比率をKi-67ラベリングインデックスという。細胞増殖能を評価する指標の一つ。
※5セリンワンカーボン代謝経路
セリンに由来する炭素原子1個が葉酸回路・メチオニン回路により他の代謝産物に受け渡されていく経路。メチル基転移などに関与する。
論文情報
研究者プロフィール
田中真二 (タナカ シンジ) Tanaka Shinji
東京医科歯科大学 大学院医歯学総合研究科
分子腫瘍医学分野 教授
・研究領域
分子腫瘍医学、消化器外科学
島田周 (シマダ シュウ) Shimada Shu
東京医科歯科大学 大学院医歯学総合研究科
分子腫瘍医学分野 助教
・研究領域
分子腫瘍医学、システム生物学
問い合わせ先
<研究に関すること>
東京医科歯科大学大学院医歯学総合研究科
分子腫瘍医学分野 島田周(シマダ シュウ)
田中真二(タナカ シンジ)
E-mail: shimada.monc@tmd.ac.jp
tanaka.monc@tmd.ac.jp
<報道に関すること>
東京医科歯科大学 総務部総務秘書課広報係
〒113-8510 東京都文京区湯島1-5-45
E-mail:kouhou.adm[@]tmd.ac.jp
※E-mailは上記アドレス[@]の部分を@に変えてください。
関連リンク
プレス通知資料PDF
「非ウイルス性肝細胞がんの特異的予後予測因子SFXN1の同定と脂肪毒性に対する耐性機序の解明」