「 新規CRISPR screeningを用いた薬剤耐性の解明 」【倉田盛人 講師】
公開日:2023.6.1
「 新規CRISPR screeningを用いた薬剤耐性の解明 」
― がん微小環境における細胞間相互作用の理解 ―
― がん微小環境における細胞間相互作用の理解 ―
ポイント
- がんの再発の原因である微小環境を解析できる新しいスクリーニング法を開発しました。
- 治療抵抗性を示す白血病や膵癌などの新規治療法開発への応用が期待できます。
東京医科歯科大学 大学院医歯学総合研究科 包括病理学分野の倉田盛人講師と杉田佳祐大学院生の研究グループは、がん微小環境のメカニズムを解明する新規スクリーニング法を開発しました。この研究は文部科学省科学研究費補助金の支援のもとでおこなわれたもので、その研究成果は、Springer Natureが発行する国際科学誌Communications Biology (コミュニケーションズ バイオロジー) に、2023年6月1日にオンライン版で発表されました。
研究の背景
がんの治療抵抗性は、現在でもがん治療における大きな問題であり、薬剤耐性機構※1の解明は克服すべき重要な課題です。がんをとりまく「がん微小環境」※2も薬剤耐性に寄与することが知られており、研究上で大きな焦点となっています。
これまでの「がん微小環境」に関する多くの報告が主に予後不良のがんそのものを主体とした研究であったことに対し、本研究チームでは、包括的に腫瘍周囲支持細胞による薬剤耐性誘導のメカニズムを解明するために、新たなCRISPR screening法※3の確立を行いました。
これまでの「がん微小環境」に関する多くの報告が主に予後不良のがんそのものを主体とした研究であったことに対し、本研究チームでは、包括的に腫瘍周囲支持細胞による薬剤耐性誘導のメカニズムを解明するために、新たなCRISPR screening法※3の確立を行いました。
研究成果の概要
従来のCRISPR screening法では、薬剤曝露などの条件下でランダム変異を誘発するCRISPRライブラリーを用いて腫瘍細胞の選択的な生存/死滅を検出することにより、薬剤耐性候補遺伝子が同定されてきました。しかし、「がん微小環境」などの周辺環境からの細胞間相互作用による薬剤耐性の場合、細胞間相互作用による薬剤耐性の責任候補遺伝子の同定は困難でありました。これは、周囲の支持細胞にランダムな変異が誘導されても、支持細胞自身は薬剤下で選択的に生存/死滅することがないためです。そこで、本研究チームでは薬剤耐性を誘導できる支持細胞を分離するシステムを併用し、「間接的CRISPR screening」と名付けました(図1)。
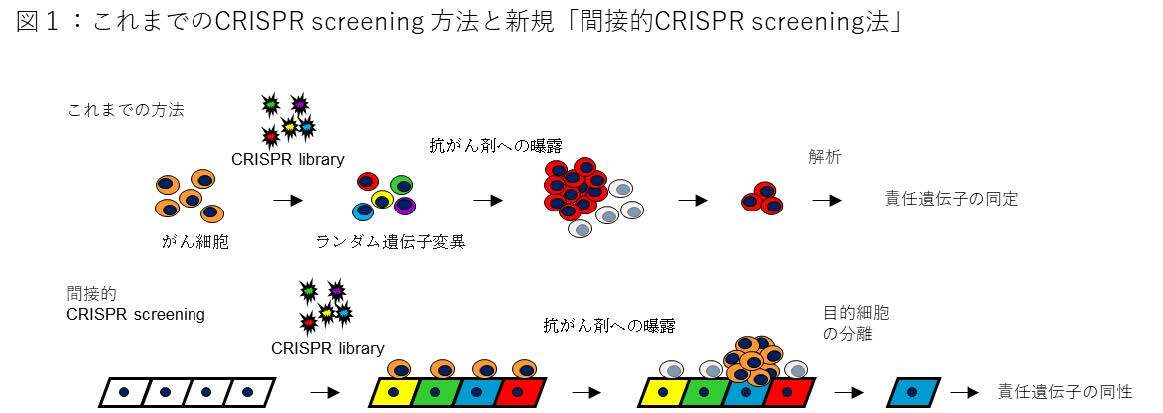
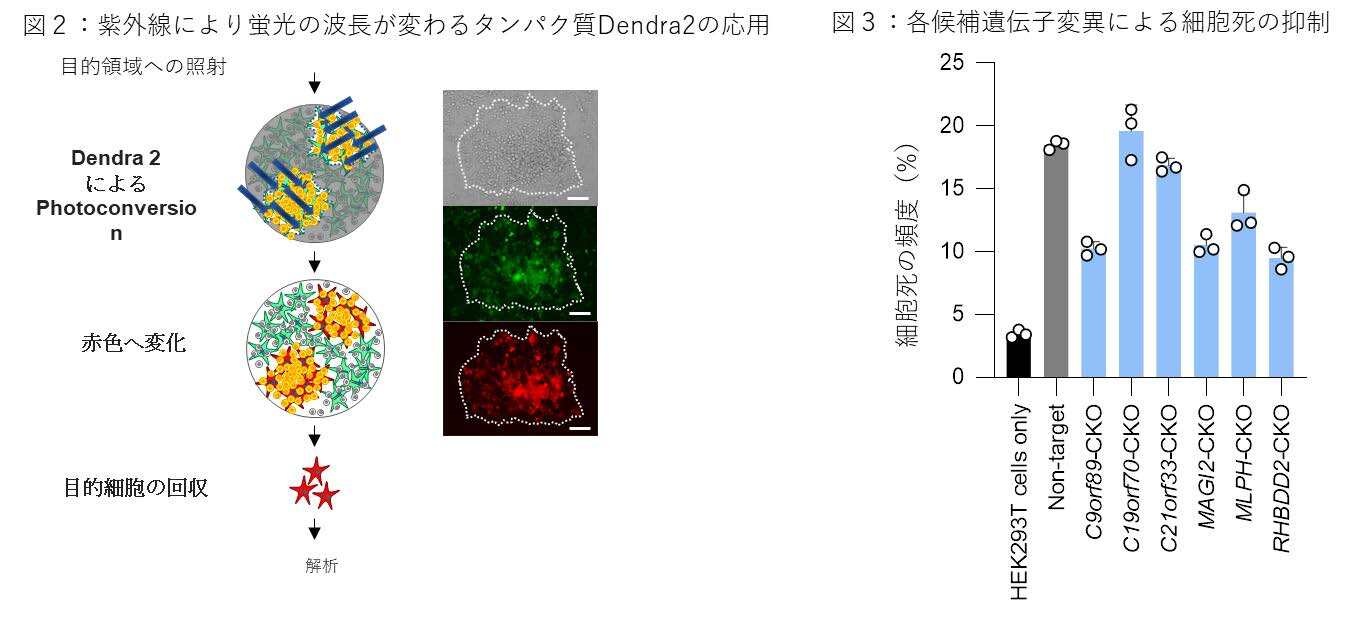
具体的には、紫外線により蛍光の波長が変わる(Photoconversion)タンパク質Dendra2を支持細胞に組み込んでおき、その支持細胞と接触することにより、腫瘍細胞が薬剤中で生存できることができる状態を誘導し、その薬剤耐性を誘導した責任支持細胞(腫瘍細胞が増殖した細胞の支えになっている細胞)に紫外線を照射し、蛍光波長を緑色から赤色に変換させることにより、薬剤耐性を誘導できなかった細胞と区別し、責任細胞を回収・解析しました(図2)。
回収した細胞から責任となる候補遺伝子を同定しました。得られた候補遺伝子に対して、抗癌剤により細胞死の抑制ができるか、再度支持細胞に各候補遺伝子の欠損を誘導し、腫瘍細胞と共培養する確認実験を行ったところ、候補遺伝子の中でC9orf89、MAGI2、MLPH、RHBDD2において細胞死の抑制がみられました(図3)。
回収した細胞から責任となる候補遺伝子を同定しました。得られた候補遺伝子に対して、抗癌剤により細胞死の抑制ができるか、再度支持細胞に各候補遺伝子の欠損を誘導し、腫瘍細胞と共培養する確認実験を行ったところ、候補遺伝子の中でC9orf89、MAGI2、MLPH、RHBDD2において細胞死の抑制がみられました(図3)。
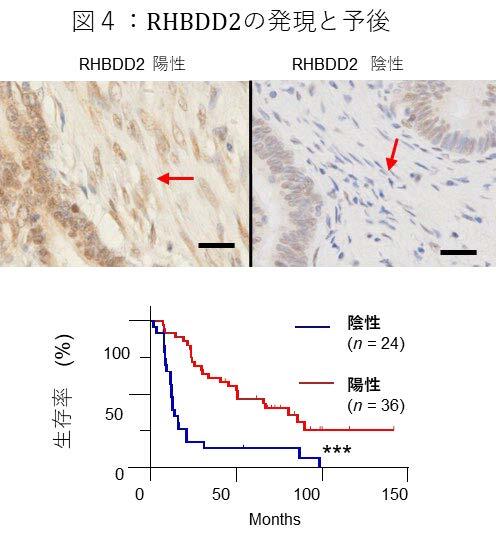
さらなる解析の為、腫瘍細胞の周囲に間質細胞が豊富で治療抵抗性をしめす膵癌検体を用いて解析しました。実際に、候補遺伝子の中でRHBDD2において、癌周囲間質細胞での発現陰性群では陽性群と比較して有意に全生存期間が短縮していることが判明しました(図4)。この結果は、今回の「間接的CRISPR screening」で同定されたRHBDD2が、腫瘍周囲の間質で発現が欠損することにより、抗癌剤の薬剤耐性を誘導し、生存期間が短縮している可能性を示唆しています。
研究成果の意義
本研究では、紫外線照射により光変換可能な蛍光タンパク質Dendra2を用いた新たなCRISPR screeningシステムである「間接的CRISPR screening法」を確立し、細胞間相互作用で誘導される新たな薬剤耐性責任分子を同定することに成功しました。
用語解説
※1 薬剤耐性・・・・・・・・腫瘍細胞に対して抗がん剤が効かなくなる状態。
※2 がん微小環境・・・・・・・がん細胞や特にがん幹細胞の環境で、間質細胞などがん細胞以外の成分からも構成される。
※3 CRISPR screening・・・・・・・・CRISPR(遺伝子編集技術)により、数万種類の遺伝子にランダムに変異を加え、個々の変異から薬剤耐性などの機能変化を解析するスクリーニング法。
※2 がん微小環境・・・・・・・がん細胞や特にがん幹細胞の環境で、間質細胞などがん細胞以外の成分からも構成される。
※3 CRISPR screening・・・・・・・・CRISPR(遺伝子編集技術)により、数万種類の遺伝子にランダムに変異を加え、個々の変異から薬剤耐性などの機能変化を解析するスクリーニング法。
論文情報
掲載誌:Communications Biology
論文タイトル:Indirect CRISPR screening with photoconversion revealed key factors of drug resistance with cell-cell interactions
DOI:http://doi.org/10.1038/s42003-023-04941-9
論文タイトル:Indirect CRISPR screening with photoconversion revealed key factors of drug resistance with cell-cell interactions
DOI:http://doi.org/10.1038/s42003-023-04941-9
研究者プロフィール

杉田 佳祐 (スギタ ケイスケ) Sugita Keisuke
東京医科歯科大学 大学院医歯学総合研究科
包括病理学分野 大学院生
・研究領域
薬剤耐性
CRISPR screening

倉田 盛人 (クラタ モリト) Kurata Morito
東京医科歯科大学 大学院医歯学総合研究科
包括病理学分野 講師
・研究領域
薬剤耐性
CRISPR screening
がん遺伝子
東京医科歯科大学 大学院医歯学総合研究科
包括病理学分野 講師
・研究領域
薬剤耐性
CRISPR screening
がん遺伝子
問い合わせ先
<研究に関すること>
東京医科歯科大学大学院医歯学総合研究科
包括病理学分野 倉田盛人(クラタ モリト)
E-mail:kurata.pth2[@]tmd.ac.jp
<報道に関すること>
東京医科歯科大学 総務部総務秘書課広報係
〒113-8510 東京都文京区湯島1-5-45
E-mail:kouhou.adm[@]tmd.ac.jp
※E-mailは上記アドレス[@]の部分を@に変えてください。

