「脂質結合型DNA /RNAヘテロ2本鎖核酸による、脳梗塞病巣への効果的な薬剤送達と遺伝子抑制を達成」【横田隆徳 教授】
「脂質結合型DNA /RNAヘテロ2本鎖核酸による、脳梗塞病巣への効果的な薬剤送達と遺伝子抑制を達成」
― 脳梗塞の新たな治療法への一歩―
ポイント
- 研究グループがこれまでに独自に開発した次世代核酸医薬である「DNA /RNAヘテロ2本鎖核酸(HDO)」※1に脂質リガンドを結合し、脳梗塞の動物モデルへの治療効果を検証しました。
- 脳梗塞超急性期には、病巣において血管や脳神経細胞内への脂質受容体を介した物質の取り込みが通常よりも亢進していることを発見しました。脂質型送達分子(リガンド)を結合させたHDOの効果はこの現象を利用することで成り立っており、従来のアンチセンス核酸※2と比較して、病巣への薬剤送達・遺伝子抑制効果を飛躍的に向上させることに成功しました。
- 超急性期の脳梗塞病巣に対して静脈投与による薬剤送達が極めて困難であるという従来の課題を克服しえた脂質リガンド結合HDOにより、脳梗塞治療への応用が期待されます。
研究の背景
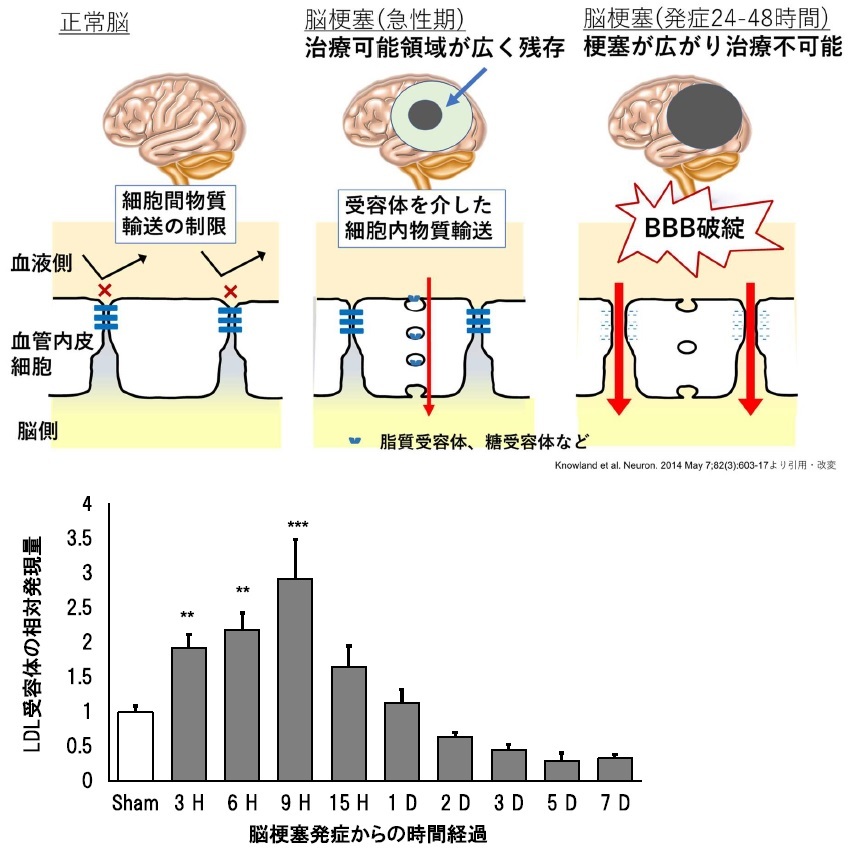
上図:脳梗塞と脳血管関門 (BBB)
超急性期脳梗塞では、治療可能な領域が広く残存しているが、BBBのバリア機能が保たれているため虚血部位への薬剤輸送が制限されている。 発症24時間以降は、物質通過は可能だが梗塞が完成してしまっており脳神経細胞のダメージは不可逆的な状態である。
下図:超急性期脳梗塞における病変部位での脂質受容体の発現亢進
BBBでの細胞間物質輸送の他に、脳血管内皮細胞は特定の物質を受容体などで介して輸送する細胞内輸送が知られており、薬物送達のもう一つのルートとなり得る。研究グループでは、細胞内輸送を担う受容体の一つである、脂質受容体がマウス脳梗塞モデルにおいて超急性期の病変部位でのみ発現が増加することを発見し(下図)、この超急性期に見られる細胞内輸送亢進現象を利用して正常脳では不可能な有効量の薬物を脳実質内に送達することが出来るのではないかと考えた。
研究成果の概要
さらに、ビタミンE結合DNA/RNA ヘテロ2本鎖核酸を投与した脳梗塞マウスでは、脳梗塞に伴う神経症状や、脳梗塞のサイズ、血管の再生なども有意に変化し、有効な治療効果が得られることも確認しました。なお、この薬剤の送達や遺伝子抑制効果には、脳梗塞部位での脂質受容体の発現の亢進が関与していることも確認できました。
また、近年、核酸医薬で臓器障害などの副作用が問題となっていますが、ビタミンE結合DNA/RNA ヘテロ2本鎖核酸は、脳梗塞マウスに投与しても肝臓や腎臓への障害は認められませんでした。
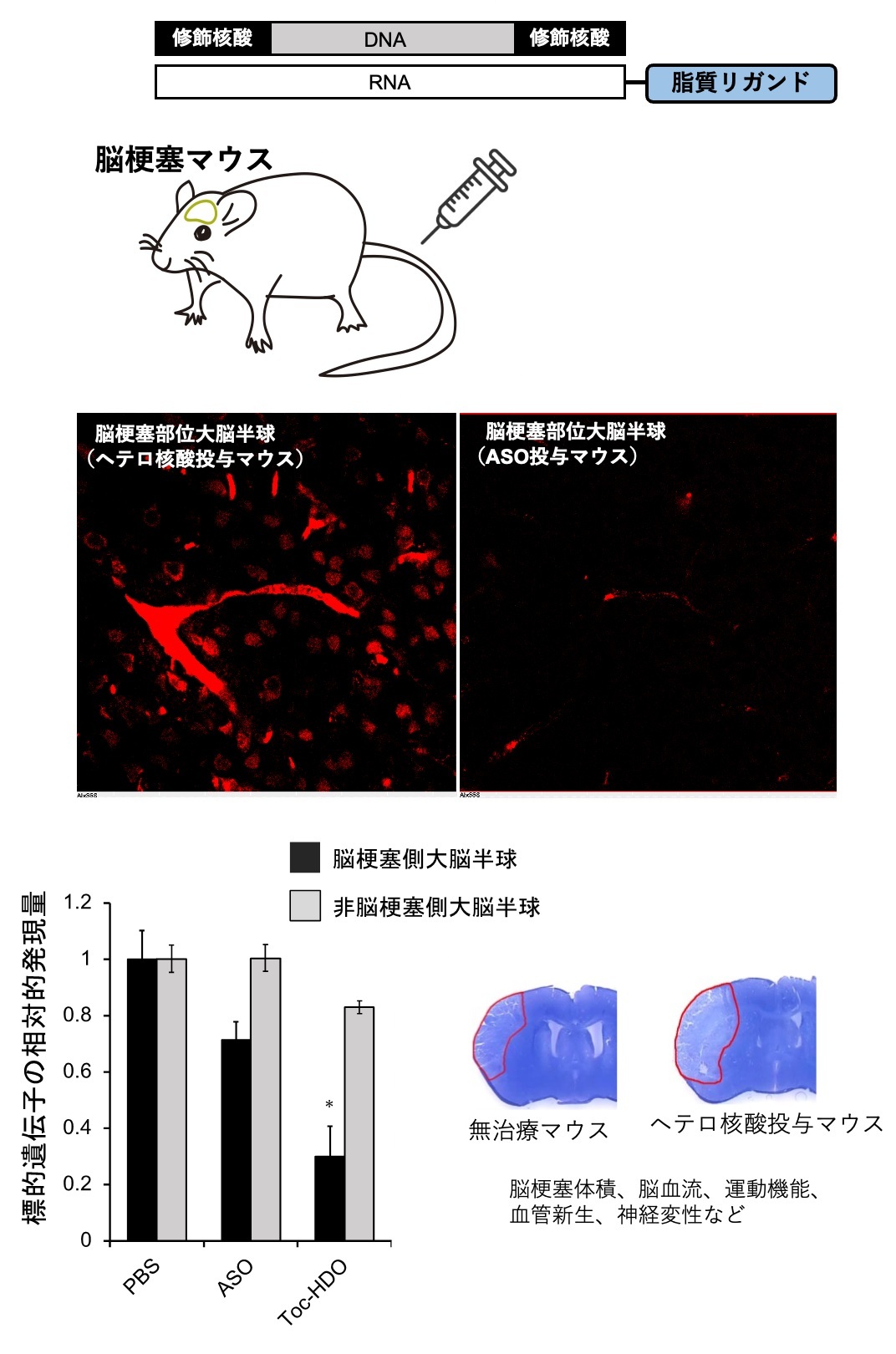
上:脳梗塞モデルマウス超急性期に脂質リガンド結合2本鎖ヘテロ核酸を静脈投与した。
中:脂質リガンド付きヘテロ核酸は脳梗塞部位選択的に薬剤送達され、その効果はアンチセンス核酸と比較して格段に優れている。
左下:脂質リガンド付きヘテロ核酸は強い遺伝子抑制効果を梗塞病巣選択的に示した。
右下:脂質リガンド付きヘテロ核酸は脳梗塞の表現型も変化させた。
研究成果の意義
核酸医薬は脊髄筋萎縮症などに実際臨床応用され始めていますが、薬剤の投与方法は髄腔内への直接投与です。脳梗塞急性期の患者さんでは、プラスミノーゲンアクチベーターや抗血小板薬など血液を固まりにくくする薬の投与をする場合が多く、髄腔内投与は出血のリスクが高まります。脂質リガンド結合DNA/RNA ヘテロ2本鎖核酸は、経静脈的投与により投与が可能であることは合併症予防の観点からも非常に優れているといえます。
用語解説
※1 DNA/RNA ヘテロ 2 本鎖核酸 (HDO)
核酸医薬としての活性を有する アンチセンス核酸核酸分子 (DNA 鎖)に対して相補的なRNA鎖を結合させた DNA/RNA ヘテロ2本鎖構造を有する、研究グループが独自に開発した新規構造の核酸医薬技術。
※2 アンチセンス核酸
細胞内に存在する RNA(mRNA、pre-RNA、miRNA など)を標的とする核酸医薬で、DNA 鎖を基本構造とし様々な化学修飾が施されている。既存の低分子医薬や抗体医薬では標的にできない細胞内の RNA を標的にすることが可能で、その標的 RNA から翻訳される疾患に係わるタンパク質量を一過性に機能を制御することが可能であることから、これまで治療法のなかった疾患の治療薬として注目されている。主な承認薬として脊髄性筋萎縮症に対するヌシネルセンや家族性ポリアミロイドニューロパチーに対するイノテルセン(米国、欧州)などがあり、現在も複数の臨床治験が進行中である。
※3 脳血液管門(BBB)
脳実質組織とそこに酸素と栄養を供給する血管との間には、血液脳関門 (BBB) と呼ばれるバリアが存在する。BBBは解剖学的には,脳毛細血管内皮細胞,アストロサイトおよびペリサイトの3種類の細胞が機能的に一体となって構築している。BBBの存在により脳組織を外因物質から保護している。多くのトランスポーターによって、栄養素(グルコース、アミノ酸など)は選択的に血液脳関門を透過する。一方で水溶性の高い物質あるいはタンパク質などの大きな分子はこの関門を透過し難く、核酸医薬自体は通過しないことがよく知られている。脳内に薬剤を送達させるには、この関門の透過することが必須である。
論文情報
掲載誌:Molecular Therapy
論文タイトル: Preferential delivery of lipid-ligand conjugated DNA/RNA heteroduplex oligonucleotide to ischemic brain in hyperacute stage
DOI:https://doi.org/10.1016/j.ymthe.2023.01.016
研究者プロフィール

横田 隆徳 (ヨコタ タカノリ) Takanori Yokota
東京医科歯科大学 脳神経病態学分野 教授
・研究領域
神経内科学、脳血管障害、核酸医薬

東京医科歯科大学 脳神経病態学分野 准教授
・研究領域
神経内科学、脳血管障害、核酸医薬

東京医科歯科大学 脳神経病態学分野 元特任研究員
・研究領域
神経内科学、脳血管障害、核酸医薬

東京医科歯科大学 脳神経病態学分野 大学院生
・研究領域
神経内科学、脳血管障害、核酸医薬
問い合わせ先
<研究に関すること>
東京医科歯科大学 大学院医歯学総合研究科
脳神経病態学分野横田 隆徳 (ヨコタ タカノリ)
E-mail:tak-yokota.nuro[@]tmd.ac.jp
<報道に関すること>
東京医科歯科大学 総務部総務秘書課広報係
〒113-8510 東京都文京区湯島1-5-45
E-mail:kouhou.adm[@]tmd.ac.jp
※E-mailは上記アドレス[@]の部分を@に変えてください。

