「 ZNF185は血管バリアを構築し血管外への過剰な物質の漏出を抑制する 」【安藤史顕 助教】
― PKA/RhoAのシグナル伝達を仲介する分子の発見 ―
ポイント
- プロテインキナーゼA(PKA)シグナルは血管内皮細胞においてRhoA※1活性を阻害し、細胞に収縮力を発生させるstress fiber※2の形成を抑制することで、強固な細胞間接着を維持し血管のバリア機能を高めています。
- PKAシグナルの活性と特異性はPKAが結合するタンパクに依存しますが、ZNF185※3がPKAの足場タンパクであることを新規に同定し、PKAからRhoA へのシグナル伝達を仲介する役割があることを明らかにしました。
- ZNF185を介した血管バリア維持機構の解明により、癌や糖尿病、敗血症、アナフィラキシーなどの血管バリア機能が破綻する疾患の治療開発につながることが期待されます。
研究の背景
PKAシグナルは血管バリア機能を高める主要な因子として知られており、RhoA活性を阻害することで細胞間接着を強固にしますが、細胞内においてPKAの局在と活性がどのように制御されているかは不明でした。
研究成果の概要
ZNF185の存在下では、PKAが活性化されるとRhoA活性を抑制して血管内皮細胞同士の強固な細胞接着が保持されます。しかし、ZNF185が消失すると足場を失ったPKAが細胞膜領域に存在できず、RhoA活性の上昇により細胞を収縮させるstress fiberが形成され血管透過性が亢進します(図1)。ZNF185の相同体※4であるZfp185をノックアウトしたマウスの解析でも、血管透過性が亢進しました(図2)。
本研究により、血管内皮細胞においてZNF185はPKA/RhoAのシグナル伝達を仲介する足場の役割をしていることが明らかになりました。
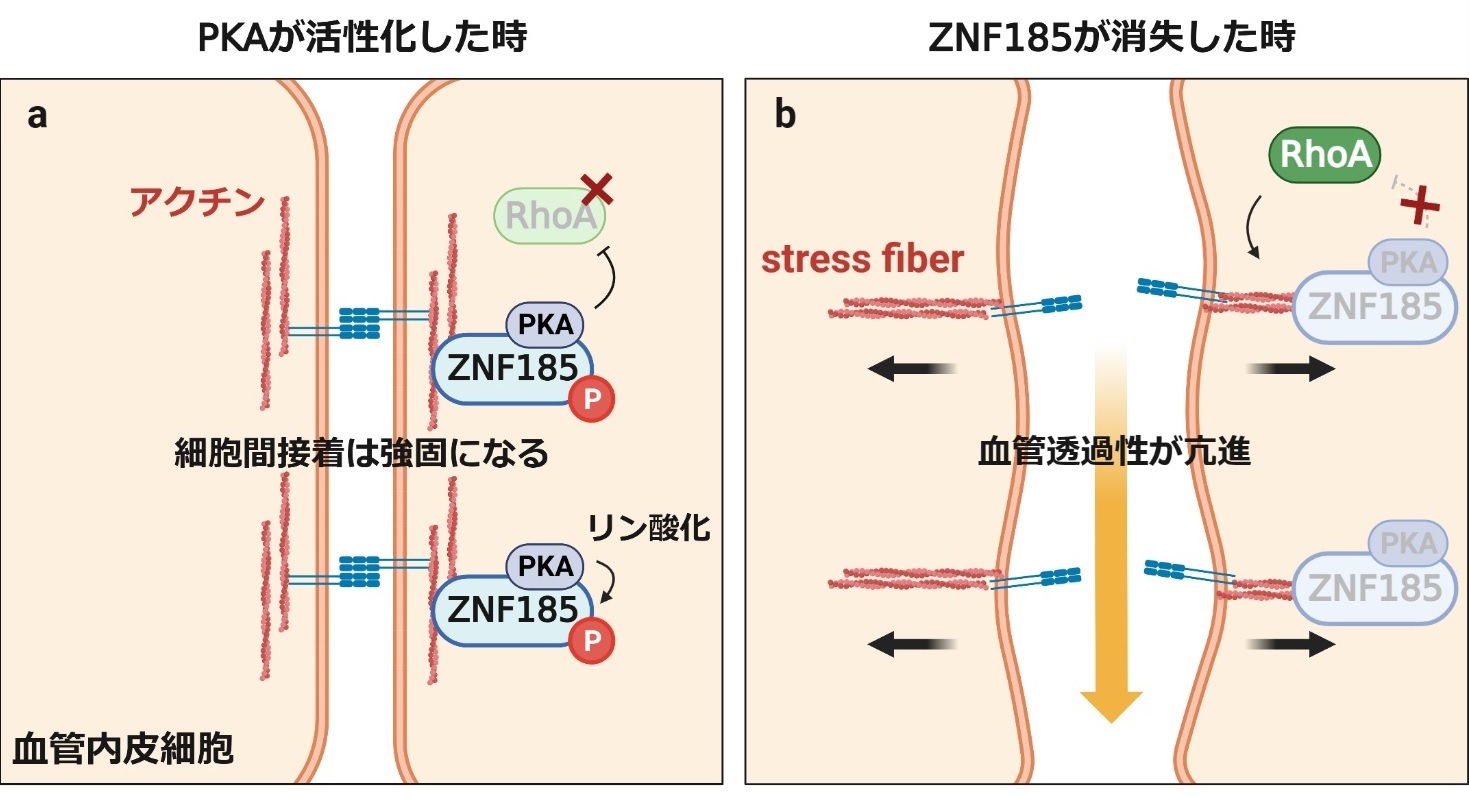
図1:ZNF185とPKAによるRhoA活性制御機構
a. ZNF185とPKAは細胞膜領域でアクチンと結合してRhoAの活性化を抑制し細胞接着を強くします(図中のPはリン酸化を表す)。
b. ZNF185が消失すると、PKAがRhoAを抑制できなくなります。活性化したRhoAはstress fiberを
形成して、細胞を収縮させることで血管透過性を亢進させます。

図2:マウスの血管透過性評価
マウスの尾静脈に色素(エバンスブルー)を投与した後に、血管透過性を亢進させるマスタードオイルを右耳に塗布しました。Zfp185をノックアウトしたマウスでは、野生型と比して色素の漏出が亢進しました。
研究成果の意義
用語解説
-
-
※1 RhoA・・・細胞骨格制御の中心的な役割を担うタンパクのひとつ。活性化したRhoAはアクチンに作用し、stress fiberと呼ばれる収縮性の線維を形成する。
-
※2 stress fiber・・・アクチンとミオシンからなる線維束であり細胞に張力を与える。
-
※3 ZNF185・・・Zinc finger protein (ZNF) と呼ばれるタンパク質間の相互作用を仲介する分子のひとつ。腫瘍細胞では、細胞の分化・増殖に関与することが知られている。
-
※4 相同体・・・類似した塩基配列の遺伝子で、共通の祖先に由来するもの。
論文情報
掲載誌:Communications Biology
論文タイトル: ZNF185 prevents stress fiber formation through the inhibition of RhoA in endothelial cells
DOI:https://doi.org/10.1038/s42003-023-04416-x
研究者プロフィール

安藤 史顕 (アンドウ フミアキ) Fumiaki Ando
東京医科歯科大学 大学院医歯学総合研究科
腎臓内科学分野 助教
・研究領域
腎臓 水・電解質輸送学

東京医科歯科大学 大学院医歯学総合研究科
腎臓内科学分野 大学院生
・研究領域
腎臓 細胞骨格制御

東京医科歯科大学 大学院医歯学総合研究科
腎臓内科学分野 教授
・研究領域
腎臓 水・電解質輸送
問い合わせ先
<研究に関すること>
東京医科歯科大学 大学院医歯学総合研究科
腎臓内科学分野 安藤 史顕 (アンドウ フミアキ)
E-mail:fandkidc[@]tmd.ac.jp
<報道に関すること>
東京医科歯科大学 総務部総務秘書課広報係
〒113-8510 東京都文京区湯島1-5-45
E-mail:kouhou.adm[@]tmd.ac.jp
※E-mailは上記アドレス[@]の部分を@に変えてください。

