細胞内のコレステロールが炎症や動脈硬化を促進
公開日:2022.11.23
日本医科大学
国立大学法人東京医科歯科大学
国立大学法人千葉大学
日本医科大学
国立大学法人東京医科歯科大学
国立大学法人千葉大学
細胞内のコレステロールが炎症や動脈硬化を促進
~細胞内のコレステロール蓄積の抑制が抗炎症治療となる可能性~
~細胞内のコレステロール蓄積の抑制が抗炎症治療となる可能性~
ポイント
- 動脈硬化の発症にマクロファージが重要です。
- 本研究では、マクロファージが活性化すると細胞内にコレステロールが蓄積すること、薬剤を用いてコレステロールの蓄積を抑制するとマクロファージの炎症応答を抑制できることを明らかにしました。さらに、ヒト動脈硬化症において、単球/マクロファージ中のコレステロール量の増加は動脈硬化の重症度と相関することを明らかにしました。
- この成果は、マクロファージ中のコレステロールを標的とした、新たな抗炎症治療・ならびに動脈硬化予防法の開発へと道を拓く可能性があります。
この研究は、日本医療研究開発機構(AMED) の革新的先端研究開発支援事業(PRIME)「生体組織の適応・修復機構の時空間的解析による生命現象の理解と医療技術シーズの創出」研究開発領域における研究開発課題「細胞代謝が規定するマクロファージの多様性に基づく筋修復メカニズムの解明」(研究開発代表者:大石由美子)、文部科学省科学研究費補助金等の支援のもと行われたもので、その研究成果は2022年11月22日、国際科学誌であるJCI Insight誌で公開されました。
研究の背景
動脈硬化は、低レベルの炎症が持続する「慢性炎症」を基盤に生じ、心筋梗塞や脳卒中の原因となります。高齢化社会を迎えた我が国においても、動脈硬化性心血管疾患は年々増加しています。これまで、血清コレステロール値のコントロールは動脈硬化の予防に重要であることがわかっていました。しかし、コレステロール値を完全に正常化しても予防出来ない例が数多く存在することから、新たな治療・予防法の開発が求められています。また、動脈硬化は無症状のうちに進行してしまうことが多く、血液検査で動脈硬化の進展を予測できる指標はありませんでした。
研究成果の概要
今回、大石教授らの研究グループは、慢性炎症に重要なマクロファージという免疫細胞が刺激を受けると、細胞内にコレステロールが蓄積されることを見つけました。また、溜まったコレステロール排出を促進するPRX(ポリロタキサン)という薬剤をマウスに投与すると、動脈硬化が起こりにくくなることを明らかにしました。また、ヒトにおいても血液中に存在する単球中のコレステロール量が、動脈硬化の重症度と関連することが明らかとなりました。
研究グループが着目したのは、マクロファージという免疫細胞の中に存在するコレステロールです。研究グループは、炎症を引き起こす刺激を受けるとマクロファージの細胞の中にあるリソソームという細胞内小器官にコレステロールが溜まることを見いだしました。さらに細胞内コレステロールの増加が、炎症を起こす刺激を細胞内に伝えることに必須であることが分かりました。マクロファージの細胞表面にあるToll型受容体TLR4は、Myd88(*用語解説1)というアダプタータンパク質を介して炎症の刺激を細胞内に伝えます。研究グループはコレステロールがMyd88にあるCRAC (CLR recognition/interaction amino acid consensus)配列に結合して炎症のシグナルを増幅することを見いだしました。
PRX(*用語解説2)という薬剤はリソソーム内のコレステロールの排出を促します。PRXを用いてリソソームへのコレステロールの蓄積を抑制すると、マクロファージの炎症応答を効果的に抑制することを見いだしました。動脈硬化になりやすいマウスにPRXを投与すると、動脈硬化部位におけるマクロファージによる炎症が抑制されて動脈硬化を抑制することができました。このことから、マクロファージの細胞内コレステロール蓄積を抑制すると、炎症や動脈硬化が抑制できる可能性が示唆されます。
さらに、ヒトでは、頚動脈の壁の厚さを超音波で測定することによって動脈硬化の重症度を評価することができます。研究グループは、血液中に存在し、マクロファージに分化できる単球に着目しました。動脈硬化のある症例において、単球に含まれるコレステロールと頚動脈の壁の厚さを測定しました。その結果、動脈硬化が重症であるほど白血球中のコレステロール量が高い傾向を認めました。このことから、マクロファージの細胞内コレステロール量は動脈硬化の重症度を予測するよい指標となる可能性があります。
研究グループが着目したのは、マクロファージという免疫細胞の中に存在するコレステロールです。研究グループは、炎症を引き起こす刺激を受けるとマクロファージの細胞の中にあるリソソームという細胞内小器官にコレステロールが溜まることを見いだしました。さらに細胞内コレステロールの増加が、炎症を起こす刺激を細胞内に伝えることに必須であることが分かりました。マクロファージの細胞表面にあるToll型受容体TLR4は、Myd88(*用語解説1)というアダプタータンパク質を介して炎症の刺激を細胞内に伝えます。研究グループはコレステロールがMyd88にあるCRAC (CLR recognition/interaction amino acid consensus)配列に結合して炎症のシグナルを増幅することを見いだしました。
PRX(*用語解説2)という薬剤はリソソーム内のコレステロールの排出を促します。PRXを用いてリソソームへのコレステロールの蓄積を抑制すると、マクロファージの炎症応答を効果的に抑制することを見いだしました。動脈硬化になりやすいマウスにPRXを投与すると、動脈硬化部位におけるマクロファージによる炎症が抑制されて動脈硬化を抑制することができました。このことから、マクロファージの細胞内コレステロール蓄積を抑制すると、炎症や動脈硬化が抑制できる可能性が示唆されます。
さらに、ヒトでは、頚動脈の壁の厚さを超音波で測定することによって動脈硬化の重症度を評価することができます。研究グループは、血液中に存在し、マクロファージに分化できる単球に着目しました。動脈硬化のある症例において、単球に含まれるコレステロールと頚動脈の壁の厚さを測定しました。その結果、動脈硬化が重症であるほど白血球中のコレステロール量が高い傾向を認めました。このことから、マクロファージの細胞内コレステロール量は動脈硬化の重症度を予測するよい指標となる可能性があります。
研究の意義・今後の展開
本研究では、細胞内のコレステロール蓄積を調節することによって、マクロファージの炎症応答を制御できることが明らかになりました。また、血液検査として単球中のコレステロールを測定すると、動脈硬化の重症度を診断できる可能性も示されました。これらは動脈硬化をはじめとした慢性炎症の新たな治療・予防標的となる可能性が示唆され、今後の展開が期待されます。
【図1】
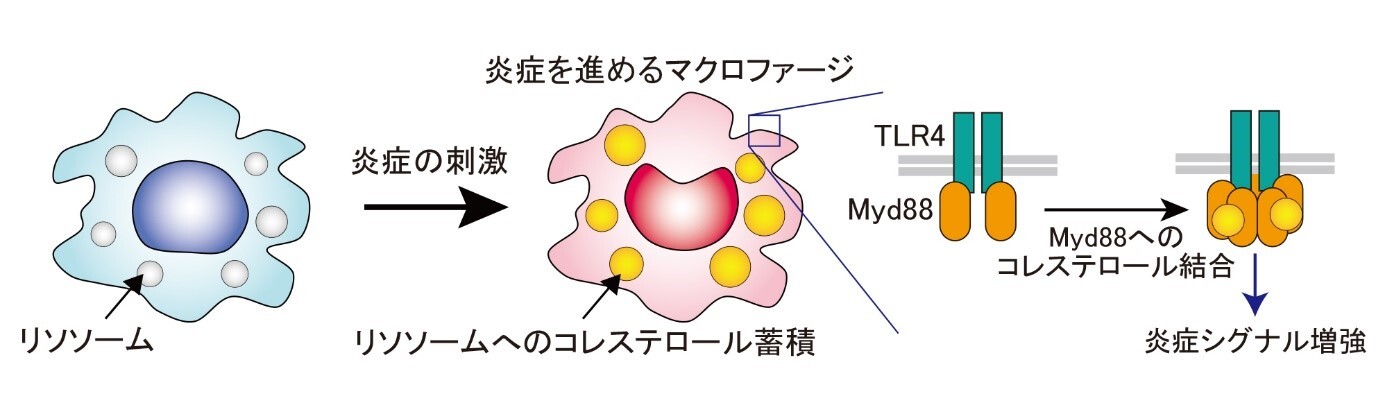
マクロファージは、炎症を引き起こす刺激を受けると、細胞の中にあるリソソームにコレステロールが溜まります。溜まったコレステロールは、細胞表面にあるToll型受容体TLR4の下にあるMyd88に結合して炎症のシグナルを増幅し、炎症の刺激を細胞内に伝えます。
【図2】
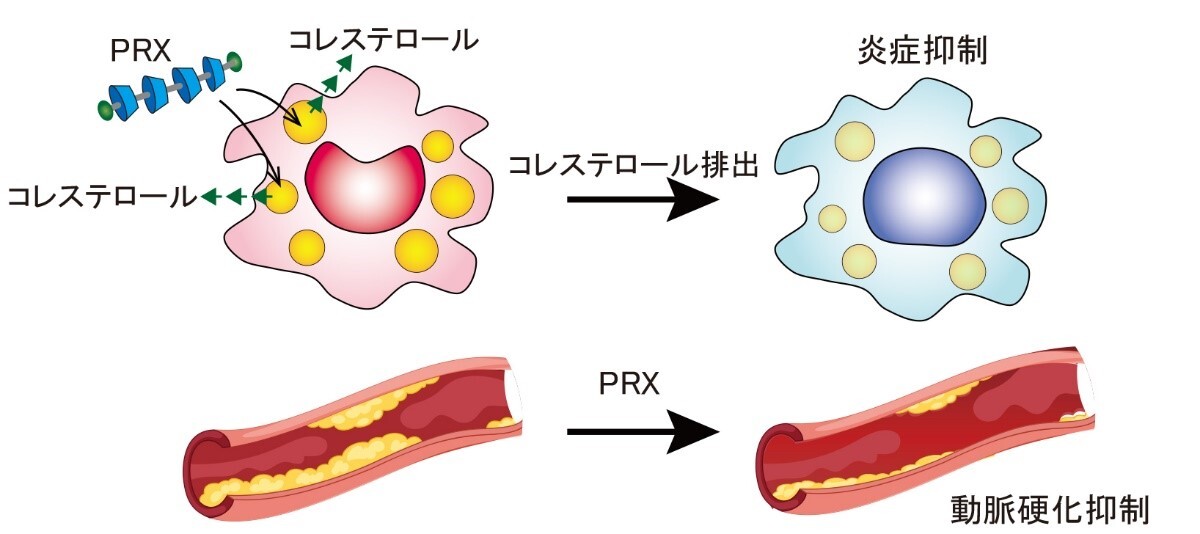
PRXという薬剤はリソソーム内のコレステロールの排出を促します。PRXを用いてリソソームへのコレステロールの蓄積を抑制すると、動脈硬化部位におけるマクロファージの炎症活性化を効果的に抑制し、動脈硬化を抑制することができました。
用語解説
1. Myd88:自然免疫応答において重要な役割を果たすアダプタータンパク質で、細胞質に存在する。インターロイキン1やToll様受容体(TLR)シグナルの伝達に不可欠で、コレステロールを直接結合するアミノ酸配列(CRAC配列)をもつ。
2.ポリロタキサン(PRX): 多数の環状分子の空洞部に線状高分子が貫通した超分子ポリマーの総称。コレステロールに作用するβ-シクロデキストリンを環状分子として利用し、リソソーム内でβ-シクロデキストリンを放出する設計を施すことで、リソソーム内に蓄積したコレステロールの排泄を促すことが明らかになっている。
2.ポリロタキサン(PRX): 多数の環状分子の空洞部に線状高分子が貫通した超分子ポリマーの総称。コレステロールに作用するβ-シクロデキストリンを環状分子として利用し、リソソーム内でβ-シクロデキストリンを放出する設計を施すことで、リソソーム内に蓄積したコレステロールの排泄を促すことが明らかになっている。
論文情報
-
雑誌名: JCI Insight
-
論文タイトル:Activated metabolism of cholesterol and its binding to Myd88 via its CRAC domain are integral to the macrophage innate response
-
著者:Sumio Hayakawa, Atsushi Tamura, Nikita Nikiforov, Hiroyuki Koike, Fujimi Kudo, Yinglan Cheng, Takuro Miyazaki, Marina Kubekina, Tatiana V. Kirichenko, Alexander N. Orekhov, Nobuhiko Yui, Ichiro Manabe and Yumiko Oishi
-
-
著者(日本語):早川清雄、田村篤志、小池博之、工藤藤美、成英瀾、宮崎拓郎、由井伸彦、眞鍋一郎、大石由美子
問い合わせ先
【研究に関するお問い合わせ】
日本医科大学
生化学・分子生物学(代謝・栄養学)教室
大学院教授 大石 由美子
E-mail:y-oishi[@]nms.ac.jp
【本プレスリリースに関するお問い合わせ】
日本医科大学 学事部庶務課
E-mail:nms-shomuka[@]nms.ac.jp
東京医科歯科大学 総務部総務秘書課広報係
〒113-8510 東京都文京区湯島1-5-45
E-mail:kouhou.adm[@]tmd.ac.jp
国立大学法人千葉大学 広報室
E-mail:koho-press[@]chiba-u.jp
※E-mailは上記アドレス[@]の部分を@に変えてください。

