「筋肉と骨の両方を強くし運動機能を向上させる創薬シーズを発見」【中島友紀 教授】
― “薬による運動ベネフィット”の実現で健康寿命の向上に期待 ―
ポイント
- これまで、運動が骨粗鬆症やサルコペニアなどの運動器疾患の治療や予防に効果的であることが知られていましたが、そのメカニズムはよくわかっていませんでした。
- 本研究グループは、運動による健康への恩恵、すなわち、運動ベネフィット※1を実現する創薬シーズを発見し、生体レベルで運動機能の向上およびそのメカニズムを明らかにしました。
- 本研究の成果から、運動を模倣した“薬による運動ベネフィット”が運動器疾患の治療や予防、さらには健康寿命の延伸へつながることが期待されます。
東京医科歯科大学大学院医歯学総合研究科分子情報伝達学分野の中島友紀教授、小野岳人助教らの研究グループは、運動ベネフィットを実現する創薬シーズを発見し、生体レベルで運動機能の向上および運動器疾患を改善するメカニズムをつきとめました。この研究は、科学技術振興機構(JST)の戦略的創造研究推進事業 さきがけ「生体における動的恒常性維持・変容機構の解明と制御(研究総括:春日雅人)」における研究課題「運動器の動的恒常性を司るロコモ・サーキットの解明」(研究代表者:中島友紀)、日本医療研究開発機構 (AMED) 革新的先端研究開発支援事業(AMED-CREST) 「メカノバイオロジー機構の解明による革新的医療技術の創出(研究開発総括: 曽我部正博)」研究開発領域における研究開発課題「骨恒常性を司る骨細胞のメカノ・カスケードの解明」(研究開発代表者:中島友紀)、文部科学省・科学研究費補助金、セコム科学技術振興財団、武田科学振興財団、第一三共TaNeDS等の支援のもとでおこなわれたもので、その研究成果は国際科学誌Bone Researchに、2022年8月3日にオンライン版で発表されました。
研究の背景
この現状からも見て取れるように、運動器疾患は、まさに“現代国民病”と言っても過言ではありません。そして、重要なことに、運動器疾患や運動不足では、認知症やうつ病など精神神経疾患、肥満や糖尿病など代謝性疾患を高頻度に合併します。一方、身体活動の強化や運動介入療法が、運動器疾患だけでなく様々な全身疾患の改善や予防、そして、抗老化に効果的である証拠が世界レベルで積み上げられています。しかしながら、運動器である骨と筋肉は、連動して運動を実現するにも関わらず、個別の医学領域として研究が発展してきたため、その臓器間の連環メカニズムの理解はいまだ未成熟です。そして、運動することで私たちの運動機能が向上したり、運動器疾患の改善や予防にどのようにつながるのか、いまだ不明な点が多いが現状です。
研究成果の概要
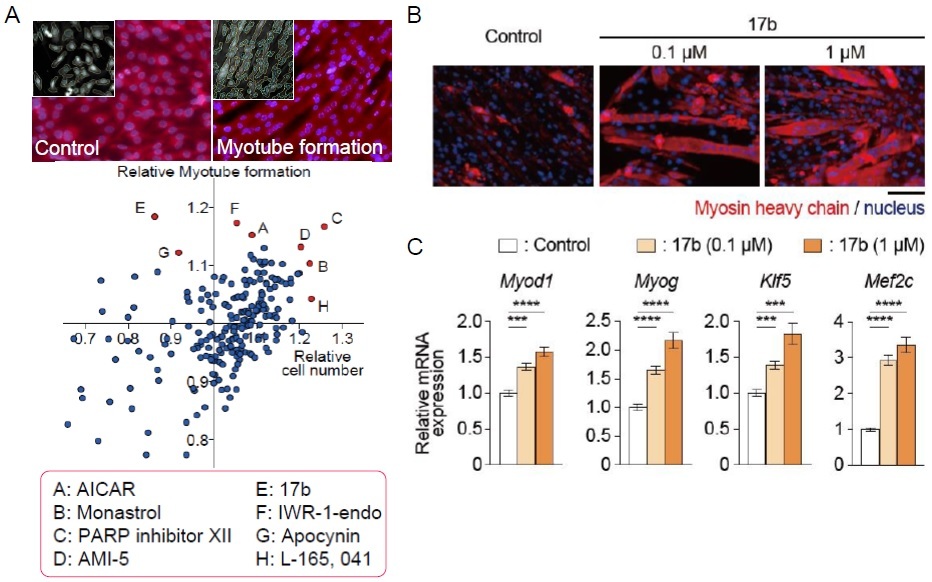
図1: 筋細胞の分化・増殖を基盤にした新規アッセイ系の構築
A: イメージングサイトメーターを用いた候補薬物による細胞の増殖と分化の定量解析
B: 候補薬物17bによる筋線維分化の促進
C: 候補薬物17bによる筋分化マーカー遺伝子の発現上昇
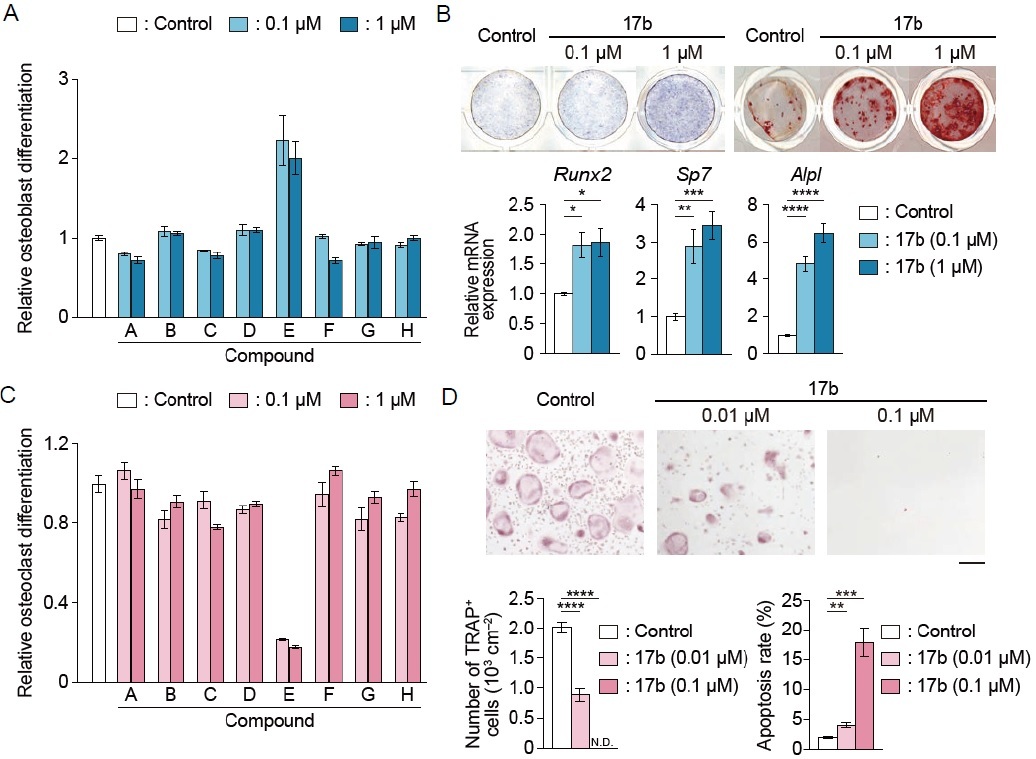
図2: 骨構成細胞の分化を基盤にした新規アッセイ系の構築
A: 候補薬物による骨芽細胞分化の定量解析
B: 候補薬物17bによる骨芽細胞分化、石灰化、分化マーカー遺伝子発現の上昇
C: 候補薬物による破骨細胞分化の定量化
D: 候補薬物17bによる破骨細胞形成の抑制
さらに、病態下でのLAMZの治療効果を検討するため、骨粗鬆症やサルコぺニアを模倣する尾部懸垂マウスモデルにこの薬物を投与しました。本モデルはマウス尾部を飼育ケージの上部に固定し、後肢のみ荷重を消失させることで微少重力環境に感化させる実験モデルです。微小重力に伴う著明な筋肉の萎縮と骨量の減少を誘導することができる本モデルは、寝たきりや宇宙空間など力学的負荷の減少状態で速やかに骨と筋肉が同時に弱くなる現象と類似しており、運動器疾患の人為的な制御法を確立する上で、生体レベルでの機能スクリーニングに有効であると考えられます。本モデルを用いて、LAMZによる治療効果を検討したところ、微少重力に伴う著明な筋肉の萎縮と骨量の減少を、有意に改善する結果が得られました (図4)。
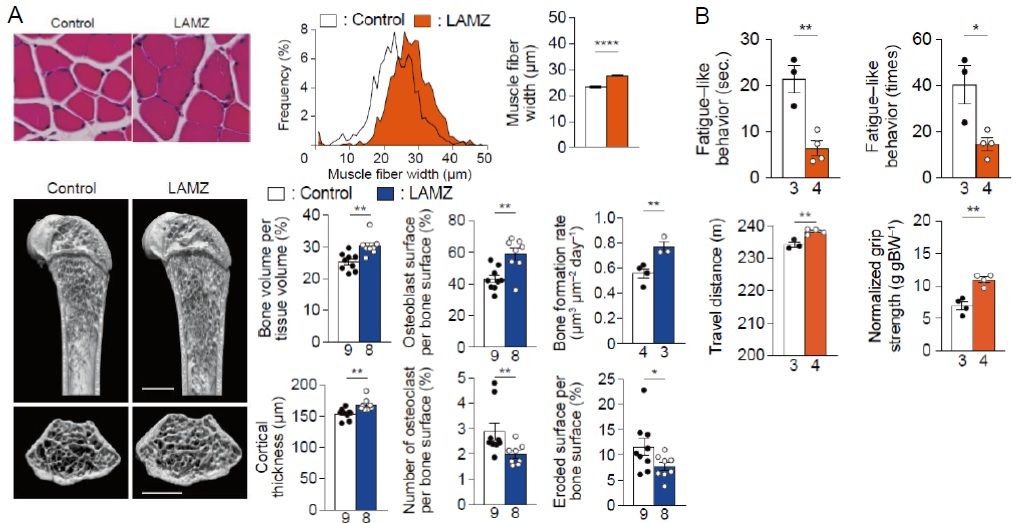
図3:LAMZによる生体レベルでの運動ベネフィットの効果
A: 筋および骨組織の変化(筋:HE画像、筋線維計測、骨:マイクロCT解析、骨形態計測)
B: 筋持久力と筋力の変化
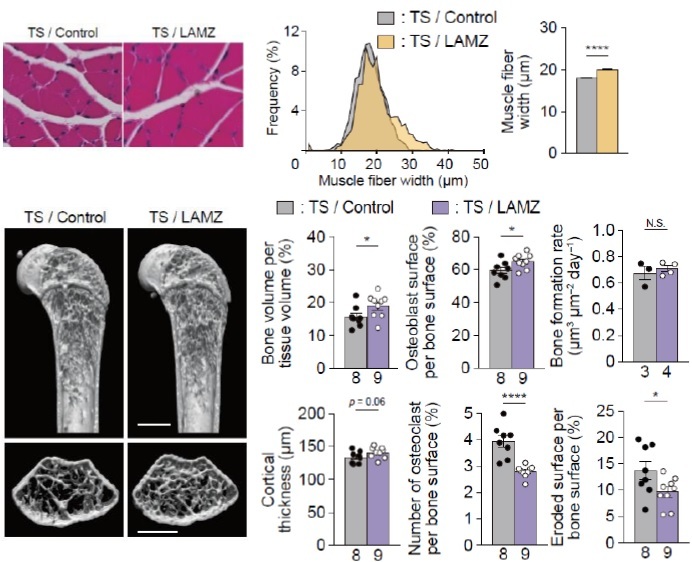
図4:LAMZによる運動器疾患の改善効果
筋および骨組織の変化(筋:HE画像、筋線維計測、骨:マイクロCT、骨形態計測)
これまでに運動による力学的な刺激によってカルシウムシグナルが誘導されPGC-1aの活性化に関与することが見出されています。そこで、LAMZによるカルシウムシグナルの誘導性を検討した結果、筋細胞と骨芽細胞においてLAMZが細胞内カルシウムシグナルを誘導することが明らかになりました。また、カルシウムシグナル経路を抑制する阻害剤(FK506, KN93)によってPGC-1a活性が抑制され、LAMZによる筋線維形成、および、骨形成、骨石灰化の抑制が見出されました。さらに、カルシウムシグナルで誘導されるMef2cの発現がLAMZによって有意に誘導され、カルシウムシグナルとPGC-1aの阻害により、その発現がキャンセルされることが明らかになりました。また、Mef2c遺伝子をノックダウンした筋芽細胞と骨芽細胞では、LAMZによる筋線維形成、および、骨形成、骨石灰化の誘導が抑制されることも見出されました。
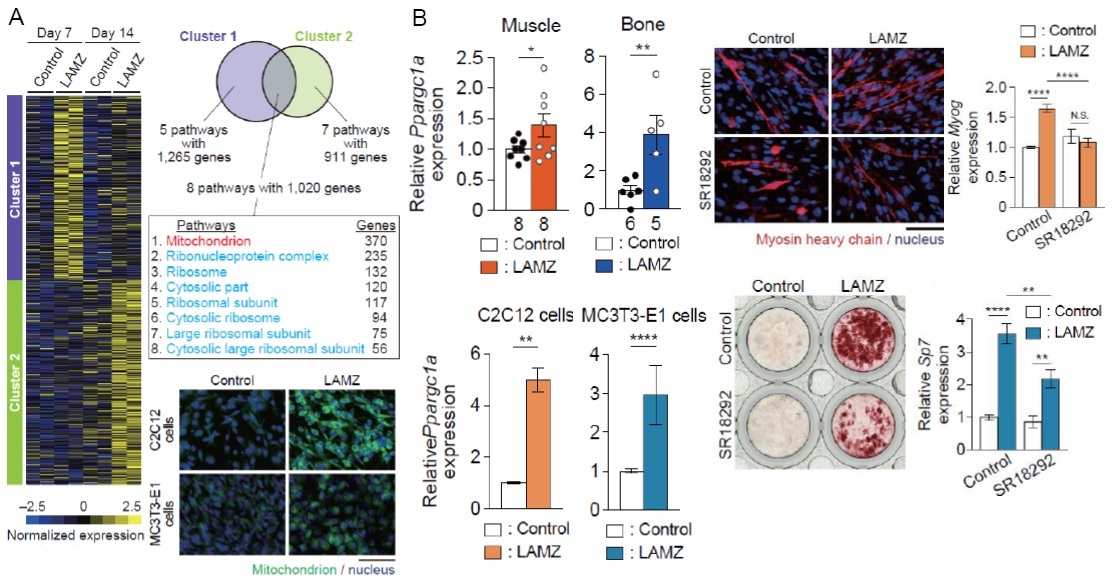
図5: LAMZの作用点の探索
A: 網羅解析による発現プロファイリング B: 標的分子PCG-1αの同定
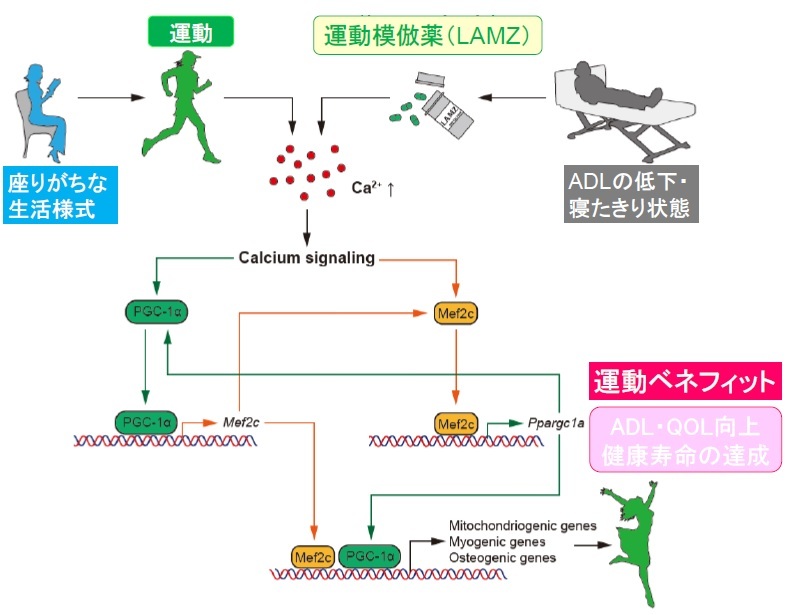
図6: 運動ベネフィットを実現するメカニズムと運動模倣薬
研究成果の意義
我々人類は何世紀にもわたって、『身体活動や運動が、健康な身体と健康な心を維持するための基本である』と信じてきました。重要なことに、運動が様々な恩恵をもたらすことは十分に認知されている一方で、運動器構成細胞では、運動によってどのようなシステムが駆動され、遠隔臓器に作用し、健康向上や抗老化を実現しているか?そして、その破綻による全身性疾患を、どのようなシステムが改善・予防できるのか?明確な科学的エビデンスの発見が、世界レベルで期待されています。さらに、現在、COVID-19パンデミックによる身体活動の制限が、感染や感染予後のリスクファクターであることが明らかになり、本領域研究の必然性が、益々浮き彫りとなっています。その研究成果は、日常生活動作(ADL)、生活の質(QOL)や健康寿命の促進、ひいては増え続ける医療費の負担軽減のゲームチェンジャーになると考えられます。
本研究は、運動ベネフィットを実現するメカニズムを明らかにし、運動を模倣することで骨粗鬆症やサルコペニアを改善する創薬シーズ“薬による運動”への開発に道をつけたと言えます(図6)。また、この成果は、様々な疾病により身体活動が制限される個人(例えば、脳血管障害や心疾患障害の合併患者)に対して運動効果を模倣したり、運動に対する無反応や有害反応者の治療介入を補完するために利用できる新たな“運動模倣療法”の創成にも繋がるだけでなく、運動によって改善や予防できる精神神経疾患や代謝性疾患など様々な全身性疾患への応用の可能性も期待されます。
用語解説
※1運動ベネフィット
身体活動の強化や運動、心肺フィットネスは、心血管疾患、肥満、糖尿病、認知症、骨粗鬆症、サルコペニアなどの全身性疾患の予防と改善に効果的であり、健康寿命の向上につながる。一方、運動不足は死亡率の増加と顕著な経済的負担に関連している。
※2骨粗鬆症
骨の量が減ったり、質が低下したりして弱くなり、骨折しやすくなる運動器疾患。特に脊椎の圧迫骨折や大腿部頸部骨折はADLやQOLを低下させ、ひいては健康寿命の低下につながる高齢化社会における大きな問題である。現在、我国では約12000万人の罹患者があり、その数は増加する一方である。古い骨を取り除く破骨細胞と骨を新しくする骨芽細胞のバランスの破綻が骨粗鬆症の病因と考えられている。
※3サルコペニア
加齢に伴い筋肉量と減少と筋力の低下を引き起こす運動器疾患。サルコペニアは姿勢を保つ、歩行する、立ち上がるなど、ADLを障害し転倒しやすくなったり、骨折しやすくなったりして、介護が必要となることから、健康寿命に直結する病気であることが知られている。
※4 PGC-1(遺伝子名:Ppargc1a)
転写子アクチベーターであり、ミトコンドリア生合成、エネルギー産生や熱消費に関る多くの遺伝子発現を制御している。また、PGC-1は、イリシンの誘導による脳由来神経栄養因子BDNFの発現上昇やキヌレニンアミノトランスフェラーゼを誘導することで神経保護キヌレン酸への有益シフトを誘発するなど、認知症やうつ病などの精神神経疾患の改善にも重要な役割を担っている。
論文情報
掲載誌:Bone Research
論文タイトル:Simultaneous augmentation of muscle and bone by locomomimetism through calcium-PGC-1α signaling
DOI:https://doi.org/10.1038/s41413-022-00225-w
研究者プロフィール

東京医科歯科大学大学院医歯学総合研究科
分子情報伝達学分野 教授
・研究領域
骨生物学、運動器科学、分子生物学

東京医科歯科大学大学院医歯学総合研究科
分子情報伝達学分野 助教
・研究領域
運動器科学、分子生物学
問い合わせ先
<研究に関すること>
東京医科歯科大学大学院医歯学総合研究科
分子情報伝達学分野 氏名 中島 友紀(ナカシマ トモキ)
E-mail:naka.csi[@]tmd.ac.jp
<報道に関すること>
東京医科歯科大学 総務部総務秘書課広報係
〒113-8510 東京都文京区湯島1-5-45
E-mail:kouhou.adm[@]tmd.ac.jp
※E-mailは上記アドレス[@]の部分を@に変えてください。

