「皮膚の若さの維持と老化のメカニズムを解明」【西村栄美 教授】

西村 栄美(ニシムラ エミ)教授 難治疾患研究所 幹細胞医学分野(中央)
松村 寛行(マツムラ ヒロユキ)助教 同上(左)
劉 楠(リュウ ナン)大学院生 同上(右)
ポイント
| ● | 表皮幹細胞が隣接する幹細胞との間で細胞競合を行うことによって皮膚の質(若さ)と恒常性を維持していることを発見しました。 |
| ● | 加齢によって表皮幹細胞のXVII型コラーゲン(COL17A1)を介した細胞競合が減弱すると皮膚の老化が起きることを明らかにしました。 |
| ● | 幹細胞競合の制御による抗老化、再生、加齢関連疾患の予防や治療への道が開かれました。 |
東京医科歯科大学難治疾患研究所幹細胞医学分野の西村栄美教授、松村寛行助教、劉楠氏らの研究グループは、同大学院皮膚科学分野の並木剛准教授らとの共同研究で、皮膚の老化の仕組みが、幹細胞競合による恒常性維持機構の疲弊によることをつきとめました。この研究はAMED『老化メカニズムの解明・制御プロジェクト』、ならびに文部科学省科学研究費補助金の支援のもとで行われたもので、その研究成果は、国際科学誌Nature(ネイチャー)に、2019年4月3日午後6時(英国時間)、4月4日午前2時(日本時間)にオンライン版で発表されました。
研究の背景
老化のメカニズムについては古くより諸説あるものの、臓器において絶えず生じる損傷やストレスを受けた細胞が生体内でどのような運命を辿っているのか、その運命と動態については未だ殆ど明らかにされておらず、臓器が長期にわたって若さと機能を保つ仕組み、ならびに老化する仕組みについては未解明でした。研究グループは、これまでに加齢によって色素幹細胞の疲弊や枯渇が起こると白髪を発症すること(Nishimura EK et al. Science, 2004)や、加齢による毛包幹細胞の枯渇により毛包がミニチュア化し消失していくことによって加齢性の脱毛が引き起こされること (Matsumura H et al. Science, 2016)を明らかにするなどのステムセルエイジング(幹細胞老化)の先駆的な研究に基づいて、器官再生の要である組織幹細胞が老化においても鍵を握ることを示しています。一方、人体において最大の臓器である皮膚は、個体と外界との境界に位置しながら生涯にわたり生命を維持しており、極めて頑健な抗老化機構によって幹細胞の疲弊を防いでいることが想定されますが、その実体と仕組みは不明でした。
一方、『細胞競合』と呼ばれる現象が、近年、ショウジョウバエの発生や腫瘍形成の過程において観察され、哺乳類においてもMDCK上皮細胞やマウスの初期胚において観察されており、遺伝子変異を獲得した細胞を排除する機構として注目を集めています。しかし、これまで生涯にわたる組織・臓器の恒常性維持ならびに老化における『細胞競合』の生理的な関与や役割については明らかにされていませんでした。
一方、『細胞競合』と呼ばれる現象が、近年、ショウジョウバエの発生や腫瘍形成の過程において観察され、哺乳類においてもMDCK上皮細胞やマウスの初期胚において観察されており、遺伝子変異を獲得した細胞を排除する機構として注目を集めています。しかし、これまで生涯にわたる組織・臓器の恒常性維持ならびに老化における『細胞競合』の生理的な関与や役割については明らかにされていませんでした。
研究成果の概要
組織・臓器の老化においては、日々発生する内因性ならびに外因性の損傷やストレスがその誘因となることが知られています。しかし、通常は紫外線を少々多めに浴びたところで直ちに皮膚に老化細胞が蓄積して高齢者のような皮膚になるわけではなく、皮膚は何十年という長期にわたってその若さと機能を維持し続けます。こうした組織や臓器の恒常性を維持する機構として幹細胞システムが知られています。皮膚表面の表皮をはじめ上皮組織は活発な新陳代謝を行っており、多くの幹細胞クローンが消滅する一方で一部の残存クローンが増大する現象が共通して観察されます。この幹細胞の消滅と残存は一見ランダムに見えることから“中立的幹細胞競合”と呼ばれています。しかし、それが生涯にわたって本当に中立的におこる現象なのか、むしろ選択的に適応度の高い細胞を選択する細胞競合を反映しているのかについては明らかにされていませんでした。
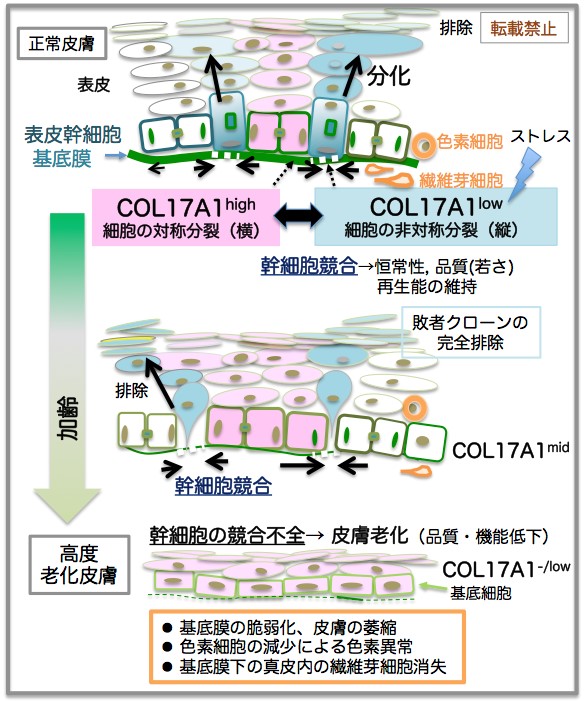
本研究では、実際に生体内の幹細胞の動態と運命を解析することにより、表皮幹細胞においてストレス応答性の幹細胞競合が起こっていること、特に幹細胞と基底膜を繋ぐヘミデスモソーム構成成分であるXVII型コラーゲン(COL17A1)の発現がゲノムストレス/酸化ストレス誘導性のタンパク質分解によって生理学的に変動し、その結果、個々の幹細胞におけるCOL17A1の発現量に有意な差異を生じていること、その差異が幹細胞分裂の様式に差を生じることで、幹細胞間における細胞競合を引き起こすことを明らかにしました。
マウス成体内でのin vivo多色幹細胞クローン分析とin vitroの3次元細胞培養モデルなどを駆使することにより、COL17A1高発現細胞が水平方向に対称性分裂して基底膜上で増幅する(勝者幹細胞クローンとなる)のに対して、加齢によりCOL17A1を失った細胞(低発現細胞)は非対称分裂(縦分裂)を連続して行いながらヘミデスモソーム構成分子やヘミデスモソーム構造を失って基底層との係留が減弱していく過程が観察されました。その結果、限られた空間内で両者が互いに競合しあうこととなり、後者は次第に基底層(ニッチ)から排除され分化を経て皮膚表面から排除されることが明らかになりました。これらの敗者クローンは、酸化ストレスやゲノムストレスに続くDNA損傷応答を経てCOL17A1の発現減少、ヘミデスモソームの消失を引き起こし、基底膜からの微小剥離により皮膚から排除することも明らかになりました。したがって、COL17A1高発現細胞が表皮幹細胞として長期にわたって維持されており、COL17A1レベルのより低い低品質細胞を皮膚から排除し続けるなかで、自身も次第にCOL17A1の発現を失ってしまうため細胞競合が減弱して表皮の細胞競合が減弱して表皮の老化が顕著となることが明らかになりました。
さらに表皮の角化細胞以外に表皮内でメラニン色素を産生している色素細胞や表皮の基底膜下に分布する繊維芽細胞などに着目して解析したところ、表皮幹細胞の細胞競合が反復されるなかで、表皮基底層から排除されていく敗者クローン細胞集団に囲まれていた色素細胞も周囲の敗者細胞と一緒に排除されること、ならびに基底膜下の真皮内の線維芽細胞も表皮幹細胞におけるヘミデスモソームの構築変化と並行して消失していくことが観察されました。このような真皮浅層の繊維芽細胞の消失は真皮の細胞外マトリックスの構築にも変化を及ぼして深部に波及しうるため、臓器としての老化へと繋がっていくものと考えられました。
最後に、表皮幹細胞においてCOL17A1を恒常的に発現させた高週齢マウスを解析すると、皮膚の老化の抑制効果ならびに再生促進効果が得られました。さらにCOL17A1の発現を誘導する低分子化合物によって皮膚の再生促進効果が得られており、今後皮膚老化の新規治療的戦略や予防へと繋がることが期待されます(特許出願中)。他の臓器の上皮組織においても同様に幹細胞競合が臓器の恒常性と老化を制御している可能性や、その制御が健康長寿に繋がる可能性も考えられるため、今後の広がりやあらたな展開が期待されます。
本研究では、実際に生体内の幹細胞の動態と運命を解析することにより、表皮幹細胞においてストレス応答性の幹細胞競合が起こっていること、特に幹細胞と基底膜を繋ぐヘミデスモソーム構成成分であるXVII型コラーゲン(COL17A1)の発現がゲノムストレス/酸化ストレス誘導性のタンパク質分解によって生理学的に変動し、その結果、個々の幹細胞におけるCOL17A1の発現量に有意な差異を生じていること、その差異が幹細胞分裂の様式に差を生じることで、幹細胞間における細胞競合を引き起こすことを明らかにしました。
マウス成体内でのin vivo多色幹細胞クローン分析とin vitroの3次元細胞培養モデルなどを駆使することにより、COL17A1高発現細胞が水平方向に対称性分裂して基底膜上で増幅する(勝者幹細胞クローンとなる)のに対して、加齢によりCOL17A1を失った細胞(低発現細胞)は非対称分裂(縦分裂)を連続して行いながらヘミデスモソーム構成分子やヘミデスモソーム構造を失って基底層との係留が減弱していく過程が観察されました。その結果、限られた空間内で両者が互いに競合しあうこととなり、後者は次第に基底層(ニッチ)から排除され分化を経て皮膚表面から排除されることが明らかになりました。これらの敗者クローンは、酸化ストレスやゲノムストレスに続くDNA損傷応答を経てCOL17A1の発現減少、ヘミデスモソームの消失を引き起こし、基底膜からの微小剥離により皮膚から排除することも明らかになりました。したがって、COL17A1高発現細胞が表皮幹細胞として長期にわたって維持されており、COL17A1レベルのより低い低品質細胞を皮膚から排除し続けるなかで、自身も次第にCOL17A1の発現を失ってしまうため細胞競合が減弱して表皮の細胞競合が減弱して表皮の老化が顕著となることが明らかになりました。
さらに表皮の角化細胞以外に表皮内でメラニン色素を産生している色素細胞や表皮の基底膜下に分布する繊維芽細胞などに着目して解析したところ、表皮幹細胞の細胞競合が反復されるなかで、表皮基底層から排除されていく敗者クローン細胞集団に囲まれていた色素細胞も周囲の敗者細胞と一緒に排除されること、ならびに基底膜下の真皮内の線維芽細胞も表皮幹細胞におけるヘミデスモソームの構築変化と並行して消失していくことが観察されました。このような真皮浅層の繊維芽細胞の消失は真皮の細胞外マトリックスの構築にも変化を及ぼして深部に波及しうるため、臓器としての老化へと繋がっていくものと考えられました。
最後に、表皮幹細胞においてCOL17A1を恒常的に発現させた高週齢マウスを解析すると、皮膚の老化の抑制効果ならびに再生促進効果が得られました。さらにCOL17A1の発現を誘導する低分子化合物によって皮膚の再生促進効果が得られており、今後皮膚老化の新規治療的戦略や予防へと繋がることが期待されます(特許出願中)。他の臓器の上皮組織においても同様に幹細胞競合が臓器の恒常性と老化を制御している可能性や、その制御が健康長寿に繋がる可能性も考えられるため、今後の広がりやあらたな展開が期待されます。
研究成果の意義
| ● | 表皮幹細胞における細胞競合は、皮膚において日々発生している損傷やストレスを受けた幹細胞を選択的に排除しながら、COL17A1を発現する再生能力の高い表皮幹細胞を増幅することで、表皮角化細胞の品質(若さ)を保っていると考えられます。 |
| ● | 加齢により表皮での幹細胞競合が減弱し表皮や基底膜の維持が不十分になると、表皮内の色素細胞や真皮上層の繊維芽細胞の減少も引き起こすことから、上皮組織の老化は上皮内の細胞のみならず隣接する異なる系譜の細胞や間葉系組織にも影響し臓器の老化を促すと考えられます。 |
| ● | 今後、幹細胞競合の制御により上皮系臓器の老化制御や健康長寿へと繋がることが期待されます。 |
用語解説
表皮幹細胞
皮膚の最外層に位置する表皮は、その大部分が表皮角化細胞(ケラチノサイト)で構成されている。表皮角化細胞は基底層で分裂したのち、分化しながら皮膚表面に向かって移動し、角層を形成してバリア機能を担っている。表皮基底層に位置する細胞は未分化でその多くが自己複製するため表皮幹細胞と呼ばれていることが多いが、生体内でどの細胞集団が長期にわたり幹細胞として機能するのかについては正確には明らかにされていなかった。
ヘミデスモソーム (半接着斑)
上皮細胞が基底膜に接着する接着装置の一種で、多くの細胞膜裏打ちタンパク質が複合体を形成している。上皮細胞を膜貫通性に基底膜へと繋げて係留する。
XVII型コラーゲン(COL17A1)
ヘミデスモソームの構成分子の一つ。表皮においては基底細胞が発現する膜貫通性蛋白。その先天性の欠損により表皮真皮接合部が不安定化し、接合部型表皮水疱症を発症し、皮膚の萎縮、脆弱性、びらん、色素異常、脱毛などを引き起こす。
細胞競合
組織中で近接する同種細胞間で相対的に環境適応度の高い細胞が低い細胞を集団から排除する現象。
論文情報
掲載誌: Nature
論文タイトル: Stem cell competition orchestrates skin homeostasis and ageing
論文タイトル: Stem cell competition orchestrates skin homeostasis and ageing
研究者プロフィール
西村 栄美 (ニシムラ エミ) Emi K. Nishimura
東京医科歯科大学 難治疾患研究所
幹細胞医学分野 教授
研究領域
幹細胞生物学、老化生物学、皮膚科学、癌生物学など
松村 寛行 (マツムラ ヒロユキ) Hiroyuki Matsumura
東京医科歯科大学 難治疾患研究所
幹細胞医学分野 助教
研究領域
幹細胞生物学、老化生物学、癌生物学など
劉楠 (リュウ ナン) Nan Liu
東京医科歯科大学 難治疾患研究所
幹細胞医学分野 大学院生
研究領域
幹細胞生物学、老化生物学など
東京医科歯科大学 難治疾患研究所
幹細胞医学分野 教授
研究領域
幹細胞生物学、老化生物学、皮膚科学、癌生物学など
松村 寛行 (マツムラ ヒロユキ) Hiroyuki Matsumura
東京医科歯科大学 難治疾患研究所
幹細胞医学分野 助教
研究領域
幹細胞生物学、老化生物学、癌生物学など
劉楠 (リュウ ナン) Nan Liu
東京医科歯科大学 難治疾患研究所
幹細胞医学分野 大学院生
研究領域
幹細胞生物学、老化生物学など
問い合わせ先
研究に関すること
報道に関すること
東京医科歯科大学 総務部総務秘書課広報係
〒113-8510 東京都文京区湯島1-5-45
TEL:03-5803-5833 FAX:03-5803-0272
E-mail:kouhou.adm@tmd.ac.jp
〒113-8510 東京都文京区湯島1-5-45
TEL:03-5803-5833 FAX:03-5803-0272
E-mail:kouhou.adm@tmd.ac.jp

