臨床研究(倫理審査委員会・治験等審査委員会対象)
概要
倫理審査委員会・治験等審査委員会の審査対象となる臨床研究は、申請後速やかに、研究責任者が倫理審査申請システムの当該課題のメニューから利益相反状況を申告してください。利益相反が存在する場合には、分担研究者全員の利益相反自己申告が必要です。利益相反申告が倫理審査委員会・治験等審査委員会の審査予定月の利益相反申告スケジュールに間に合わなかった場合は、倫理審査委員会・治験等審査委員会の審査が次月以降に遅れることになりますので、ご注意ください。
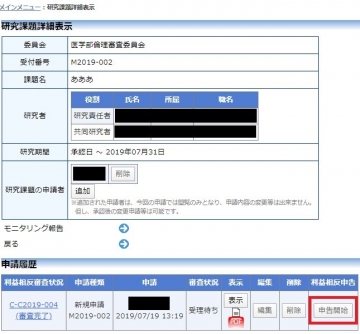
倫理審査委員会への申請課題については、
研究責任者が倫理システム上から申告してください
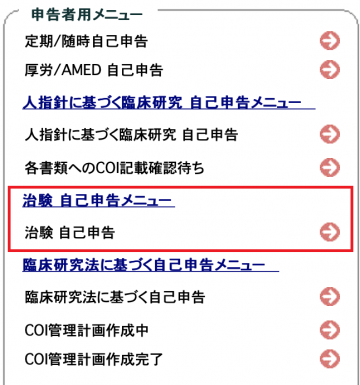
治験等審査委員会への申請課題については、
研究責任者が利益相反システムの上記メニューから申告してください
利益相反申告方法等マニュアル
申告方法
COI記載確認方法
- COI記載確認マニュアル
研究計画書・被験者用説明書での利益相反状況開示について
臨床研究の実施に際しては、研究を審査する審査委員や研究に参加する被験者に対して、各研究者の利益相反状況を開示する必要があります。研究計画書に利益相反の内容を記載するとともに、被験者用説明書には以下の文例案を参考に利益相反状況の記載を行ってください。

