選択的スプライシングの可視化
Nature Methods (2006), Nature Protocols (2010)
私たちが開発した、複数の蛍光タンパク質を用いて生体におけるmRNA前駆体の選択的スプライシングパターンを個々の細胞レベルで可視化する手法について紹介します.
私たちが開発した、複数の蛍光タンパク質を用いて生体におけるmRNA前駆体の選択的スプライシングパターンを個々の細胞レベルで可視化する手法について紹介します.
この研究成果は、Nature Methods(2006年3巻11号)の表紙に掲載されました.
選択的スプライシングレポーターの開発
私たちは、複数の蛍光タンパク質を用いて選択的スプライシングのパターンを可視化するレポーターミニ遺伝子作製法を開発し、培養細胞やマウス、線虫などの動物個体で生きたままスプライシングパターンを可視化することに成功しました.
これらのレポーターミニ遺伝子では、選択的スプライシングパターンに応じて複数の異なる蛍光タンパク質が発現するように工夫されています.単色のスプライシングレポーターが各細胞における転写量等の差異を考慮せず特定のmRNAアイソフォームの最終的な生成量をモニターするのに対し、複数の蛍光タンパク質を用いる方法では、一方の蛍光タンパク質の発現が対照として機能し、蛍光タンパク質間で発現量を比較することによって、個々の細胞や組織におけるスプライシングパターンをプロファイリングできる長所があります.
これらのレポーターミニ遺伝子では、選択的スプライシングパターンに応じて複数の異なる蛍光タンパク質が発現するように工夫されています.単色のスプライシングレポーターが各細胞における転写量等の差異を考慮せず特定のmRNAアイソフォームの最終的な生成量をモニターするのに対し、複数の蛍光タンパク質を用いる方法では、一方の蛍光タンパク質の発現が対照として機能し、蛍光タンパク質間で発現量を比較することによって、個々の細胞や組織におけるスプライシングパターンをプロファイリングできる長所があります.
レポーターミニ遺伝子の構造
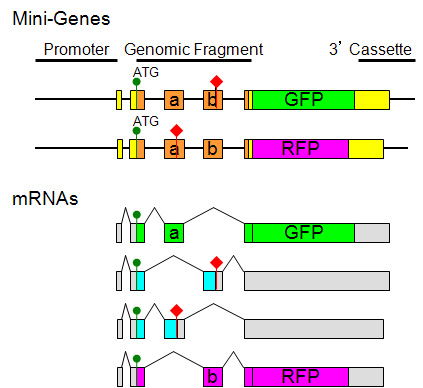
ミニ遺伝子の構造(Nature Protocols, 2010より)
図は、相互排他的な2つのエクソン(エクソンaとエクソンb)の使い分けを可視化するために私たちが用いている、典型的な2コンストラクト混合型レポーターミニ遺伝子の模式図です.
選択的エクソンの上流の構成的エクソンから下流の構成的エクソンまでの遺伝子断片(オレンジ色)の下流にGFPまたはRFPのcDNAを翻訳の読み枠を合わせて連結し、共通のプロモーターと3’カセットで挟んであります.さらに、上流の構成的エクソンに翻訳開始コドン(緑色の丸)、エクソンaまたはエクソンbのいずれかに終止コドン(赤色の菱形)を人為的に導入してあります.
各ミニ遺伝子から産生され得る2つのmRNAアイソフォームのうち、それぞれ一方のmRNAだけ、蛍光タンパク質との融合タンパク質(この図の例ではExon a - GFPとExon b - RFP)が発現します.したがって、この図の場合では、GFP融合タンパク質の発現はエクソンaの選択を、RFP融合タンパク質の発現はエクソンbの選択を示します.
これらのミニ遺伝子を同じプロモーター制御下で同時に発現させることで、各細胞でのスプライシングバリアントの比率を、GFP/RFPの比(視覚的には色)という形で可視化することができます.
他の型の選択的スプライシングについても、同様に、GFP/RFPの発現がそれぞれ特定のスプライシングパターンを反映するように工夫することで、レポーターミニ遺伝子を構築できます.私たちは、3つの蛍光タンパク質を利用して3種類のスプライスバリアントの発現をモニターすることにも成功しています.
選択的エクソンの上流の構成的エクソンから下流の構成的エクソンまでの遺伝子断片(オレンジ色)の下流にGFPまたはRFPのcDNAを翻訳の読み枠を合わせて連結し、共通のプロモーターと3’カセットで挟んであります.さらに、上流の構成的エクソンに翻訳開始コドン(緑色の丸)、エクソンaまたはエクソンbのいずれかに終止コドン(赤色の菱形)を人為的に導入してあります.
各ミニ遺伝子から産生され得る2つのmRNAアイソフォームのうち、それぞれ一方のmRNAだけ、蛍光タンパク質との融合タンパク質(この図の例ではExon a - GFPとExon b - RFP)が発現します.したがって、この図の場合では、GFP融合タンパク質の発現はエクソンaの選択を、RFP融合タンパク質の発現はエクソンbの選択を示します.
これらのミニ遺伝子を同じプロモーター制御下で同時に発現させることで、各細胞でのスプライシングバリアントの比率を、GFP/RFPの比(視覚的には色)という形で可視化することができます.
他の型の選択的スプライシングについても、同様に、GFP/RFPの発現がそれぞれ特定のスプライシングパターンを反映するように工夫することで、レポーターミニ遺伝子を構築できます.私たちは、3つの蛍光タンパク質を利用して3種類のスプライスバリアントの発現をモニターすることにも成功しています.
スプライシング制御機構への遺伝学的アプローチ
私たちは、透明で生きたまま観察が可能な線虫C. elegansをモデル生物として用い選択的スプライシングパターンを生体内で可視化しました.
線虫は、変異体の単離とマッピング、トランスジェニック線虫の作製、RNAiによるノックダウンなど各種の遺伝学的解析法が揃っており、多細胞生物として最初にゲノムが解読されるなど、広くさまざまな医学生理学の研究に利用されている優れたモデル生物です.
線虫の遺伝子は、哺乳類同様にほとんどの遺伝子にイントロンがあり、さまざまなパターンの選択的スプライシングが見られます.それにもかかわらず、イントロンの平均の長さが哺乳類よりもずっと短いため、ミニ遺伝子を利用した生体内での選択的スプライシング制御機構の解析に適した生物であるといえます.
さまざまな遺伝子の選択的スプライシングパターンの線虫生体内で可視化したことによって、スプライシングレポーター発現の表現型を指標にした遺伝学的解析が可能になりました.このホームページの他のページでは、これまでの研究成果を紹介しています.
線虫は、変異体の単離とマッピング、トランスジェニック線虫の作製、RNAiによるノックダウンなど各種の遺伝学的解析法が揃っており、多細胞生物として最初にゲノムが解読されるなど、広くさまざまな医学生理学の研究に利用されている優れたモデル生物です.
線虫の遺伝子は、哺乳類同様にほとんどの遺伝子にイントロンがあり、さまざまなパターンの選択的スプライシングが見られます.それにもかかわらず、イントロンの平均の長さが哺乳類よりもずっと短いため、ミニ遺伝子を利用した生体内での選択的スプライシング制御機構の解析に適した生物であるといえます.
さまざまな遺伝子の選択的スプライシングパターンの線虫生体内で可視化したことによって、スプライシングレポーター発現の表現型を指標にした遺伝学的解析が可能になりました.このホームページの他のページでは、これまでの研究成果を紹介しています.
生体内選択的スプライシング可視化技術を用いた研究成果の意義
私たちの開発した生体内選択的スプライシング可視化技術とそれをモデル生物線虫で応用した研究成果の意義は次のようにまとめられます.
1.選択的スプライシングレポーターの発現がモデルとして用いた内在性の遺伝子の選択的スプライシングパターンを反映しており、生体内における組織特異性や発生段階依存性などの選択性を1細胞の解像度でプロファイリングできます.
2.レポーターミニ遺伝子および内在性遺伝子の選択的スプライシングを制御する制御因子の同定、生体での選択性の制御に必要なシスエレメントの同定をしました.
3.スプライシング制御因子変異体を利用して、プロセシング中間体の同定によるイントロン除去の順序などmRNA前駆体の運命決定機構を解明しました.
4.選択的スプライシング制御因子やシスエレメントの配列が線虫から脊椎動物まで進化的に保存されていることを明らかにしました.
1.選択的スプライシングレポーターの発現がモデルとして用いた内在性の遺伝子の選択的スプライシングパターンを反映しており、生体内における組織特異性や発生段階依存性などの選択性を1細胞の解像度でプロファイリングできます.
2.レポーターミニ遺伝子および内在性遺伝子の選択的スプライシングを制御する制御因子の同定、生体での選択性の制御に必要なシスエレメントの同定をしました.
3.スプライシング制御因子変異体を利用して、プロセシング中間体の同定によるイントロン除去の順序などmRNA前駆体の運命決定機構を解明しました.
4.選択的スプライシング制御因子やシスエレメントの配列が線虫から脊椎動物まで進化的に保存されていることを明らかにしました.

