「エイズウイルスの感染成立に重要な宿主タンパク質を発見」【武内寛明 助教、山岡昇司 教授】

武内 寛明(タケウチ ヒロアキ)助教 大学院医歯学総合研究科ウイルス制御学分野(左)
山岡 昇司(ヤマオカ ショウジ)教授 同上(右)
ポイント
| ● | エイズウイルスは、CD4陽性Tリンパ球*1) やマクロファージに感染し、感染細胞内にタンパク質でできた殻(コア構造体)を放出します。 |
| ● | コア構造体内にはウイルス遺伝子であるRNAや逆転写酵素等が内包されており、ウイルスDNA合成の場を提供します。 |
| ● | ウイルスDNA合成ステップには、コア構造体が「適切なタイミング」で崩壊する必要があります。 |
| ● | 本研究では、長らく謎であったコア構造体崩壊の制御を、細胞内リン酸化酵素の一つとして知られているMaternal Embryonic Leucine Zipper Kinase (MELK)が、コア構造体の段階的リン酸化を通して担っていることをつきとめました。 |
| ● | 本研究成果から、変異しやすいウイルス由来酵素タンパク質ではなく宿主側感染制御因子を標的とした新規エイズ治療法開発への応用が期待できます。 |
東京医科歯科大学大学院医歯学総合研究科ウイルス制御学分野の武内寛明(たけうち ひろあき)助教と山岡昇司(やまおか しょうじ)教授らの研究グループは、京都大学、国立感染症研究所、塩野義製薬株式会社との共同研究で、エイズウイルス感染細胞内のウイルスコア構造体崩壊の原因が、細胞内リン酸化酵素MELKのコア構造体リン酸化によることをつきとめました。この研究は文部科学省科学研究費補助金、厚生労働科学研究費補助金、日本医療研究開発機構(AMED)、東京医科歯科大学・産学連携共同研究(塩野義製薬株式会社)、公益信託今井保太郎記念エイズ研究助成金および武田科学振興財団の支援のもとでおこなわれたもので、その研究成果は、国際科学誌PLOS Pathogens(プロス パソジェンズ)に、2017年7月6日午後2時(米国東部時間)にオンライン版で発表されました。
研究の背景
エイズの原因ウイルスであるヒト免疫不全ウイルス(HIV-1)は遺伝子としてRNAを持ち、感染標的細胞内で逆転写という過程によってRNAを鋳型としてDNAを合成して、感染した細胞の遺伝子にウイルスDNAを組み込みます。HIV-1がCD4陽性Tリンパ球やマクロファージ等の感染標的細胞に侵入する際に、ウイルス粒子に内包されているコア構造体を細胞内に放出します(脱殻)。コア構造体にはウイルスRNAや逆転写酵素等のウイルスDNA合成に必要な材料が入っており、HIV感染が成立するためには、ウイルスDNA合成ステップとコア構造体崩壊との「時空間的」な協調が必要不可欠であることが以前から分かっていました。ところが、コア構造体崩壊のタイミングを制御する具体的なメカニズムについては長らく謎のままでした。
研究成果の概要
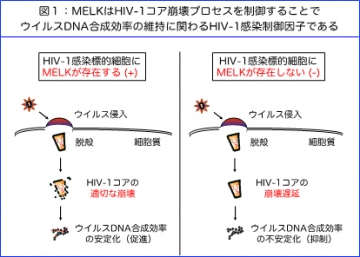
研究グループは、HIV-1感染標的細胞のひとつであるCD4陽性Tリンパ球を用いたゲノムワイドRNA干渉(RNA interference: RNAi)スクリーニング*2) を行い、HIV-1感染を制御する宿主細胞内因子としてリン酸化酵素MELKを見出しました。そしてMELKのHIV-1感染制御能を解析したところ、MELKの発現を抑制したCD4陽性Tリンパ球にHIV-1が感染するとウイルスコア構造体の崩壊タイミングが遅れてしまい、ウイルスDNA合成ステップが阻害されてしまうことがわかりました [図1:MELKが存在しない (-)] 。
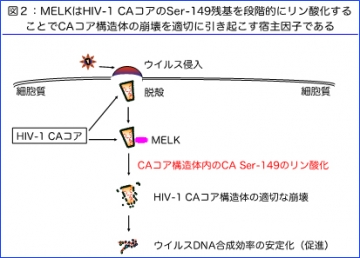
またMELKはコア構造体を形成するHIV-1キャプシドタンパク質(HIV-1 CA)の特定アミノ酸残基(149番目のセリン残基:CA Ser-149)を段階的にリン酸化することによりHIV-1コア構造体崩壊制御を行っていることを明らかにしました(図2)。
研究成果の意義
本研究成果によって、長らく謎であったHIV-1コア構造体崩壊制御メカニズムが明らかになり、HIV-1感染に必要不可欠な宿主側要因がつきとめられました。それに加えて、発見した宿主タンパク質がリン酸化酵素であったことから、変異しやすいウイルス由来酵素タンパク質ではなく宿主側感染制御因子を標的とした新規エイズ治療法開発への応用が期待できます。
用語解説
*1) CD4陽性Tリンパ球
免疫システムの司令塔の役割を担う細胞であり、HIVはこの細胞に侵入し増殖する。HIV感染により血中のCD4陽性Tリンパ球数は大幅に低下し、それに伴って免疫力低下につながる。
*2)ゲノムワイドRNA干渉スクリーニング
RNA干渉(RNA interference: RNAi)は、21-23塩基対から成る二本鎖RNAと相補的な塩基配列を持つメッセンジャーRNA(mRNA)が分解される現象である。ゲノムワイドRNA干渉スクリーニングは、RNA干渉を利用して特異的な細胞間/分子間相互作用を網羅的に解析する方法として用いられている。
免疫システムの司令塔の役割を担う細胞であり、HIVはこの細胞に侵入し増殖する。HIV感染により血中のCD4陽性Tリンパ球数は大幅に低下し、それに伴って免疫力低下につながる。
*2)ゲノムワイドRNA干渉スクリーニング
RNA干渉(RNA interference: RNAi)は、21-23塩基対から成る二本鎖RNAと相補的な塩基配列を持つメッセンジャーRNA(mRNA)が分解される現象である。ゲノムワイドRNA干渉スクリーニングは、RNA干渉を利用して特異的な細胞間/分子間相互作用を網羅的に解析する方法として用いられている。
論文情報(英文で記載)
掲載誌: PLOS Pathogens
論文タイトル: Phosphorylation of the HIV-1 capsid by MELK triggers uncoating to promote viral cDNA synthesis
http://journals.plos.org/plospathogens/article?id=10.1371/journal.ppat.1006441
論文タイトル: Phosphorylation of the HIV-1 capsid by MELK triggers uncoating to promote viral cDNA synthesis
http://journals.plos.org/plospathogens/article?id=10.1371/journal.ppat.1006441
問い合わせ先
研究に関すること
東京医科歯科大学大学院医歯学総合研究科
ウイルス制御学分野 武内 寛明(たけうち ひろあき)
TEL:03-5803-5178
E-mail: htake.molv@tmd.ac.jp
東京医科歯科大学大学院医歯学総合研究科
ウイルス制御学分野 山岡 昇司(やまおか しょうじ)
TEL:03-5803-5181
E-mail: shojmmb@tmd.ac.jp
ウイルス制御学分野 武内 寛明(たけうち ひろあき)
TEL:03-5803-5178
E-mail: htake.molv@tmd.ac.jp
東京医科歯科大学大学院医歯学総合研究科
ウイルス制御学分野 山岡 昇司(やまおか しょうじ)
TEL:03-5803-5181
E-mail: shojmmb@tmd.ac.jp
AMED事業に関すること
国立研究開発法人日本医療研究開発機構 戦略推進部 感染症研究課
〒100-0004 東京都千代田区大手町1-7-1
TEL:03-6870-2225 FAX:03-6870-2243
E-mail:kansen@amed.go.jp
〒100-0004 東京都千代田区大手町1-7-1
TEL:03-6870-2225 FAX:03-6870-2243
E-mail:kansen@amed.go.jp
報道に関すること
東京医科歯科大学 総務部総務秘書課広報係
〒113-8510 東京都文京区湯島1-5-45
TEL:03-5803-5833 FAX:03-5803-0272
E-mail:kouhou.adm@tmd.ac.jp
〒113-8510 東京都文京区湯島1-5-45
TEL:03-5803-5833 FAX:03-5803-0272
E-mail:kouhou.adm@tmd.ac.jp

