「高効率を実現した遺伝子改変技術の開発」【田中光一 教授】

田中 光一 教授 難治疾患研究所 分子神経科学分野(右)
相田 知海 助教 難治疾患研究所 分子神経科学分野(左)
― 生体の遺伝子をより自在に操る新たな手法 ―
ポイント
| ● | 極めて簡便な遺伝子改変技術を開発しました。 |
| ● | 従来困難であった、数千塩基の長さの人工遺伝子を正確に挿入したマウスの作製に、50%もの高い効率で成功しました。 |
| ● | 基礎医学・生物学研究から、創薬・遺伝子治療・品種改良による食料生産の効率化・バイオエタノールの効率的な生産等のエネルギー資源に至るまで広い分野での研究開発を加速すると期待されます。 |
東京医科歯科大学難治疾患研究所分子神経科学分野の田中光一教授と相田知海助教の研究グループは、広島大学、慶應義塾大学、株式会社ファスマックとの共同研究で、遺伝子改変生物を極めて簡便に、かつ高効率で作製する技術を開発しました。この研究は文部科学省脳科学研究戦略推進プログラムの一貫として実施され、また文部科学省科学研究費補助金、東京医科歯科大学学長裁量優秀若手研究者奨励賞、東京医科歯科大学難疾患研究所・難治疾患に対する研究助成、同・難治疾患共同研究拠点の支援の下でおこなわれたもので、その研究成果は、国際科学誌Genome Biology (ゲノムバイオロジー)に、2015年4月29日午前1 時(英国時間)にオンライン版で発表されました。
研究の背景
1989年にノックアウトマウス*1(2007年ノーベル賞)が作製されて以来、遺伝子改変生物は基礎研究から遺伝子治療に至るまで、生命科学の発展の原動力となってきました。しかしながら、その作製には長い時間、多大な労力、多額の費用が必要でした。さらにそのような生物の作製は、マウス等、ごく一部の生物に限られてきました。2013年に開発されたゲノム編集*2技術の一つ、CRISPR/Cas(クリスパー/キャス)システム*3は、この状況を一変させ、生命科学に革命をもたらしました。既に、多くの生物で、容易に迅速に遺伝子を破壊したノックアウト生物を作出する事が可能になっています。しかし、より技術レベルが高く、広い応用が期待される、遺伝子の置換や外来遺伝子の挿入(ノックイン*4)は、困難な状況のままでした。今回、研究グループは従来のCRISPR/Casシステムを改良し、ノックイン生物を極めて高い効率で簡便に作製するシステムの開発に成功しました。
研究成果の概要
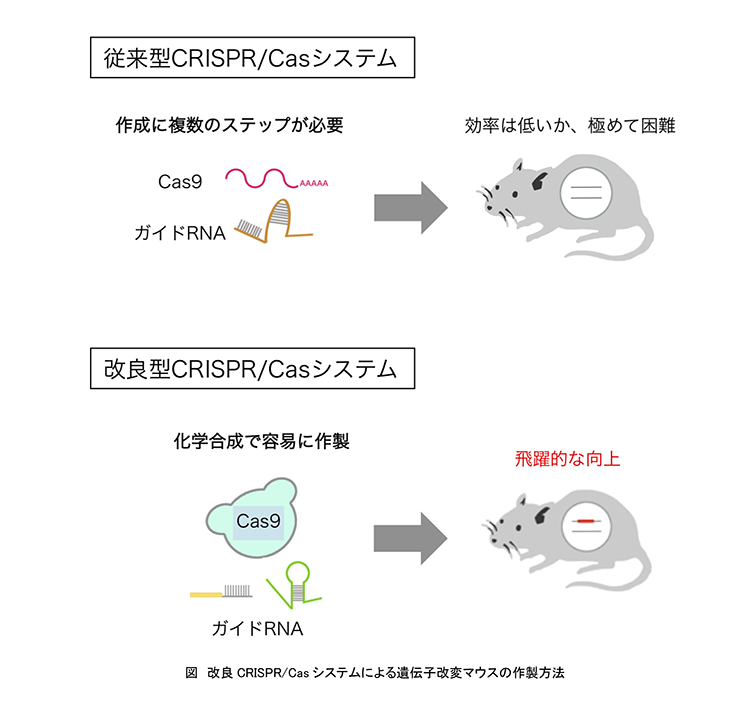
CRISPR/Casシステムを用いた遺伝子改変には、改変する場所を決めるための核酸(ガイドRNA*3)と、その場所でDNAを切断するためのハサミ(Cas9*3)の2つの部品を用います。従来、これらの部品は、大腸菌での遺伝子組換え操作により作製されてきました。研究グループはまず従来法を用いて、蛍光タンパク質遺伝子を含む長い遺伝子を目的の場所に正確に挿入したノックインマウスの作製を試みましたが、意図したとおりのマウスはほとんど得られませんでした。
そこで研究グループは、従来のCRISPR/Casシステムを改良しました。ガイドRNAをより自然界に近い状態にするため、2つに分割し、化学合成により作成しました。2つに分割したガイドRNAをDNAの切断に必要なCas9タンパク質および蛍光タンパク質遺伝子を含む長い遺伝子と伴に受精卵に注入したところ、この長い外来遺伝子が意図したとおりに挿入されたノックインマウスの作成効率は50%に上昇しました。さらにノックインされた遺伝子カセットは、全て次世代に安定に引き継がれる事も分かりました。
改良型CRISPR/Casシステムの利点は、ノックインマウスの作成効率を飛躍的に上昇させたこと、またガイドRNAを2分割したことにより、化学合成が可能になり、ガイドRNAの作成を簡便化した点にあります。
今回の研究成果は、改良型CRISPR/Casシステムを用いる事で、生体の遺伝子を極めて簡便・高効率・自在に改変可能になる事を示唆しています。
そこで研究グループは、従来のCRISPR/Casシステムを改良しました。ガイドRNAをより自然界に近い状態にするため、2つに分割し、化学合成により作成しました。2つに分割したガイドRNAをDNAの切断に必要なCas9タンパク質および蛍光タンパク質遺伝子を含む長い遺伝子と伴に受精卵に注入したところ、この長い外来遺伝子が意図したとおりに挿入されたノックインマウスの作成効率は50%に上昇しました。さらにノックインされた遺伝子カセットは、全て次世代に安定に引き継がれる事も分かりました。
改良型CRISPR/Casシステムの利点は、ノックインマウスの作成効率を飛躍的に上昇させたこと、またガイドRNAを2分割したことにより、化学合成が可能になり、ガイドRNAの作成を簡便化した点にあります。
今回の研究成果は、改良型CRISPR/Casシステムを用いる事で、生体の遺伝子を極めて簡便・高効率・自在に改変可能になる事を示唆しています。
研究成果の意義
わずか2年余りで生命科学に劇的な革命をもたらしたCRISPR/Casシステムを巡り、現在、CRISPR狂騒と称される程の、産学入り乱れた激しい開発競争が世界中で繰り広げられています。効率的なノックイン法の開発は、その最も重要な課題でしたが、今回開発された改良型CRISPR/Casシステムが決着させる事になります。また改良型CRISPR/Casシステムは1980年代から続く、遺伝子改変技術の一つの到達点であり、日本発の世界標準技術となる事が期待されます。CRISPR/Casシステムが大きな注目を集める理由は、動物にかぎらずあらゆる生物のあらゆる遺伝子を改変可能である事から、その影響が基礎医学・生物学研究のみならず、極めて多くの分野にわたるためです。簡便で高効率の改良型CRISPR/Casシステムは、創薬・遺伝子治療から品種改良による食料生産の効率化、バイオエタノールの効率的な生産等のエネルギー資源に至るまで幅広い分野での研究開発を加速する事が期待されます。
用語説明
*1 ノックアウトマウス: 特定の遺伝子が破壊された遺伝子改変マウス。医学生物学研究の最も重要なツール。マリオ・カペッキ、マーティン・エヴァンズ、オリヴァー・スミティーズらにより開発され、2007年のノーベル医学生理学賞の対象となった。胚性幹細胞(ES細胞)を用いて、多くの操作、時間、費用をかけて作製される。応用は、ES細胞が使用可能な生物に限定される。
*2 ゲノム編集: 任意の生物や細胞の任意の遺伝子を、自由に改変する技術。第1世代のZFN(Zinc Finger Nuclease、ジンクフィンガーヌクレアーゼ)、第2世代のTALEN(ターレン、Transcription Activator-Like Effector Nuclease)、第3世代のCRISPR/Casシステム*3がある。学術上および産業上の巨大な利用価値から、激しい開発競争が行われている、現在最も注目を集める技術。
*3 CRISPR/Cas(クリスパー/キャス)システム: 1987年に大阪大学の中田篤男氏(現大阪大学名誉教授)・石野良純氏(現九州大学大学院農学研究院教授)らにより発見された、ヨーグルトの乳酸菌など微生物に広く存在する免疫システム。2013年以降、遺伝子改変に応用され、爆発的に普及している。改変する場所を決めるための核酸(ガイドRNA)と、その場所でDNAを切断するためのハサミ(Cas9)の2つの部品から成るシンプルなシステム。核酸配列を変えるだけでどのような遺伝子にも応用できるため、非常に簡便。
*4 ノックインマウス: 外来の遺伝子カセットが、ゲノムDNAの任意の場所に、正確に挿入された遺伝子改変マウス。ヒト遺伝子を持つヒト化マウスによる疾患研究、正常な遺伝子の挿入による遺伝子治療、蛍光タンパク質の挿入による生体内での細胞の詳細な解析等、医学生物学研究の重要なツール。
*2 ゲノム編集: 任意の生物や細胞の任意の遺伝子を、自由に改変する技術。第1世代のZFN(Zinc Finger Nuclease、ジンクフィンガーヌクレアーゼ)、第2世代のTALEN(ターレン、Transcription Activator-Like Effector Nuclease)、第3世代のCRISPR/Casシステム*3がある。学術上および産業上の巨大な利用価値から、激しい開発競争が行われている、現在最も注目を集める技術。
*3 CRISPR/Cas(クリスパー/キャス)システム: 1987年に大阪大学の中田篤男氏(現大阪大学名誉教授)・石野良純氏(現九州大学大学院農学研究院教授)らにより発見された、ヨーグルトの乳酸菌など微生物に広く存在する免疫システム。2013年以降、遺伝子改変に応用され、爆発的に普及している。改変する場所を決めるための核酸(ガイドRNA)と、その場所でDNAを切断するためのハサミ(Cas9)の2つの部品から成るシンプルなシステム。核酸配列を変えるだけでどのような遺伝子にも応用できるため、非常に簡便。
*4 ノックインマウス: 外来の遺伝子カセットが、ゲノムDNAの任意の場所に、正確に挿入された遺伝子改変マウス。ヒト遺伝子を持つヒト化マウスによる疾患研究、正常な遺伝子の挿入による遺伝子治療、蛍光タンパク質の挿入による生体内での細胞の詳細な解析等、医学生物学研究の重要なツール。
問い合わせ先
<研究に関すること>
東京医科歯科大学難治疾患研究所
分子神経科学分野 田中 光一(タナカ コウイチ)
TEL:03-5803-5864 FAX:03-5803-5843
E-mail:tanaka.aud(ここに@を入れてください)mri.tmd.ac.jp
東京医科歯科大学難治疾患研究所
分子神経科学分野 相田 知海(アイダ トモミ)
TEL:03-5803-5864 FAX:03-5803-0370
E-mail:aida.aud(ここに@を入れてください)mri.tmd.ac.jp
<報道に関すること>
東京医科歯科大学 広報部広報課
〒113-8510 東京都文京区湯島1-5-45
TEL:03-5803-5833 FAX:03-5803-0272
E-mail:kouhou.adm(ここに@を入れてください)tmd.ac.jp
東京医科歯科大学難治疾患研究所
分子神経科学分野 田中 光一(タナカ コウイチ)
TEL:03-5803-5864 FAX:03-5803-5843
E-mail:tanaka.aud(ここに@を入れてください)mri.tmd.ac.jp
東京医科歯科大学難治疾患研究所
分子神経科学分野 相田 知海(アイダ トモミ)
TEL:03-5803-5864 FAX:03-5803-0370
E-mail:aida.aud(ここに@を入れてください)mri.tmd.ac.jp
<報道に関すること>
東京医科歯科大学 広報部広報課
〒113-8510 東京都文京区湯島1-5-45
TEL:03-5803-5833 FAX:03-5803-0272
E-mail:kouhou.adm(ここに@を入れてください)tmd.ac.jp

