2018年度第1回報告(安健博氏)RESEARCH INSTITUTE INFORMATION
旅程
| 2018年10月9日 | 出発(東京・成田 → ブリュッセル → ルーヴェン) |
| 2018年10月10日 | ルーヴェン市内及びルーヴェン カトリック大学視察 |
| 2018年10月11日 10:00~11:00 |
Prof. Massimiliano Mazzoneと挨拶、センター及び研究室の紹介を受ける。 |
| 11:00~12:00 | セミナー実施 |
| 12:00~13:00 | 研究室メンバーとランチ会 |
| 13:00~14:00 | Jens Serneels(Lab Management)と研究室見学。 |
| 14:00~14:45 | Ward Celus(PhD student)Ana Oliveira(PhD student)と面談。 |
| 14:45~15:30 | Federico Virga(PhD student)と面談。 |
| 15:30~16:15 | Christel Vanslembrouck(Human Resource officer)と面談。 |
| 16:15~17:00 | Min Shang(PhD student)と面談。 |
| 2018年10月12日 10:00~10:45 |
Mario di Matteo(Staff scientist)と面談。 |
| 10:45~11:30 | Rosa Martin Pérez(Postdoc) Carla Riera Domingo(PhD student)と面談。 |
| 11:30~12:15 | Ricardo Amorim(PhD student) Chiara Varamo(Visiting scientist)と面談。 |
| 12:15~15:00 | ランチ、センター見学。 |
| 15:00~16:00 | Prof. Massimiliano Mazzoneと共同研究についての打ち合わせ、 今回の訪問についてのまとめ。 |
| 2018年10月13日 | 移動(ルーヴェン → パリ) |
| 2018年10月14日 | パリ滞在 |
| 2018年10月15日 | 帰国(パリ → 東京・羽田) |
行ったセミナー
(タイトル、要旨、日時、ホスト、参加者数(概数)、セミナーのポスター)
| タイトル | MKL1 affects proliferation/survival properties of pro-atherogenic macrophages |
| 日時 | 2018/01/08 13時 |
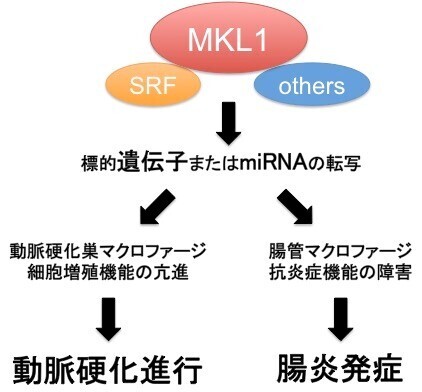
| 要旨 | As an essential component of innate immunity, macrophages respond to metabolic, immunologic and inflammatory stimuli, and contribute to the maintenance of tissue homeostasis. Any aberrant activation of macrophages may lead to the development of inflammatory diseases. Atherosclerosis is a lipid-driven chronic inflammatory disease. Accumulation of lipid-laden macrophages, also called as foam cells, within intima has been recognized as a hallmark of atherosclerotic plaques, and is responsible for the development of atherosclerosis. MKL1 (Megakaryoblastic Leukemia-1) is a Rho-Rock signaling-responsive co-activator of serum response factor, and regulates a variety of cellular functions. We have previously reported from a genome-wide association study that a promoter SNP in MKL1, which conferred higher transcriptional activity, was significantly associated with the susceptibility to coronary artery disease, as well as coronary atherosclerosis. We have previously established a transgenic mouse line, MKL1-TgM, in which human MKL1 was specifically overexpressed in monocyte/macrophage lineage cells under the regulation of CD68 promoter element. We found a skewed activation/polarization of macrophages in the MKL1-TgM and reported that MKL1-TgM was susceptible to DSS-induced colitis, suggesting the functional involvement of MKL1 in the inflammatory process in vivo (An J. et al., Sci Rep 7:13650, 2017). In this study, MKL1-TgM was crossbred onto ApoE-KO background, which is prone to develop atherosclerosis. We investigated whether the MKL1 overexpression would affect the progression of atherosclerosis. I will report the results of our experiments and discuss about the role of MKL1 in atherosclerosis. |
| ホスト | Prof. Massimiliano Mazzone, PhD Laboratory of Tumor Inflammation and Angiogenesis, VIB Center for Cancer Biology Department of Oncology, KU Leuven |
| 参加者数 | 約20名 |
セミナーにおける主な討論・質問点
Q:1 炎症性腸疾患の発症は遺伝要因が大きく関わることが知られているが、なぜ日本における発症率は上昇し続けるのか?
A:1 炎症性腸疾患の遺伝要因は、日本人と欧米人でかなり異なり、例えば欧米人集団においてクローン病との関連が報告された遺伝子変異は日本人集団では稀である。日本における発症率の上昇は遺伝背景と環境要因(食生活の変化など)が関わることが考えられる。
Q:2 MKL1-Tgに見られる腸炎の発症は、マクロファージ抗炎症機能の障害を伴うが、その際T細胞の活性化状況は?
A:2 MKL1-Tgの腸管リンパ球集団でIFN-?、IL-4、IL-17などのサイトカインの産生量が上昇していることは確認できたが、具体的なT細胞亜集団の活性化状況は今後精査する予定である。
Q:3 MKL1は炎症性疾患の発症に伴いマクロファージにおける発現レベルが上昇するようだが、具体的にどのように制御されているのか、また疾患との因果関係は?
A:3 疾患関連解析及び遺伝子欠損マウスを用いた研究結果から、MKL1発現レベルの上昇は炎症性疾患発症に寄与することが示唆されている。しかしながら、MKL1の発現制御機構は未だに不明であり、我々は様々な炎症性疾患の危険因子、典型的な炎症性刺激物などをマクロファージに投与したが、発現レベルに変化は見られなかった。今後引き続き精査する必要がある。
Q:4 CD68プロモーターはマクロファージ全般に制御をもたらしているが、今後具体的なマクロファージ亜集団を標的に解析を進める予定について?
A:4 近年、各組織に存在するマクロファージの多様性及びそれらの役割が注目されており、動脈硬化巣においても少なくとも四種類性質が異なったマクロファージが存在することが報告されている。さらに、これらマクロファージは、マーカーを用いた分類で機能を説明できるよう単純ではない。今回の研究ではMKL1をマクロファージ全般に高発現させているが、今後特定な亜集団に着目し、MKL1の役割の詳細を検討する予定である。
Q:5 MKL1-TgではMKL1が炎症性疾患へ寄与することがわかったが、プロモーター多型がもたらす程度の発現変化が、果たして疾患に影響するかどうか?
A:5 MKL1プロモーター多型を持つマクロファージにおいて、MKL1の発現量がどれほど上昇するか、また疾患への影響について具体的に解析できていないが、複数の実験系でMKL1の発現制御を行った結果から、MKL1のマクロファージに及ぼす影響(細胞増殖など)は確認できたため、MKL1のマクロファージにおける役割は確実だと考えられる。また、今回我々が作製したMKL1-Tgを用いた研究から、マクロファージにおけるMKL1の高発現性は、少なくとも炎症性疾患発症の一つの危険因子であることが強く示された。
A:1 炎症性腸疾患の遺伝要因は、日本人と欧米人でかなり異なり、例えば欧米人集団においてクローン病との関連が報告された遺伝子変異は日本人集団では稀である。日本における発症率の上昇は遺伝背景と環境要因(食生活の変化など)が関わることが考えられる。
Q:2 MKL1-Tgに見られる腸炎の発症は、マクロファージ抗炎症機能の障害を伴うが、その際T細胞の活性化状況は?
A:2 MKL1-Tgの腸管リンパ球集団でIFN-?、IL-4、IL-17などのサイトカインの産生量が上昇していることは確認できたが、具体的なT細胞亜集団の活性化状況は今後精査する予定である。
Q:3 MKL1は炎症性疾患の発症に伴いマクロファージにおける発現レベルが上昇するようだが、具体的にどのように制御されているのか、また疾患との因果関係は?
A:3 疾患関連解析及び遺伝子欠損マウスを用いた研究結果から、MKL1発現レベルの上昇は炎症性疾患発症に寄与することが示唆されている。しかしながら、MKL1の発現制御機構は未だに不明であり、我々は様々な炎症性疾患の危険因子、典型的な炎症性刺激物などをマクロファージに投与したが、発現レベルに変化は見られなかった。今後引き続き精査する必要がある。
Q:4 CD68プロモーターはマクロファージ全般に制御をもたらしているが、今後具体的なマクロファージ亜集団を標的に解析を進める予定について?
A:4 近年、各組織に存在するマクロファージの多様性及びそれらの役割が注目されており、動脈硬化巣においても少なくとも四種類性質が異なったマクロファージが存在することが報告されている。さらに、これらマクロファージは、マーカーを用いた分類で機能を説明できるよう単純ではない。今回の研究ではMKL1をマクロファージ全般に高発現させているが、今後特定な亜集団に着目し、MKL1の役割の詳細を検討する予定である。
Q:5 MKL1-TgではMKL1が炎症性疾患へ寄与することがわかったが、プロモーター多型がもたらす程度の発現変化が、果たして疾患に影響するかどうか?
A:5 MKL1プロモーター多型を持つマクロファージにおいて、MKL1の発現量がどれほど上昇するか、また疾患への影響について具体的に解析できていないが、複数の実験系でMKL1の発現制御を行った結果から、MKL1のマクロファージに及ぼす影響(細胞増殖など)は確認できたため、MKL1のマクロファージにおける役割は確実だと考えられる。また、今回我々が作製したMKL1-Tgを用いた研究から、マクロファージにおけるMKL1の高発現性は、少なくとも炎症性疾患発症の一つの危険因子であることが強く示された。
派遣で得られたこと
今回の派遣プログラムを通して、受け入れ先であるProf. Mazzoneの研究室において学術交流及び情報交換を行い、非常に有意義な時間を過ごすことができ、親密な関係を築くことができた。また、セミナーを含む派遣プログラムの内容が評価され、今後共同研究の可能性を広げることができた。
マクロファージは様々な炎症性疾患の発症及び進行において重要な役割を果たすことが知られているが、Prof. Mazzoneの研究室では、腫瘍微小環境における腫瘍関連マクロファージの役割を精力的に解析してきた。我々の研究から、マクロファージにおけるMKL1の高発現性はマクロファージの様々な機能に大きく影響することが判明し、腫瘍微小環境においても、腫瘍細胞へ何らかの影響を及ぼすことが考えられた。実際、MKL1を高発現するマクロファージでは、腫瘍細胞の機能と関係する遺伝子の発現レベルが大きく変化していることが分かった。しかしながら、in vivoの癌モデルは多数存在かつ複雑なため、どの実験系へアクセスするかの判断は現段階では困難である。一つの案として、まずin vitroの共培養の系を用いて、マクロファージにおけるMKL1の高発現性が腫瘍細胞のどの遺伝子あるいはどの遺伝子群へ影響するか、さらに関連する細胞機能への影響を検討する。その結果から疾患背景を交えて、in vivoの癌モデルにアクセスする。病理像に関しては組織変化を丁寧に評価することが必要なため、共同研究を進められた。
VIB Center for Cancer Biologyでは各研究室間の連携と、コアラボのサポートが非常に機能していると感じた。実際、研究室間の交流を促すための大小セミナー室、食事スペースなどが多数設置されており、また他研究室へは気軽にアクセスできる雰囲気を感じた。一方、各コアラボには専門知識と技術を備えたスタツフが常時滞在しており、研究テーマ及びデータ自体に関する相談が随時可能であり、効率の良さやコミュニケーションの楽しさを感じた。VIB Center for Cancer Biologyでは、地元のベルギー人の割合はわずかで、非常にグローバルな環境である。VIBでは優れた人材世界中からリクルートできるようHuman Resource部門が機能している。
最後になりますが、このような貴重な海外訪問の機会をくださった難治疾患研究所海外派遣プログラム、ご協力くださった難治疾患研究所事務の方々、ご指導ご意見くださった分子病態分野の皆様方に心より感謝申し上げます。
マクロファージは様々な炎症性疾患の発症及び進行において重要な役割を果たすことが知られているが、Prof. Mazzoneの研究室では、腫瘍微小環境における腫瘍関連マクロファージの役割を精力的に解析してきた。我々の研究から、マクロファージにおけるMKL1の高発現性はマクロファージの様々な機能に大きく影響することが判明し、腫瘍微小環境においても、腫瘍細胞へ何らかの影響を及ぼすことが考えられた。実際、MKL1を高発現するマクロファージでは、腫瘍細胞の機能と関係する遺伝子の発現レベルが大きく変化していることが分かった。しかしながら、in vivoの癌モデルは多数存在かつ複雑なため、どの実験系へアクセスするかの判断は現段階では困難である。一つの案として、まずin vitroの共培養の系を用いて、マクロファージにおけるMKL1の高発現性が腫瘍細胞のどの遺伝子あるいはどの遺伝子群へ影響するか、さらに関連する細胞機能への影響を検討する。その結果から疾患背景を交えて、in vivoの癌モデルにアクセスする。病理像に関しては組織変化を丁寧に評価することが必要なため、共同研究を進められた。
VIB Center for Cancer Biologyでは各研究室間の連携と、コアラボのサポートが非常に機能していると感じた。実際、研究室間の交流を促すための大小セミナー室、食事スペースなどが多数設置されており、また他研究室へは気軽にアクセスできる雰囲気を感じた。一方、各コアラボには専門知識と技術を備えたスタツフが常時滞在しており、研究テーマ及びデータ自体に関する相談が随時可能であり、効率の良さやコミュニケーションの楽しさを感じた。VIB Center for Cancer Biologyでは、地元のベルギー人の割合はわずかで、非常にグローバルな環境である。VIBでは優れた人材世界中からリクルートできるようHuman Resource部門が機能している。
最後になりますが、このような貴重な海外訪問の機会をくださった難治疾患研究所海外派遣プログラム、ご協力くださった難治疾患研究所事務の方々、ご指導ご意見くださった分子病態分野の皆様方に心より感謝申し上げます。


(「2018年度難治疾患研究所国際研究者海外派遣プログラム報告書」より)
