石野研究室
石野研究室
東京医科歯科大学難治疾患研究所・エピジェネティクス分野
〒113-8510 東京都文京区湯島1-5-45tel: 03-5803-4862 fax: 03-5803-4863
(医歯学総合研究棟II期 23階 map)
 石野研究室
石野研究室哺乳類の胎盤は、胎児と母体間の物質交換の場となる哺乳類の胎生に必須な臓器であり、哺乳類が進化の過程で独自に獲得したものである。これまでに、胎盤形成の初期段階で必要となる遺伝子は、様々なものが報告されていたが、胎児と母体間でガスや栄養交換が活発に行われる胎生後期に必要となる遺伝子はほとんど知られていなかった。今回、私達はPeg11/Rtl1 (paternally expressed 11/retrotransposon-like 1)が胎生後期の胎盤で重要な役割を担っていることを発見し、報告した。面白いことにPeg11/Rtl1は、フグのゲノムに存在するsushi-ichi(スシイチ)というレトロトランスポゾンと高い相同性を持つ、レトロトランスポゾン由来の遺伝子であり、哺乳類の中でも真獣類にのみ保存されている。さらに、私達の研究室ではPeg10もまた、Peg11/Rtl1と同じレトロトランスポゾンを起源とし、胎盤の初期形成の段階で必須な働きを担っていることを報告した。Peg11/Rtl1、Peg10の胎盤での役割と、それらの起源を考え合わせると、哺乳類の胎盤進化にはレトロトランスポゾンが強く関与していたことが見えてきた。
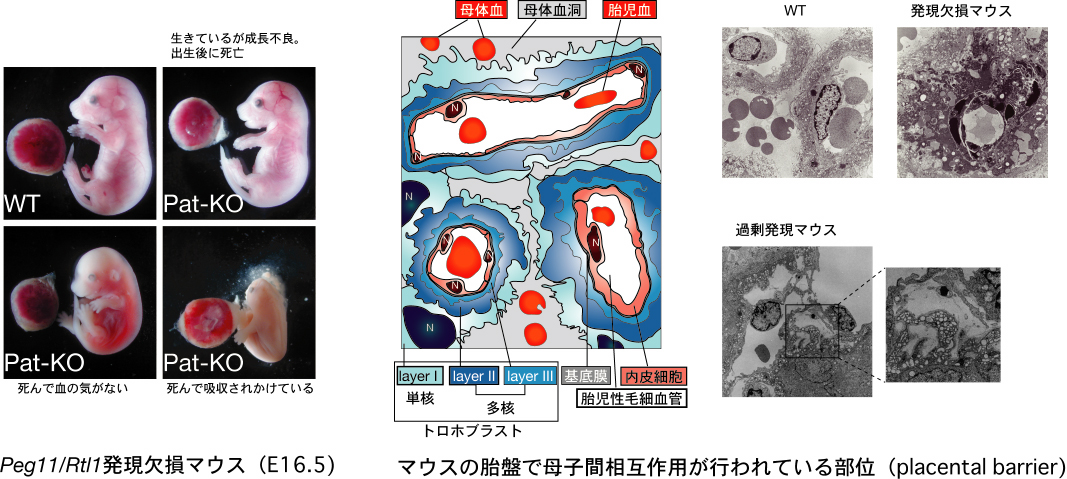
今回、私達はジーンターゲッティングによりPeg11/Rtl1の発現欠損マウスと過剰発現マウスの両方を作成し、解析を行った。その結果、Peg11/Rtl1発現欠損マウスの半数は胎生後期に致死となり、残りの半数は低体重で生まれて出生後1日で致死となった。またPeg11/Rtl1過剰発現マウスは胎児の成長は正常だが、胎盤の過形成が起こり、出生後に致死となった。
胎盤の形態を詳細に調べた所、発現欠損マウスでは胎児-母体間の栄養交換の場となる胎児毛細血管が変性したトロホブラスト細胞によって詰まっており、血流がなくなっていると考えられた。私達は放射性同位体を用いた実験から、実際に胎児-母体間の栄養交換効率が低下していることを確認した。一方、過剰発現マウスでは、胎盤の胎児性毛細血管が拡張し、毛細血管を構成するトロホブラスト細胞が栄養飢餓状態となっていた。私達は免疫染色によって、Peg11/Rtl1タンパク質が、ノックアウトマウスで異常が見られた、胎盤の胎児性毛細血管の内皮細胞で発現していることを見いだした。これらのことから、Peg11/Rtl1は胎盤の内皮細胞で発現し、周辺のトロホブラスト細胞との相互作用を制御する、哺乳類の胎生に重要な遺伝子であることが分かった。
マウスのPeg11/Rtl1は12番染色体遠位部のインプリンティング領域に存在しており、12番染色体母性ダイソミーマウスおよび父性ダイソミーマウスは、いずれも出生前後に致死となる。今回の私達の結果は、これらのマウスの致死の主な原因がPeg11/Rtl1の発現欠損と過剰発現であることを示している。また、ヒトのPEG11/RTL1は、マウスPeg11/Rtl1が存在する領域と相同な14番染色体q32領域のインプリンティング領域内に存在し、14番染色体の母性ダイソミーと父性ダイソミーでは、重篤なものも含めて幾つもの症状が見られる。今回私達はマウスの解析と並行して国立成育医療センター研究所の緒方部長、鏡博士らと共同研究を行い、ヒトにおいてもPEG11/RTL1が胸骨形成異常や羊水過多、腹直筋開裂などの症状の主要原因遺伝子であることを突き止めた。(本共同研究では、ヒトPEG11/RTL1の役割を明らかにした以外に、14番染色体のインプリンティング領域の遺伝子発現制御にIG-DMR(intergenic-differentially methylated region)のDNAメチル化が重要であることを報告した。)
哺乳類の中で有袋類(コアラやワラビーなど)は卵黄嚢胎盤を、真獣類(ヒトやマウスなど)は漿尿膜胎盤を発達させた。これら2種類の胎盤の胎児-母体間の栄養交換効率は、漿尿膜胎盤の方が高く、真獣類の妊娠期間は長い一方、卵黄嚢胎盤の有袋類の妊娠期間は短い。(有袋類は発生の早い段階で出産し、その後腹部の袋の中で新生児を育てる。)哺乳類の胎盤の様に、進化の過程で新たに臓器を発達させるためには、それまでに存在していた遺伝子ネットワークを利用すると共に、そのネットワークを補完するための新規遺伝子が必要になると考えられる。哺乳類の胎盤進化においてその証拠となるのが、Peg11/Rtl1と前述のPeg10と言える。Peg11/Rtl1は真獣類に特異的な遺伝子であり、真獣類特有の妊娠期間の長い胎生を発達させたと考えられる。Peg10は真獣類と有袋類に存在しており、真獣類では胎盤形成の初期段階で機能していることから、真獣類と有袋類の胎生進化に寄与したと考えられる。
Peg10の解析によって、レトロトランスポゾンは新規遺伝子の発生源となっている、というS. J. Gouldらによって提唱された"exaptatio"の証拠を示した。今回、Peg11/Rtl1の研究成果から新たに見えてきたことは、これら二つの遺伝子が同じレトロトランスポゾンを起源としているにも関わらず、互いに異なる機能を獲得し、別々に胎盤進化に寄与したということである。このことは、それぞれのタンパク質が異なる機能モチーフを持っていることからも示唆される。すなわち、レトロトランスポゾンから生じる新規機能遺伝子は、似通ったものになるのだけではなく、様々な機能を獲得し得るということである。(exaptationによって様々な新規遺伝子が発生している!)私達は、レトロトランスポゾンを起源とする遺伝子の探索と、機能解析を行い、レトロトランスポゾンの生物学的意義を探ろうとしている。
私達の研究室では、哺乳類の胎盤進化はレトロトランスポゾンによって促進されている、という仮説を提唱している。とある研究室員がこの仮説をDream Island Hypothesis(夢の島仮説)と命名した。名前の由来は、東京都江東区にあるゴミを埋め立てて作られた夢の島である。レトロトランスポゾンはかつてジャンク(がらくた)と呼ばれていた。人間はゴミを埋め立てて海に島を作った。しかし、哺乳類はそれよりも1億年以上も前にゲノムのがらくたを利用して胎盤(子宮内の胎児からは、胎盤は島のように見えるだろう)を作った(のかもしれない)。