細胞を浄化する新たなメカニズムを発見FINDING / PRESS
-癌、神経疾患などの新規治療法開発に期待-
清水重臣教授らの研究成果がNatureのオンライン版に掲載されました。
「細胞を浄化する新たなメカニズムを発見」
清水重臣教授等 (難治病態研究部門病態細胞生物学分野)
"Discovery of Atg5/Atg7-independent alternative macroautophagy"
Yuya Nishida, Satoko Arakawa, Kenji Fujitani, Hirofumi Yamaguchi, Takeshi Mizuta, Toku Kanaseki, Masaaki Komatsu, Kinya Otsu, Yoshihide Tsujimoto & Shigeomi Shimizu
Nature 461, 654-658 (1 October 2009)
『オートファジー(自食作用)』とは、細胞が自己構成成分を分解・処理する生体機構を指し、酵母からヒトに至るまで、すべての真核生物が保有しています。この機構は、細胞浄化(古い蛋白質やオルガネラを分解し、新陳代謝に貢献します)やストレス応答などにおいて重要な役割を果たしており、種々の疾患にも深く関連しています。
これまでは、哺乳動物におけるオーファジーの分子機構は、酵母のそれと基本的に同じ過程をたどると信じられてきました。即ち、酵母におけるオートファジーに不可欠な分子群(Atg5、Atg7、Atg8など)は、哺乳動物においてもオートファジーを支配していると考えられてきました。その結果、Atg5やAtg7を抑制することは、オートファジーを抑制する事と同義に翻訳され、LC3(Atg8の哺乳動物相同分子)の変化の有無はオートファジー誘導の有無を示していると考えられてきました。しかし、我々は、Atg5欠損マウスが周産期まで正常であることや、哺乳動物では酵母よりも進化している可能性があることより、新たなオートファジー機構が存在しうると考えました。
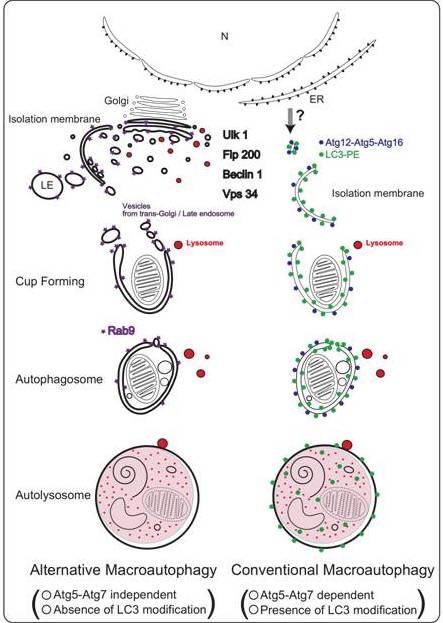
実際に、野生型マウス線維芽細胞とAtg5欠損マウス線維芽細胞に、DNA傷害によるストレスを負荷しまうと、両方の細胞とも、ほぼ同程度にオートファジーが観察されました。しかしながら、Atg5欠損細胞に見られるオートファジーは野生型細胞のオートファジーと異なり、LC3の変化を伴うことはありませんでした。これらの結果より、我々はAtg5を必要とするオートファジーを“conventional macroautophagy”、新たなオートファジーを“alternative macroautophagy”と命名しました。“alternative macroautophagy”の実行には、形態学的にはtrans-Golgiとendosome(輸送小胞)の関与が示唆され、実行に関わる分子としてはUlk1、PI3kinase、Rab9などが重要でした。また、生体内では、赤血球の最終分化過程においてミトコンドリアの処理を担っていました。
今後は、分子機構の詳細を解明するとともに、生理的、病理的役割を明らかにして行く必要があります。
Yuya Nishida, Satoko Arakawa, Kenji Fujitani, Hirofumi Yamaguchi, Takeshi Mizuta, Toku Kanaseki, Masaaki Komatsu, Kinya Otsu, Yoshihide Tsujimoto & Shigeomi Shimizu
Nature 461, 654-658 (1 October 2009)
『オートファジー(自食作用)』とは、細胞が自己構成成分を分解・処理する生体機構を指し、酵母からヒトに至るまで、すべての真核生物が保有しています。この機構は、細胞浄化(古い蛋白質やオルガネラを分解し、新陳代謝に貢献します)やストレス応答などにおいて重要な役割を果たしており、種々の疾患にも深く関連しています。
これまでは、哺乳動物におけるオーファジーの分子機構は、酵母のそれと基本的に同じ過程をたどると信じられてきました。即ち、酵母におけるオートファジーに不可欠な分子群(Atg5、Atg7、Atg8など)は、哺乳動物においてもオートファジーを支配していると考えられてきました。その結果、Atg5やAtg7を抑制することは、オートファジーを抑制する事と同義に翻訳され、LC3(Atg8の哺乳動物相同分子)の変化の有無はオートファジー誘導の有無を示していると考えられてきました。しかし、我々は、Atg5欠損マウスが周産期まで正常であることや、哺乳動物では酵母よりも進化している可能性があることより、新たなオートファジー機構が存在しうると考えました。
実際に、野生型マウス線維芽細胞とAtg5欠損マウス線維芽細胞に、DNA傷害によるストレスを負荷しまうと、両方の細胞とも、ほぼ同程度にオートファジーが観察されました。しかしながら、Atg5欠損細胞に見られるオートファジーは野生型細胞のオートファジーと異なり、LC3の変化を伴うことはありませんでした。これらの結果より、我々はAtg5を必要とするオートファジーを“conventional macroautophagy”、新たなオートファジーを“alternative macroautophagy”と命名しました。“alternative macroautophagy”の実行には、形態学的にはtrans-Golgiとendosome(輸送小胞)の関与が示唆され、実行に関わる分子としてはUlk1、PI3kinase、Rab9などが重要でした。また、生体内では、赤血球の最終分化過程においてミトコンドリアの処理を担っていました。
今後は、分子機構の詳細を解明するとともに、生理的、病理的役割を明らかにして行く必要があります。