 石野研究室
石野研究室
東京医科歯科大学難治疾患研究所・エピジェネティクス分野
〒113-8510 東京都文京区湯島1-5-45tel: 03-5803-4862 fax: 03-5803-4863
(医歯学総合研究棟II期 23階 map)
 石野研究室
石野研究室小林 慎 Shin Kobayashi

哺乳類におけるエピジェネティクス制御―X染色体不活性化をモデルとして-
私たちヒトを含む哺乳類の発生は、精子と卵子が受精することから始まります。1個の受精卵が細胞分裂を繰り返し、異なる種類の細胞からなる組織や器官が形成され体が形作られます。 どの細胞も受精卵と同じDNA配列を遺伝情報として持っているにも関わらず、なぜ1個体内で異なる種類の細胞が存在できるのでしょうか?近年の研究結果から、各々の細胞で必要、 または不必要な遺伝子の 発現スイッチをON、OFFにする仕組みが存在することが分かってきました。この「仕組み」または、その「仕組みを研究する学問」をエピジェネティクスと呼びます。 更にエピジェネティクスは、異なる種類の細胞への分化に関わるばかりでなく、 様々な生命現象に重要な働きを持つことが分かってきました。例えば代表的な例である「ゲノム・インプリンティング(注*)」 「X染色体の不活性化(下記研究テーマ1参照)」は正常な個体発生に必須なエピジェネティクス制御です。更に、これらの制御の異常はヒトの癌など様々な疾患やiPS細胞のリプログラミングの失敗を引き起こすことが報告されており、 特に医学分野から注目されています。実際、「ゲノム・インプリンティング」については精神遅滞を示すPrader-Willi症候群やAngelman症候群、Wilms腫瘍では原因となるインプリント遺伝子が同定されていますし、 「X染色体不活性化」はiPS細胞を含む多能性幹細胞の未分化状態を評価する指標 として利用され始めました。また薬の分野では、例えばヒストン脱アセチル化酵素阻害剤や、 DNAメチル基転移酵素阻害剤などエピジェネティクスを担う酵素に作用する化合物が、抗ガン剤として臨床応用され始めています。エピジェネティクスはこの様に注目を集める現象ですが、 その異常で起こるヒト疾患の全貌はまだ明らかにはされておらず、制御メカニズムの解明も進んでいません。我々は、これまで根治が難しかった疾患とエピジェネティックスの関りを発見し、 現在その制御機構の全容解明を目指しています。とくに、「ゲノム・インプリンティング」、「X染色体の不活性化」に注目し、これまで報告の殆どなかったX染色体上に発見したインプリント遺伝子を 解析の切り口にして、 哺乳類の初期発生におけるエピジェネティクス制御機構の解明に取り組んでいます。
哺乳類の性は、性染色体がXX(雌)かXY(雄)かにより決まります。従来の遺伝学で考えると、雌では2本のX染色体上の全遺伝子が働くことになり、その発現量は2倍になります。 しかし、実際は片方1本のX染色体上の全遺伝子の発現スイッチはOFFになっており、雌雄間に生じるX染色体の本数の違いを打ち消す仕組みが雌には存在することが分かりました。 このように同じ細胞内にある同じDNA配列でありながら、異なる発現状態(ONまたはOFF)を決める仕組みが「X染色体の不活性化」と呼ばれるエピジェネティクス制御です。 その仕組みの実態は DNAのメチル化等の化学修飾であることが示されていますが、X染色体上の全遺伝子の発現スイッチをOFFにする詳細な機構については Xist と呼ばれるタンパク質をコードしない long non-coding RNA (lncRNA) が重要な役割を果たすこと以外不明な点が多いのが現状です。我々のグループは、X染色体の不活性化機構の解明を目指し、 Xist以外に不活性化に働く因子を探すことに取り組んでいます。 これまでに不活性化が始まるマウス初期胚(胚盤胞)に注目し、雌でのみ発現する因子を探しました。この時期は一般的に性差が生じると考えられている 生殖巣の分化よりはるか前の時期であり、 もしこの時期に雌でのみ発現する遺伝子が見つかれば、不活性化に関わる有力な候補であると考え研究を開始しました。ただ、発生の非常に早い時期の雌胚と雄胚を比べるにあたり、解決すべき問題がありました。 胚盤胞は 見た目で性が判別できないのです。我々はこの問題を克服するために、X染色体にGFPレポーター遺伝子を挿入した遺伝子組換えマウス(XGFPマウス)を利用し、蛍光の有無で雌雄の判別ができるよう工夫を凝らしました(図1)。

これまで誰も判別できなかった初期胚の雌雄のサンプルを比べたところ、性分化では差が無いと考えられていた着床前時期に、雌でのみ発現する複数の遺伝子やlncRNAを発見することに成功しました (ref. 3-5 )。 更に、これらの遺伝子は、Xist 同様に「ゲノム・インプリンティング」(注*)を受けていました。実はこの時期には父親由来のX染色体が選択的に不活性化され、精子から由来したX染色体の上の多くの遺伝子の発現が 抑制されます。しかし、驚いたことに我々が見つけた遺伝子は不活性化を受けた父親由来のX染色体から発現していました(図2)。 このような片親由来の染色体からのみ発現する遺伝子はインプリント遺伝子と呼ばれ、 我々の発見した遺伝子群は、Xist以外に見つかった父親由来のX染色体から発現する初めてのインプリント遺伝子です。更にこれらの遺伝子は、既に報告のあったX染色体上の不活性化制御領域に位置することから、 この結果を不活性化機構に働く新たな候補因子として報告しました (ref. 3)。このような独自の発見により、これまで未解明であった不活性化機構解明の新たな手がかりを得ることに成功しました。

遺伝子の機能を検証する重要な方法として、その遺伝子を人工的に破壊したノックアウト(KO)マウスを作製し解析する手法が挙げられます。我々の発見したインプリント遺伝子が雌のみで発現することにどのような意味 があるのでしょうか?その機能を明らかにするため、現在複数のインプリント遺伝子についてKOマウスを作製し解析を行っています(ref.2)。
(注*)ゲノム・インプリンティング:哺乳類の少数の遺伝子は、片方の親らから由来したときのみ発現するエピジェネティクス制御を受ける。
さらに上記の研究テーマで用いた雌雄の性が判別できる系(図1、XGFPマウス)を発展させ、以下の研究テーマでは遺伝子組換え技術を用い「X染色体の不活性化状態を可視化できる"Momiji"マウス (赤、緑、黄色から連想される「紅葉」に由来します。)」の開発に成功しました。 このマウスを使うと、発生 においてダイナミックに変化する「エピジェネティクス」の状態を個体を生かしたまま可視化できるようになります。このMomijiマウスはエピジェネティクス研究の重要なツールである ばかりでなく、iPS細胞のリプログラミング解析などの幹細胞研究にも非常に役立ちます。
将来の再生医療を考えると、iPS細胞のリプログラミング等を含む多能性幹細胞の理解を深める基礎研究は重要です。我々は、H23年から採択されたさきがけ研究「X染色体再活性化 ライブイメージング技術を用いた幹細胞研究」で、幹細胞の未分化性を可視化する技術開発に取り組みました。
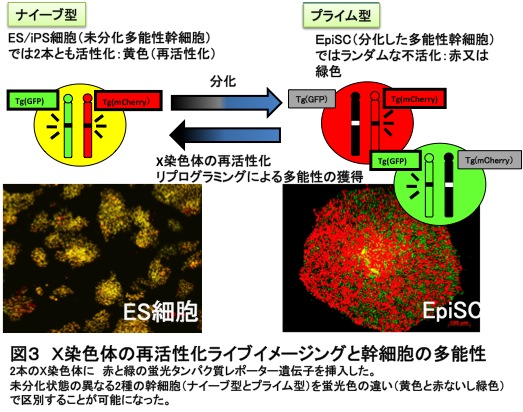
近年、ヒトiPS細胞の樹立が報告され、あらゆる種類の細胞、組織に分化できる多能性幹細胞を用いた再生医療への応用に期待が集まっています。これまでの研究から、多能性幹細胞には未分化状態の異なる 細胞種集団があり、種々の細胞に分化する能力(多能性)に違いがあることが分かってきました。未分化状態に近い「ナイーブ状態」と分化が進んだ「プライム状態」です。再生医療への応用を考えるとより多くの種類の 細胞に分化でき、他の個体とのキメラ動物を作ることできるナイーブ状態の細胞の方が、応用範囲が広いと考えられます。ただ、これら異なる状態の細胞を生かしたまま区別する方法が無いことが、幹細胞研究の一つの障害になっていま した。そこで、我々は幹細胞の多能性の指標として利用されている「X染色体再活性化」に注目しました。(幹細胞の多能性とX染色体の再活性化についての詳しい解説はDeuve JLの総説を参照ください。 PubMed Link)。現在、幹細胞の多能性を評価するマーカーとして「X染色体の再活性化」は優れた指標と考えられています(ref.1)。 我々のグループではマウスを材料に、X 染色体の活性化状態を生きた細胞で観察するため、2本あるX染色体それぞれの狙った部位に、赤(mCherry)と緑(eGFP)のレポーター遺伝子を挿入した遺伝子組換え動物を開発し、 「Momiji」マウスと名前をつけました。図3に示すようにこの「Momijiマウス」から樹立した多能性幹細胞は、 プライム状態(例:マウスエピブラスト幹細胞:EpiSC)ではX染色体の不活性化を示し赤または緑の単色の蛍光が検出されます。一方、ナイーブ状態(例、マウス胚性幹細胞:ES細胞)では再活性化が起こり、 赤と緑の蛍光が同時に発現し黄色い蛍光を示します。このように、我々は遺伝子組換えマウスを利用し、X染色体の活性化状態を可視化することにより、初めて細胞を生かしたまま幹細胞の多能性を判別できる技術開発に 成功しました(図3、ref.2&3.)。
現在この技術を利用し、iPS細胞のリプログラミング機構の解明など様々な幹細胞研究課題に取り組んでいます。また、この系の利点は多能性幹細胞それ自体の研究やiPS細胞に関するリプログラミング研究に役立つ ばかりでなく、発生学におけるエピジェネティクス研究にも有用であることです。マウスの蛍光を見るだけで、発生に従い時事刻々と変化するX染色体の動的なエピジェネティックな変化が一細胞レベルで解析できます。 この系を利用することにより今まで困難であった「発生におけるエピジェネティクスの変化 」を個体を生かしたまま観察することに成功し、報告しました(ref.3 では、着床前胚で、まさにX染色体の不活性化が始まる 瞬間を捉えることに成功しました。movie1 Link)。一細胞レベルで解析することにより、今まで検出ができなかった エピジェネティクス制御のバラツキが一個体の中にあることが分かりました。生物とは、一見綺麗に制御されているように見えますが、一つの胚に注目すれば個々の細胞レベルではバラツキがあることが一目瞭然で分かるよう になりました。現在、”Momijiマウス”を用い発生、組織再生、および発ガン機構など、多能性幹細胞が関わる可能性のある様々な研究課題に取り組んでいます。このように我々は遺伝子組み換え動物を中心として我々独自の技術、 材料を利用し、幹細胞研究や発生、疾患発症機構におけるエピジェネティクスを対象に研究を進めています。将来これらの研究は、再生医療の臨床応用やヒト疾患の発症機構の解明、治療に繋がることが期待されます。

*corresponding Author
私は哺乳類の発生に関わるエピジェネティクスについて基礎研究を続けてきました。研究では教科書に書かれていることが必ずしも正しいとは限らず、常に新しい発見が生まれます。 私はこれまでの自身の研究の中で、小さいながらもこの様な新しい発見をする幸運に恵まれました。通説で考えられていたよりかなり早い時期から、雌雄の胚に性差が生じることを世界で初めて報告することができたのです(ref.6, 7)。 私たちのグループでは他に例のない課題に独自の材料を使って取り組み、新しい分野を造り出すことを目指して日々努力を続けています。学生と一緒に研究の面白さを共有し、常識にとらわれない発想、 他の人が持っていない独自の技術開発を目指し、粘り強く問題に取り組む姿勢を見せられるよう努力しています。日進月歩で進む研究の世界は個人単位でありながら、共同組織で行われるのが現状です。 私の学んだコミュニケーション能力、協力関係の大切さを学生に伝える努力を続けていきたいと考えています。
研究は個人が単位でありながら、ひとつの課題に組織で取り組むものです。学生と教員が一緒になり、情報を収集し分析し、自ら立てた問題に自発的に取り組むことにより、解決を目指します。 研究にはあらかじめ答えが分かっている課題はなく、教員も学生も解答を知りません。研究の過程ではグループ内で徹底的な討論により、最善の解決策を模索します。 グループの中には様々な個性を持った学生が含まれますが、グループでは研究の質を高く維持する為に、学生の意識を高め自発的に問題に取り組むよう促すことを心がけています。 また、組織で行う研究活動を行には必要最低限のルールがあり、そのルールに基づいて各個人が、能力を最大限に伸ばし、自由な発想で楽しく研究を行うことが望ましいと考えています。 学生がお互いのテーマに興味を持ち、情報交換や議論を積極的に行うことで、刺激し合い成長できるよう手助けをしたいと考えています。
JST広報誌の研究者紹介 「先駆ける科学人」 で取り上げられました。
tel: 03-3599-8137(研究室)
fax: 03-3599-8141