丂丂侾丏寣媴偺桼棃 丂丂俀丏旕摿堎揑杊屼婡峔偲摿堎揑杊屼婡峔 丂丂俁丏柶塽偲儕儞僷媴 丂丂係丏柶塽墳摎 丂丂俆丏峈尨偲峈懱 丂丂俇丏峈懱暘巕
丂娭楢偡傞僒僀僩偲儕儞僋乮偙偺儁乕僕傊栠傞偲偒偼僽儔僂僓乕偺栠傞傪慖傫偱偔偩偝偄乯 丂丂The Human Immune System 丂丂僠儏乕儗儞戝妛Infection&Immunity 峏怴擔丗2001擭11寧01擔
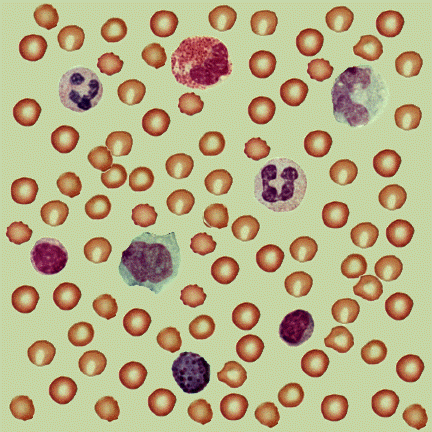
丂侾擭偺惗暔妛幚尡偱偍偙側偭偨丄寣塼揾晍昗杮偺娤嶡傪巚偄弌偟偰傎偟偄丅壗庬椶偐偺寣媴傪娤嶡偟偰丄僗働僢僠偟偨偼偢偱偁傞丅
丂寣塼拞偵偼師偺傛偆側寣媴嵶朎偑懚嵼偡傞丅
丂丂丂仠愒寣媴乮red blood cell, erythrocyte乯
丂丂丂丂丂丂巁慺偲擇巁壔扽慺傪塣斃
丂丂丂仠敀寣媴乮 white blood cell, leucoocyte乯
丂丂丂丂丂丂梓棻敀寣媴乮granulocyte乯亖懡宆妀敀寣媴乮polymorphonuclear
leucocyte乯
丂丂丂丂丂丂丂丒岲拞媴乮neutrophil乯丂丂丂
怘嶌梡偑嫮偄丄僶僋僥儕傾側偳傪婷怘偡傞
丂丂丂丂丂丂丂丒岲巁媴乮acidophil, eosinophil乯
戝宆偺婑惗惗暔傪峌寕丄傾儗儖僊乕惈墛徢偵娭梌
丂丂丂丂丂丂丂丒岲墫婎媴乮basophil乯丂丂丂
僸僗僞儈儞傪曻弌
丂丂丂丂丂丂扨媴乮monocyte乯丂丂丂丂丂丂丂怘嶌梡偑嫮偄丄慻怐傊擖傝儅僋儘僼傽乕僕偵側傞
丂丂丂丂丂丂儕儞僷媴乮lymphocyte乯
丂丂丂丂丂丂丂丒俛嵶朎乮B cell乯丂丂丂丂丂丂丂峈懱傪嶻惗
丂丂丂丂丂丂丂丒俿嵶朎乮T cell乯丂丂丂丂丂丂丂僂僀儖僗偵姶愼偟偨嵶朎傪嶦偡丄懠偺敀寣媴偺妶摦傪挷愡
丂丂丂丂丂丂僫僠儏儔儖僉儔乕乮俶俲乯嵶朎丂僂僀儖僗偵姶愼偟偨嵶朎傗庮釃嵶朎傪嶦偡
丂丂丂仠寣彫斅乮platelet乯
丂丂丂丂丂丂寣塼嬅屌
丂師偺恾偱丄偳傟偑偳傟偩迋﹤韨﹤閭緜雮﹣B

http://www.tulane.edu/~dmsander/WWW/MBChB/2a.html傛傝
丂偙傟傜偺寣媴嵶朎偼宍傗婡擻偼堎側傞偑丄傕偲傪偨偩偣偽摨偠嵶朎偵桼棃偡傞丅崪悜偵偼寣媴嵶朎偺傕偲偵側傞姴嵶朎乮stem cells乯偑懚嵼偟丄嵶朎暘楐偵傛偭偰忢偵悢傪憹傗偟丄寣媴嵶朎傪嫙媼偟偰偄傞丅偦偺偨傔丄嫮偄倃慄傪徠幩偡傞偲姴嵶朎偼巰柵偟偰偟傑偄丄屄懱偼巰偵偄偨傞丅
丂姴嵶朎偼暘楐偟偰摨偠姴嵶朎傪嶌傞偲偲傕偵丄嫟捠慜嬱嵶朎偲側傝丄偝傜偵暘楐傪孞傝曉偟偰偦傟偧傟偺嵶朎偺慜嬱嵶朎傪宱偰丄忋偵弎傋偨嵶朎傊偲暘壔偡傞丅
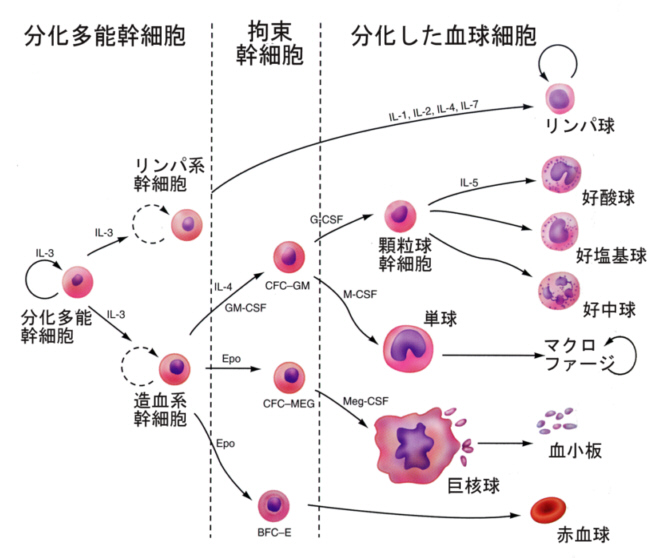
丂偦傟偧傟偺寣媴嵶朎傊暘壔偡傞偵偼丄暘壔傪懀偡暔幙偑摥偒偐偗傞丅愒寣媴傊偺暘壔傪懀偡僄儕僗儘億僄僠儞傕偦偺堦偮偱偁傞丅偙偺暘巕偼暘巕検51000偺僞儞僷僋幙偱丄恡憻偐傜暘斿偝傟傞丅抁偄帪娫偱崅偄嶳偵搊傞偲崅嶳昦偵側傞偑丄偙傟偼愒寣媴偺悢偑敄偄巁慺擹搙偵懳墳偱偒側偔側傞偐傜偱偁傞丅彊乆偵姷傜偟側偑傜搊傟偽丄偦偺娫偵僄儕僗儘億僄僠儞偑暘斿偝傟丄愒寣媴偺悢偑憹偊偰丄崅嶳昦偵側傞偙偲偼側偄丅儅儔僜儞偺崅抧僩儗乕僯儞僌傕偙傟傪墳梡偟偰偄傞偺偱偁傞丅
丂偦偺懠偺寣媴嵶朎傊偺暘壔傕丄暘壔懀恑場巕偑偼偨傜偄偰偄傞偙偲偑傢偐偭偰偄傞丅
丂偙傟傜偺嵶朎孮偺偆偪丄愒寣媴偑巁慺偺塣斃丄寣彫斅偑寣塼嬅屌偵偼偨傜偒丄懡偔偺庬椶傪娷傓敀寣媴偑偙傟偐傜弎傋傞惗懱杊屼偵怺偔娭學偟偰偄傞丅丂 丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂
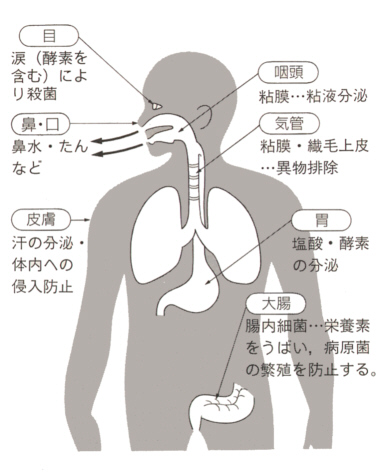
丂変乆偑廧傫偱偄傞娐嫬偼奜揋偱偁傆傟偰偄傞丅僂僀儖僗丄嵶嬠丄尨惗摦暔側偳偺旝惗暔偱昦婥偺尨場偲側傞昦尨懱乮pathogens乯偑忢偵懱撪傊偺怤擖偺婡夛傪偆偐偑偭偰偄傞丅懱偺杊塹婡擻偑掆巭偟偨傜丄偡偖偵巰傫偱偟傑偆丅
丂偙傟傜偺昦尨懱偼丄嬻婥偲偲傕偵屇媧婍偐傜丄怘傋暔偲偲傕偵徚壔婍偐傜丄偁傞偄偼彎岥傪捠偭偰懱昞偐傜怤擖偡傞丅偦偙偱丄奜揋偐傜恎傪庣傞偨傔偵偼丄侾乯偙傟傜偺応強偐傜堎暔偑擖傜側偄傛偆偵僶儕傾乕傪愝偗傞偙偲丄俀乯堎暔偑僶儕傾乕傪挻偊偰怤擖偟偨傜偡偽傗偔尒偮偗偰懳張偡傞偙偲丄偑昁梫偵側傞丅
丂恖娫偺旂晢偼昦尨懱偺怤擖傪杊偖嫮屌側僶儕傾乕偲側偭偰偄傞丅彎岥偑柍偗傟偽傆偮偆偺昦尨懱偼怤擖偡傞偙偲偼偱偒側偄丅傑偨丄旂晢偺昞柺傊娋態偐傜娋偑丄旂帀態偐傜暘斿暔偑嫙媼偝傟傞丅偙傟傜偺暘斿暔偵偼嶦嬠嶌梡偑偁傞丅
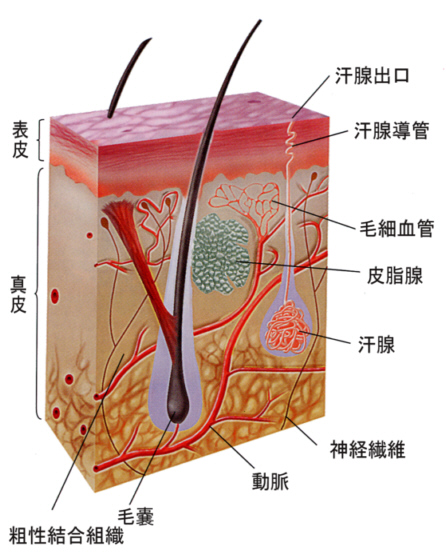
丂婥娗偺昞柺偼擲塼偱偍偍傢傟丄昦尨懱偼偙偙偱曔懆偝傟偰婷怘偝傟傞丅堓偵擖偭偨昦尨懱偼堓塼偺嫮椡側墫巁偲峺慺偵傛偭偰攋夡偝傟傞丅
丂偝傜偵僶儕傾乕傪撍攋偟偰懱撪傊怤擖偟偨昦尨懱偼丄儅僋儘僼傽乕僕偵傛偭偰婷怘偝傟傞丅忋偵堎暔偲彂偄偨偑丄惗懱偼帺屓偲旕帺屓乮self and notself乯傪抦偭偰偄偰丄偙傟傪幆暿偟側偗傟偽側傜側偄丅儅僋儘僼傽乕僕偼丄旕帺屓傪抦偭偰偄傞偙偲偵側傞丅
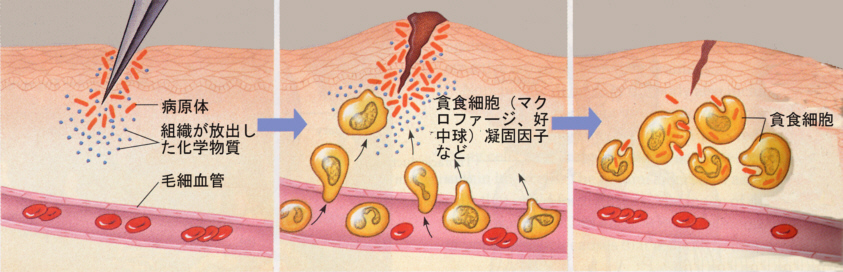
儅僋儘僼傽乕僕偑嵶嬠傪婷怘偡傞偲偙傠乮Window
Media Player 500k乯
丂丂http://www.cellsalive.com/傛傝
丂偙傟傑偱弎傋偨婡峔偼丄旕摿堎揑側杊塹婡峔偱偁傞丅柍愐捙摦暔偺懡偔偼丄偙偺旕摿堎揑側杊塹婡峔偱奜揋偐傜帺屓傪杊屼偟偰偄傞丅
丂愐捙摦暔偱偼丄偝傜偵摿堎揑側杊塹婡峔偑敪払偡傞丅偦傟偑柶塽婡峔偱偁傞丅柶塽婡峔偵偼侾丏偱弎傋偨儕儞僷媴偑廳梫側栶妱傪壥偨偡丅
丂柶塽偲偄偆尰徾偼丄宱尡揑偵屆偔偐傜抦傜傟偰偄偨丅揱愼昦偵偐偐偭偰帯桙偡傞偲丄偦偺揱愼昦偵偼姶愼偟偵偔偔側傝丄偐偐偭偰傕寉偔偡傓偲偄偆偙偲偑丄屆戙僊儕僔儍帪戙偵婰嵹偝傟偰偄傞偐傜偱偁傞丅
丂僕僃儞僫乕偼丄媿摋乮揤慠摋偵帡偨僂僔偺寉偄昦婥乯偵姶愼偟偨偙偲偺偁傞擕嶏傝偼丄恖娫偺揤慠摋(摋釋)偵偼偐偐傜側偄偲偄偆偙偲偵拝栚偟丄媿摋偺悈醰偐傜撪梕塼傪嵦庢偟偰丄彮擭偺榬偵愙庬偟偨丅彮擭偼媿摋偵姶愼偟偨偑丄揤慠摋傪愙庬偟偰傕敪昦偟側偄偙偲傪妋擣偟丄媿摋偵傛偭偰恖摋偵懳偡傞柶塽偑偱偒傞偙偲傪幚徹偟偨丅18悽婭偺廔傢傝偵嬤偄崰偺偙偲偱偁傞丅
丂偙偆偟偰柶塽偲偄偆尰徾偑偁傞偙偲偼傢偐偭偨偑丄偦偺儊僇僯僘儉偵偮偄偰柧傜偐偵側傝巒傔傞偺偼丄20悽婭偺屻敿偵側偭偰偐傜偱偁傞丅
1)柶塽偵偼儕儞僷媴偑娭梌偡傞
丂柶塽偵偼丄忋偱弎傋偨寣媴嵶朎偺偆偪丄儕儞僷媴偑娭梌偡傞偙偲偼師偺傛偆側幚尡偱妋偐傔傞偙偲偑偱偒傞丅
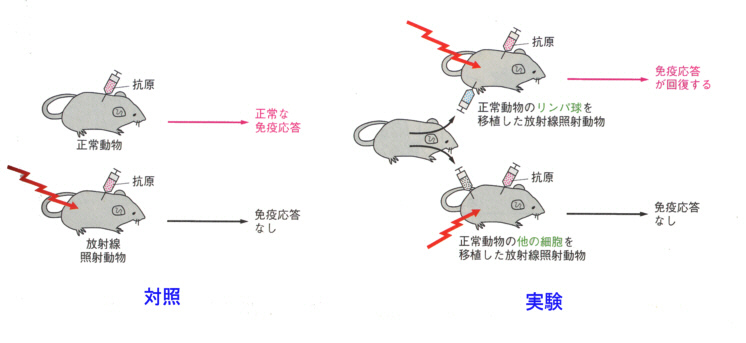
丂仠惓忢側儅僂僗偵丄峈尨傪拲幩傪偡傞偲柶塽墳摎偑婲偙傞丅
丂仠儅僂僗偵倃慄傪徠幩偟丄儕儞僷媴傪娷傓敀寣媴傪嶦偟偰偟傑偆偲丄峈尨傪拲幩偟偰傕柶塽墳摎偼偍偙傜側偔側傞丅
丂仠倃慄傪徠幩偟偨儅僂僗偵丄摨暊偺儅僂僗偐傜儕儞僷媴傪慖傃弌偟堏怉偡傞偲丄柶塽墳摎偼夞暅偡傞丅儕儞僷媴埲奜偺嵶朎偱偼懯栚偱偁傞丅
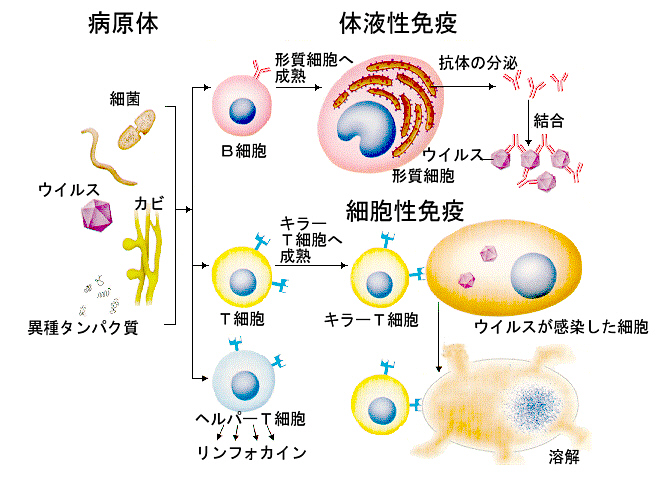
丂偡偱偵弎傋偨偑丄儕儞僷媴偵偼俀庬椶偁傞偙偲偑傢偐偭偰偄傞丅偙偙偵弎傋偨峈尨偵懳偡傞峈懱傪嶌偭偰偍偙側偆柶塽墳摎乮antibody-mediated immunity乯偵娭學偡傞偺偼丄俛嵶朎偱偁傞偙偲偑柧傜偐偵側偭偰偄傞丅
丂俀庬椶偁傞柶塽墳摎偺偆偪丄傕偆侾庬椶偼嵶朎惈柶塽乮cell-mediated immunity乯偱偁傝丄嵶朎惈柶塽偺傎偆偼俿嵶朎偑扴摉偟偰偄傞丅
俀乯儕儞僷宯婍姱
丂儕儞僷媴偺嶻惗傪娷傔丄柶塽偵娭梌偡傞偺偼儕儞僷宯婍姱偱偁傞丅儕儞僷媴偺偍偍傕偲偼丄偡偱偵弎傋偨傛偆偵崪悜偱嶌傜傟傞偑丄儕儞僷媴偑惉弉偟丄婡擻偡傞偨傔偵偼丄偙偺懠丄懡偔偺婍姱偑昁梫偲側傞丅

丂歁擕椶偱偼嫻態乮thymus乯傪惗傑傟偨偰偺摦暔偱彍嫀偡傞偲丄峈懱嶻惗傊偺塭嬁偼彮側偄偑丄嵶朎惈柶塽偑懝側傢傟傞偙偲偑柧傜偐偵側偭偨丅
丂捁偱偼僸儓僐偺偆偪偵僼傽僽儕僉僂僗擷乮bursa of Fabricius乯傪彍嫀偡傞偲丄嫻態彍嫀偲偼媡偵丄嵶朎惈柶塽偼懝側傢傟側偄偑丄峈懱嶻惗偑掅壓偡傞偙偲偑帵偝傟偨丅
丂偙偺傛偆偵儕儞僷嵶朎傊暘壔偡傞嫟捠慜嬱嵶朎偼丄崪悜傪棧傟丄偦傟偧傟偺婍姱傊堏峴偟偨偺偪暘壔偡傞丅俿嵶朎丄俛嵶朎偲偄偆柤偼丄偦傟偧傟偺憻婍偺摢暥帤傪庢偭偰偮偗傜傟偨丅偨偩偟歁擕椶偵偼僼傽僽儕僉僂僗擷偑柍偔丄俛嵶朎偼崪悜乮bone marrow乯偱暘壔丒惉弉偡傞丅
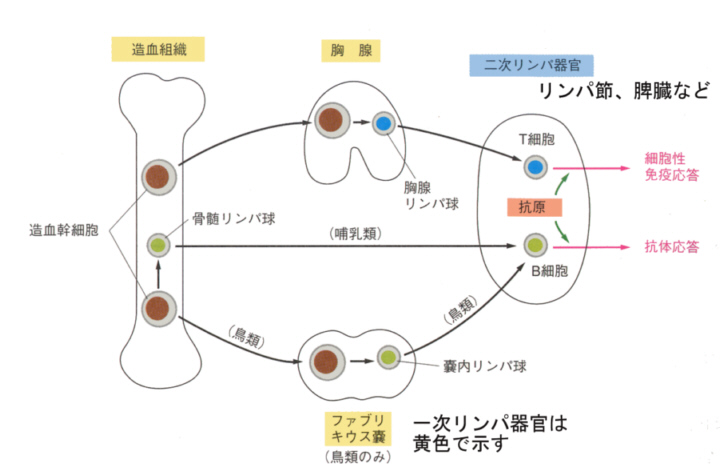
丂惉弉偟偨儕儞僷媴偼丄擇師儕儞僷婍姱乮枛徑儕儞僷婍姱乯傊摓払偟丄偦偙傊忢挀偟偐偮弞娐偡傞丅
丂妶惈壔偟偰偄側偄俿嵶朎丄俛嵶朎傪宍懺揑偵嬫暿偡傞偙偲偼丄揹巕尠旝嬀偱傕偱偒側偄丅俛嵶朎偼峈懱傪嶌傞傛偆偵側傞偲丄慹柺彫朎懱偑敪払偟偨宍幙嵶朎乮plasma cell乯偵側傞丅
丂偦傟偱偼丄堎暔偱偁傞峈尨乮antigen, antibody generator乯偼偳偺傛偆偵偟偰柶塽墳摎傪堷偒婲偙偡偺偩傠偆偐丅峈尨偑懱撪偵怤擖偡傞偲丄偙傟偵摿堎揑側峈懱偑嶌傜傟丄峈尨偲寢崌偟偰撆惈傪庛傔偨傝丄懱撪偐傜彍嫀偝傟傗偡偔偟偨傝偡傞丅偙偺傛偆側斀墳傪柶塽墳摎偲屇傇丅
丂堎暔偲側傝偆傞暔幙偼悢尷傝側偔偁傞偺偵丄偦傟偵懳墳偟偰摿堎揑側峈懱偑嶌傜傟傞偺偼偳偺傛偆側婡峔偵傛偭偰偄傞偺偩傠偆偐丅
丂偼偠傔偼丄摿掕偺峈尨偺巋寖偵傛偭偰摿堎揑偵斀墳偡傞峈懱偑屻揤揑偵嶌傜傟傞偲偄偆峫偊偑堦斒揑偩偭偨乮巌椷愢丄拻宆愢乯丅
丂1957擭偵僶乕僱僢僩偼僋儘乕儞慖戰愢乮clonal selection theory乯傪採弌偟偰丄偙偺峫偊傪暍偟偨丅僋儘乕儞慖戰愢偵傛傟偽丄偁傜備傞峈尨偵懳偟偰丄偙傟偵摿堎揑偵斀墳偡傞峈懱偑丄傕偲傕偲愭揤揑偵俛嵶朎偺僋儘乕儞乮扨堦嵶朎偵桼棃偡傞堚揱揑偵慡偔摨堦側嵶朎孮乯偲偟偰梡堄偝傟偰偄偰丄峈尨偑惗懱撪偵怤擖偡傞偲丄偙偺懡悢偺僋儘乕儞偺拞偐傜摿掕偺僋儘乕儞偑慖戰偝傟丄偦偺峈尨偲斀墳偟偰媫寖偵憹怋偟丄峈懱傪嶌傞宍幙嵶朎偵側傞偲偄偆峫偊偱偁傞丅
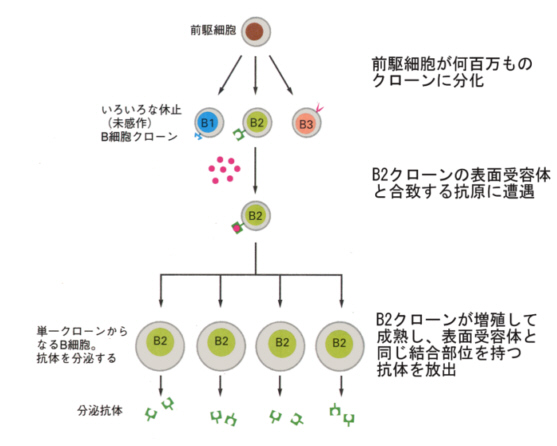
丂尰嵼偱傕偙偺峫偊偼婎杮揑偵惓偟偄偲峫偊傜傟偰偄傞丅俛嵶朎偵梡堄偝傟偰偄傞偺偼嵶朎昞柺偺庴梕懱僞儞僷僋幙偱丄峈尨偑偙傟偲寢崌偡傞偲偙偺嵶朎傪妶惈壔偟偰丄憹怋偲惉弉傪懀恑偟丄庴梕懱偲摨偠寢崌晹埵傪帩偮峈懱傪惗嶻偡傞傛偆偵側傞丅
丂僋儘乕儞慖戰愢偑惓偟偄偙偲偑丄師偺傛偆側幚尡乮壓偺幚尡俀乯偐傜帵嵈偝傟傞丅
丂仠惓忢儅僂僗偐傜儕儞僷媴傪廤傔傞丅
丂仠師偵丄偁傞摿掕偺峈尨乮峈尨俙偲偡傞乯傪價乕僘偵怉偊晅偗偰僇儔儉偵媗傔丄偙偙傊儕儞僷媴傪捠偡丅
丂仠偡傞偲丄昞柺偵峈尨俙庴梕懱傪傕偭偨儕儞僷媴偼曔懆偝傟偰丄僇儔儉偐傜偼棳傟弌偰偙側偄丅
丂仠倃慄傪徠幩偟偰柶塽墳摎擻傪幐偭偨儅僂僗偵丄僇儔儉傪捠偟偨儕儞僷媴傪堏怉偡傞丅
丂仠堏怉偝傟偨儅僂僗偼丄峈尨俙偵懳偟偰偼柶塽墳摎傪帵偝側偄偑丄偦偺懠偺峈尨偵懳偟偰偼柶塽墳摎傪帵偡丅
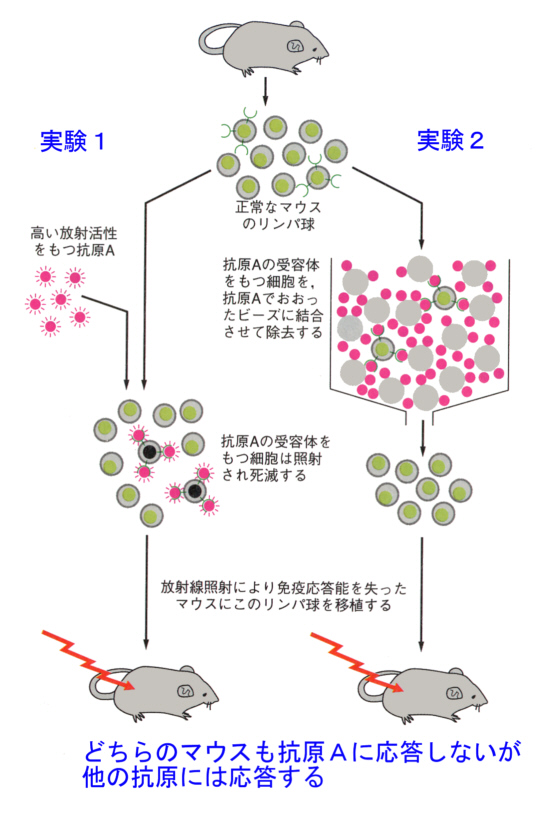
丂偙偺幚尡偼丄偁傜偐偠傔惓忢儅僂僗偺儕儞僷媴廤抍偺拞偵丄峈尨俙偵懳偡傞峈懱偑昞柺庴梕懱偲偟偰懚嵼偟偰偄傞偙偲傪帵偟偰偄傞丅
丂偙傟傑偱峈尨偲偄偆尵梩傪偁傑傝柧妋偵偟側偄偱巊偭偰偒偨丅偙偙偱丄傕偆彮偟峈尨偲偼壗偐傪柧妋偵偟偰偍偙偆丅
丂峈尨偲偄偆尵梩偼丄峈尨峈懱斀墳丒柶塽墳摎傪婲偙偡偙偲偑偱偒傞暔幙偺憤徧偲偟偰梡偄傜傟傞丅帺慠奅偱偼丄暘巕検偑1000埲忋偺僞儞僷僋幙丄懡摐椶丄偦傟傜偺暋崌懱丄帀幙偲偺暋崌懱側偳偑峈尨偲側傝偆傞丅
丂偟偐偟側偑傜丄峈尨偲偟偰峈懱偵擣幆偝傟傞偺偼丄忋偵弎傋偨暘巕慡懱偱偼側偔丄偦偺昞柺偺摿掕偺晹埵偱偁傞丅偦偙偱峈懱偵擣幆偝傟傞晹埵傪丄峈尨寛掕婎乮antigenic determinant乯偁傞偄偼僄僺僩乕僾乮epitope乯偲屇傇丅暘巕検偑戝偒偄儅僋儘儌儗僉儏乕儖偼丄偦偺昞柺偵暋悢偺峈尨寛掕婎傪帩偭偰偄傞偺偑傆偮偆偱偁傞丅
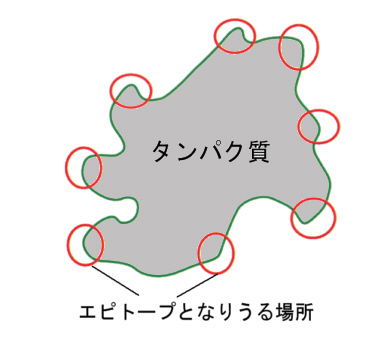
丂堦曽丄峈懱偲寢崌偼偱偒傞偑丄偦傟帺恎偱偼柶塽墳摎傪堷偒婲偙偡擻椡偑柍偄暔幙傪僴僾僥儞乮hapten乯偲屇傇丅
丂儔儞僪僔儏僞僀僫乕偼朏崄懓壔崌暔乮桳柤側偺偼僕僯僩儘僼僃僲乕儖乯傗摐椶側偳偺杮棃峈尨偲側傝摼側偄掅暘巕暔幙傪僞儞僷僋幙偵寢崌偝偣偨傕偺傪峈尨偲偟偰梡偄傞偲丄慜幰偺掅暘巕暔幙偵懳偡傞峈懱偑丄屻幰偺僞儞僷僋幙偵懳偡傞峈懱偲偼撈棫偵嶌傜傟傞偙偲傪柧傜偐偵偟偨丅偙偺偙偲偐傜丄儅僋儘儌儗僉儏乕儖偱傕丄峈懱偲寢崌偡傞偺偼峈尨暘巕慡懱偱偼側偔丄摿掕偺峈尨寛掕婎偱偁傞偙偲偑妋掕偟偨偺偱偁傞丅
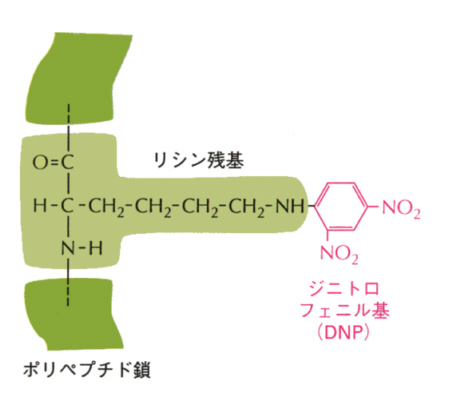
丂偟偨偑偭偰丄柶塽墳摎傪婲偙偡偙偲丄偡側傢偪峈懱偺惗嶻傪巋寖偡傞偙偲偲丄峈懱偲峈尨偑寢崌偡傞偙偲偲偼丄暿偺夁掱偲偟偰愗傝曻偣傞偙偲偵側傞丅偦偺偨傔丄in vitro偱峈尨峈懱斀墳傪挷傋傞偙偲偑偱偒傞偺偱偁傞丅
丂尰嵼偱偼丄掅暘巕偺偨傔杮棃峈懱傪嶌傜偣傞擻椡偺側偄惗暔妶惈暘巕傪丄媿寣惔傾儖僽儈儞乮bovine serum albumin, BSA乯側偳偵寢崌偟偰峈尨偲偟丄僂僒僊偵峈懱傪嶌傜偣丄偱偒偨峈懱傪棙梡偟偰儔僕僆僀儉僲傾僢僙僀乮radioimmunoassay乯傗柶塽慻怐壔妛朄乮immunohistochemistry乯側偳偵惙傫偵棙梡偝傟偰偄傞丅
丂儅僋儘儌儗僉儏乕儖偵偼丄忋偵弎傋偨傛偆偵暘巕昞柺偵峈尨寛掕婎偑暋悢偁傞丅偦偺偨傔丄偙偺儅僋儘儌儗僉儏乕儖傪峈尨偲偟偰梡偄傞偲丄偦傟偧傟偺峈尨寛掕婎偵懳偟偰撈棫偵摿堎揑側峈懱偑偱偒傞丅偙傟傪懡僋儘乕儞乮poly clonal乯偺柶塽墳摎偲偄偆丅
丂偟偨偑偭偰丄扨僋儘乕儞乮monoclonal乯峈懱偲偄偆尵梩偼丄扨堦偺峈尨寛掕婎偩偗傪擣幆偡傞峈懱傪偄偆丅
丂傕偪傠傫丄偙偺傛偆側峈懱偼帺慠柶塽偱偼摼傜傟側偄丅摦暔傪偁傞峈尨偱柶塽姶嶌傪偡傞偲丄峈尨偺懡悢偺峈尨寛掕婎偵懳偡傞峈懱偑嶌傜傟傞偐傜偱偁傞丅
丂偟偐偟側偑傜丄忋弎偟偨傛偆偵丄侾庬椶偺峈懱偼侾屄偺峈懱嶻惗嵶朎偐傜偟偐嶌傜傟側偄丅偦偙偱丄峈懱嶻惗嵶朎傪堦屄偯偮僶儔僶儔偵偟偰丄偦傟偧傟傪崪悜庮嵶朎乮儈僄儘乕儅嵶朎乯偲梈崌偝偣偰僴僀僽儕僪乕儅傪嶌傞丅偙偺僴僀僽儖僪乕儅偼摿暿側攟梴塼拞偱憹怋偟丄偐偮峈懱傪嶻惗偡傞丅
丂偦偙偱丄攟梴塼拞偺嵶朎傪96寠偺僂僄儖乮偔傏傒乯傪帩偭偨僾儗乕僩偵暘拲偟丄偳偺僂僄儖拞偵栚揑偲偡傞峈尨偵斀墳偡傞峈懱偑嶌傜傟偨偐傪挷傋傞丅
丂奩摉偡傞僂僄儖撪偺僴僀僽儕僪乕儅傪憹傗偟偰丄傑偨僾儗乕僩偵暘拲偟丄偍側偠憖嶌傪孞傝曉偡丅
丂偙偺憖嶌傪孞傝曉偣偽丄偮偄偵偼偨偭偨侾屄偺俛嵶朎桼棃偺僋儘乕儞傪摼傞偙偲偑偱偒傞丅
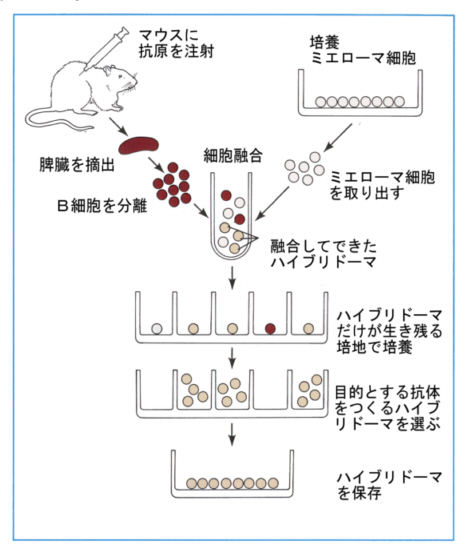
扨僋儘乕儞峈懱偺嶌傝曽
丂偙偺傛偆偵偟偰摼傜傟偨扨僋儘乕儞峈懱偼丄摿掕偺丄偟偐傕扨堦偺峈尨寛掕婎偲偺傒寢崌偡傞偺偱丄柶塽慻怐壔妛朄偺嫮椡側晲婍偲側傞偟丄帯椕傊偺墳梡傕婜懸偱偒傞丅
丂偝傜偵僴僀僽儕僪乕儅偼搥寢偟偰曐懚偱偒傞偺偱丄昁梫偵墳偠偰曐懚偟偰偍偄偨傕偺傪庢傝弌偟偰棙梡偱偒傞丅
丂峈懱偑堎暔傪尒暘偗傞偺偳偺傛偆側婡峔偵傛傞偺偩傠偆偐丅堦懱丄峈懱偼偳傫側暘巕偱丄偳偺傛偆側峔憿傪偟偰偄傞偺偩傠偆偐丅
丂寣惔拞偺僞儞僷僋幙傪揹婥塲摦偱暘棧偡傞偲丄師偺傛偆側塲摦僷僞乕儞偑摼傜傟傞丅峈懱偼 兞僌儘僽儕儞暘夋偍傛傃兝僌儘僽儕儞暘夋偺堦晹偵尒偄偩偝傟丄柶塽僌儘僽儕儞乮immunoglobulin, Ig乯偲屇偽傟傞丅
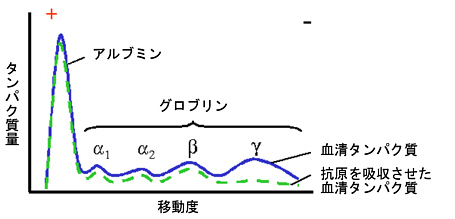
丂Ig偺側偐偱傕偭偲傕懡偄偺偼IgG乮屻弎乯偱丄慡懱偺75亾傪愯傔傞丅惓忢摦暔偺Ig偼晄嬒堦側偺偱丄偦偺扨棧偲峔憿偺悇掕偼丄峈懱偺懡條惈傪峫偊傞偲崲擄側偙偲偼憐憸偱偒傞偩傠偆丅
丂懡敪惈崪悜庮偲偄偆昦婥偑偁傝丄偙傟偼宍幙嵶朎偺僈儞偱偁傞丅傆偮偆丄侾屄懱撪偺崪悜庮嵶朎偼侾屄偺嵶朎偑僈儞壔偟偰憹怋偡傞偺偱丄侾屄懱撪偺偳偺崪悜庮嵶朎傕摨偠柶塽僌儘僽儕儞傪嶌偭偰曻弌偡傞乮昦婥偑嶌偭偨儌僲僋儘儞峈懱乯丅偦偺偨傔丄忋偺揹婥塲摦僷僞乕儞傪崪悜庮姵幰偱挷傋傞偲丄兞暘夋偺偲偙傠偵侾杮塻偄僺乕僋傪専弌偱偒傞丅寣惔拞偺丄偙偺嬒堦偺僞儞僷僋傪崪悜庮僞儞僷僋偲尵偄丄偙傟傪梡偄偰丄柶塽僌儘僽儕儞僞儞僷僋偺堦師峔憿偺夝愅偑峴傢傟偨丅
丂偄傠偄傠側尋媶偐傜師偺偙偲偑傢偐偭偨丅
丂丂仠峈尨偲寢崌偡傞晹埵偼峈懱侾暘巕拞偵俀僇強偁傞乮俀壙乯
丂丂仠俽-俽寢崌偲旕嫟桳寢崌傪奜偡偲丄俀杮偯偮摨偠係杮偺億儕儁僾僠僪嵔偵側傞
丂丂丂丂暘巕検偺戝偒側曽傪俫嵔乮廳嵔heavy chain丄傾儈僲巁440乯丄彫偝側曽傪俴嵔乮寉嵔light
chain丄傾儈僲巁220乯

丂丂丂丂丂丂丂丂
丂丂仠俫嵔丄俴嵔偲傕丄俶抂懁偼懡條惈偑戝偒偔丄俠抂懁偼傎傏堦掕偱偁傞
丂丂丂丂俶抂懁傪壜曄椞堟乮variable region乯偲尵偄丄懕偔俠抂懁傪掕忢椞堟乮constant
region乯偲尵偆丅
丂丂丂丂壜曄椞堟偼偳偪傜傕傾儈僲巁110偱丄掕忢椞堟偼丄俴嵔偱傾儈僲巁110丄俫嵔偱330偐傜側傞丅
丂丂仠僞儞僷僋暘夝峺慺傌僾僔儞偱張棟偡傞偲丄俀壙偺僼儔僌儊儞僩偲丄懡悢偺抐曅偵側傞
丂丂仠僞儞僷僋暘夝峺慺僷僷僀儞偱張棟偡傞偲丄侾壙偺僼儔僌儊儞僩俀屄偲丄峈懱壙偺側偄僼儔僌儊儞僩偵側傞丅
丂丂丂丂峈尨寢崌僼儔僌儊儞僩乮antigen
binding fragment, Fab乯
丂丂丂丂寢徎壜擻僼儔僌儊儞僩乮crystallizable
fragment, Fc乯
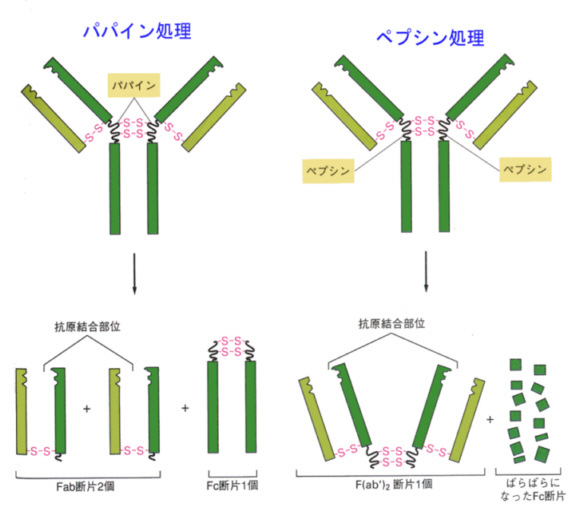
丂丂仠僞儞僷僋幙暘夝峺慺偺寢壥偑帵偟偰偄傞傛偆偵丄俫嵔偺側偐傎偳偵愗傟傗偡偄晹暘偑偁傞
丂偙偺傛偆側惈幙傪愢柧偡傞峈懱暘巕偺儌僨儖偲偟偰丄師偺傛偆側傕偺偑峫偊傜傟偨丅
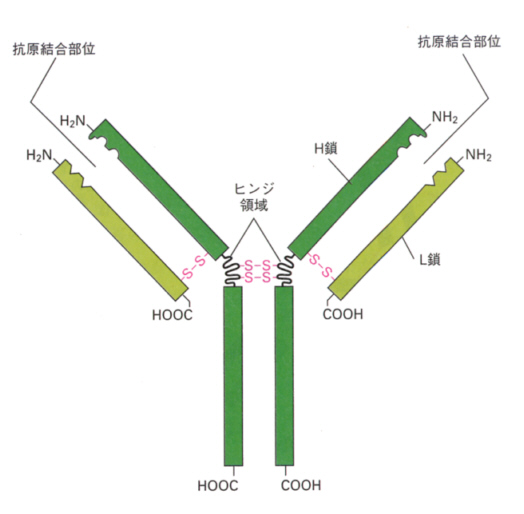
丂忋偺婰弎偐傜丄傾儈僲巁110屄偑侾偮偺扨埵乮僪儊僀儞乯傪嶌偭偰偄傞偺偑傢偐傞偲巚偆偑丄偦傟偧傟偺僪儊僀儞偵偼侾屄偺俽-俽寢崌偑懚嵼偡傞丅偟偨偑偭偰丄峈懱偼忋偺塃懁偺恾偺傛偆偵丄12屄偺僪儊僀儞偺孞傝曉偟偱偁傞丅僪儊僀儞偺娫偺憡摨惈偼崅偄丅偦傟偧傟偺僪儊僀儞偵丄堦偮偺俽-俽寢崌偑偁傞偺偱丄幚嵺偺峈懱偼忋偺傛偆側朹忬偺峔憿偱偼側偔丄師偺傛偆側峔憿偺曽偑幚嵺偵嬤偄丅
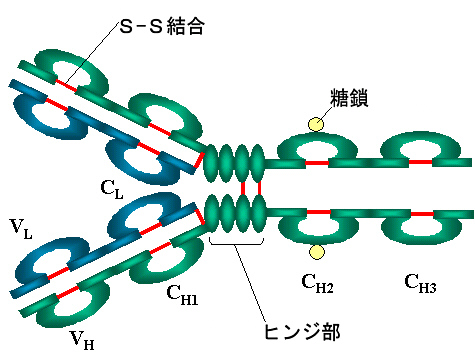
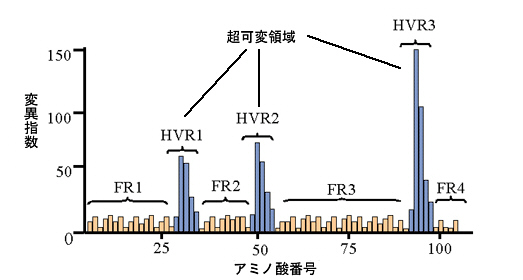
丂俫嵔丄俴嵔偲傕丄壜曄晹偺傾儈僲巁110屄偺偆偪丄偲偔偵傾儈僲巁偺曄堎偑崅偄晹暘偑俁僇強偁傞丅偙偺晹埵傪挻壜曄晹乮hypervariable region乯偲偄偆丅
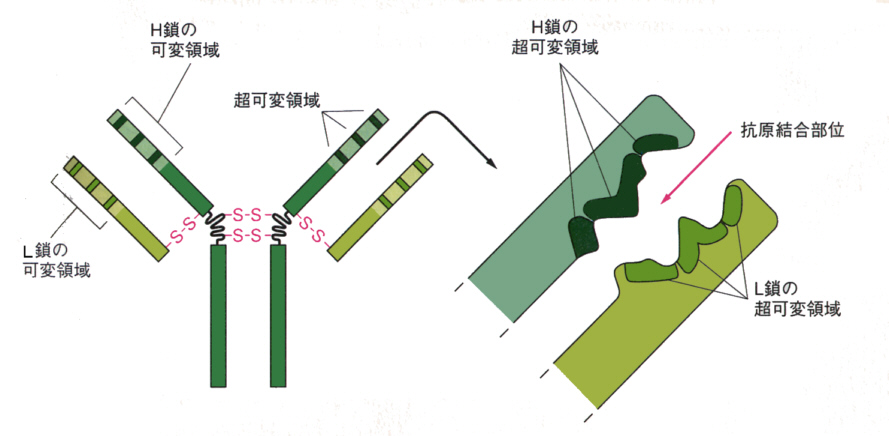
丂挻壜曄晹偼俶抂偐傜悢偊偰丄偍傛偦27-30斣栚丄55-65斣栚丄102-107斣栚偺傾儈僲巁偱尠挊偱偁傞丅偙傟傜偺俁偮偼偍屳偄偵棧傟偰偄傞偑丄 俽-俽寢崌傪傕偭偨僪儊僀儞峔憿偱偼嬤婑偭偰偄傞偙偲偑傢偐偭偨丅
丂俫嵔偲俴嵔偑廳崌偡傞偙偲偵傛偭偰丄俁偮偯偮偺挻壜曄椞堟偼屳偄偵婑傝崌偄丄億働僢僩傪宍惉偡傞丅偙偺孍傒偑峈尨擣幆寢崌晹埵偵側傞偺偱偁傞丅師恾偼丄倃慄夞愜偵傛傞僨乕僞偐傜偮偔偭偨峈懱暘巕偺僐儞僺儏乕僞僌儔僼傿僢僋偵傛傞儕儃儞儌僨儖偺恾偱偁傞丅
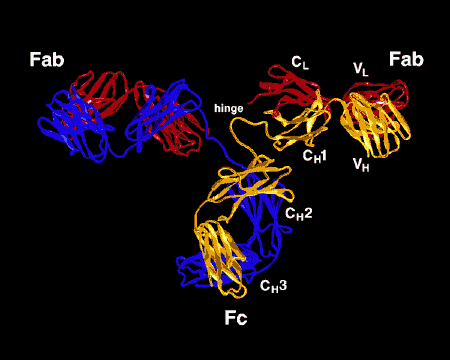
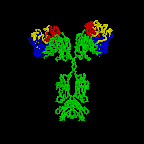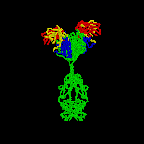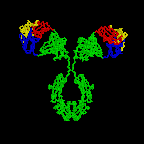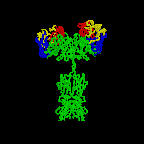
丂偙傟傑偱庡偲偟偰IgG偵偮偄偰弎傋偰偒偨偑丄峈懱偵偼偙偺懠偵IgM丄IgD丄IgA丄IgE偑偁傞丅偙偺偪偑偄偼俫嵔偺堘偄偵傛傞丅俴嵔偱偼內偲兩偩偗偩偑丄俫嵔偵偼兪丄兟丄兞丄兛丄兠偑偁傞丅
丂俴嵔偲廳崌偟偰偄側偄俫嵔偺掕忢晹偺惈幙偵傛偭偰丄庴梕懱偲偺寢崌偺堘偄丄曗懱妶惈壔偺堘偄偑惗偢傞丅
| 丂 | IgM | IgD | IgG | IgA | IgE |
| 俫嵔 | 兪 | 兟 | 兞 | 兛 | 兠 |
| 俴嵔 | 偡傋偰內偐兩 | ||||
| 擇検懱傪侾偲偟偨扨埵悢 | 俆 | 侾 | 侾 | 侾偐俀 | 侾 |
| 慡Ig拞偺妱崌 | 10 | <1 | 75 | 15 | <1 |
| 敿尭婜乮擔乯 | 俆 | 俁 | 25 | 俀 | 俇 |
| 曗懱妶惈壔 | +++ | 亅 | ++ | 亅 | 亅 |
| 婷怘嵶朎偲偺寢崌 | 亅 | 亅 | + | 亅 | 亅 |
| 旍枮嵶朎偲偺寢崌 | 亅 | 亅 | 亅 | 亅 | + |
丂IgM 偼丄柶塽斀墳偺嵟弶偵弌尰偡傞峈懱偱偁傞丅 IgG偼師偵尰傢傟丄曗懱宯傪妶惈壔偟偨傝丄儅僋儘僼傽乕僕偵寢崌偟偰婷怘偝傟傗偡偔偡傞丅 IgA偼寣拞偵傕懚嵼偡傞偑丄奜暘斿塼拞偺庡梫側柶塽僌儘僽儕儞偱丄擲枌昞柺偺姶愼杊屼偵栶棫偭偰偄傞丅 IgE偼庡偵挵娗傗婥娗偺儕儞僷慻怐偱嶌傜傟丄傾儗儖僊乕偵娭梌偡傞丅
娭楢偡傞僒僀僩偲儕儞僋乮偙偺儁乕僕傊栠傞偲偒偼僽儔僂僓乕偺栠傞傪慖傫偱偔偩偝偄乯
丂丂http://www.med.sc.edu:85/mayer/IgStruct2000.htm
丂
![]() 丂偙偺復偺倫倓倖僼傽僀儖傪僟僂儞儘乕僪偡傞偵偼秱虄A僀僐儞傪塃僋儕僢僋偟偰偔偩偝偄丅
丂偙偺復偺倫倓倖僼傽僀儖傪僟僂儞儘乕僪偡傞偵偼秱虄A僀僐儞傪塃僋儕僢僋偟偰偔偩偝偄丅