権田 幸祐
- 東北大学 大学院医学系研究科
- 教授
- 専門分野 : 医工学

連絡先
- 〒980-8574
- 宮城県仙台市青葉区星陵町1-1
- gonda@med.tohoku.ac.jp
がんリンパ行性転移の分子機構解明に基づく新治療法創発
「蛍光デバイスと生体ナノイメージングの融合により、がん転移の分子反応パラメータの解明、高感度微小がん検出トレーサー開発、薬剤送達の分子科学的理解と創発を推進する。」
基盤研究
リンパ行性転移メガにズム解明

リンパ節内転移がん細胞の好感度検出法開発
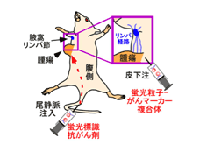
がん転移抑制分子送達システムの創製
∴ 基盤研究を基に進める研究課題を以下に示す。
本研究課題
生体ナノイメージング技術開発
高時間分解能(A01班:樋口)と生体振動抑制技術(A01班:福田)との技術の連携・融合を図る。
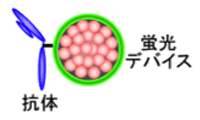
蛍光分子デバイスと生体ナノイメージングの統合
蛍光分子デバイス(A01班:由井)や蛍光性ナノ粒子(A02班:石原)と生体イメージングの融合を図り、がんメカニズムや抗がん剤送達システムの分子反応の可視化を行う。
細胞と生体組織データの連携
細胞場における分子反応やそれに基づく細胞動態データ(A02班:三宅、丸山、A03班:岩田、夏目)と生体データを連携させ、分子反応の普遍的概念構築を図る。
∴ 基盤技術と共同研究を踏まえ、以下の目標を掲げる。
期待される成果
- がん転移の入力情報(転移活性化因子の濃度・分布・受容体結合時間)と出力情報(がん細胞動態)の間の分子科学的理解が深まる。
- がん転移検出トレーサーの開発により、微小がん転移の発見確率が高まる。的確ながん診断は治療の選択性拡大と効率化を生むため、無駄な医療費削減に繋がる。
- 薬剤送達の分子科学的理解により、薬剤の効果増強と副作用減弱を導出できる。
主な論文
- K. Gonda, T. M. Watanabe, N. Ohuchi, H. Higuchi, In vivo nano-imaging of membrane dynamics in metastatic tumor cells using quantum dots, J. Biol. Chem., 285, 2750-2757 (2010).
- M. Hikage, K. Gonda, M. Takeda, T. Kamei, M. Kobayashi, M. Kumasaka, M. Watanabe, S. Satomi, N. Ohuchi, Nano-imaging of the lymph network structure with quantum dots, Nanotechnology, 21, 185103 (2010).
- Y. Hamada, K. Gonda, M. Takeda, A. Sato, M. Watanabe, T. Yambe, S. Satomi, N. Ohuchi, In vivo imaging of the molecular distribution of the VEGF receptor during angiogenesis in a mouse model of ischemia, Blood, 118, e93-e100, (2011).