幹細胞医学分野 2008-2009 研究内容 概要 生体を構築する多くの組織の恒常性維持において、幹細胞システムが大きな役割を果たしている。本研究分野では、幹細胞システムの動作原理の解明とその破綻によりおこる病態研究を中心として、生体組織の再生、老化、がん化の仕組みを理解し臨床に応用すべく研究を行っている。特に、マウスやヒトの皮膚の幹細胞システムをモデルとして、幹細胞およびニッチ細胞の同定、幹細胞周囲の微小環境(ニッチ)が幹細胞運命を制御する仕組みとその分子基盤の解明、幹細胞システムが様々なゲノム損傷ストレスや加齢に抗して幹細胞プールを保持し組織の恒常性を維持する仕組みの解明に取り組んでいる。幹細胞医学という新しい研究領域を開拓しながら、再生医療や抗老化戦略、がん根治療法へと応用することを目指している。 研究紹介幹細胞 西村 東京医科歯科大学 老化 がん 白髪 幹細胞医学分野 業績 西村栄美 Cell CellStemCell 1. 皮膚における組織幹細胞の同定 皮膚は、最大の臓器であり、他の多くの組織や臓器と同様、新陳代謝を行いながらその恒常性を維持している。日々なんら変化がないように見えても、表皮やその付属器において構成細胞が少しずつ入れ替わっており、表皮や毛包の幹細胞が細胞の供給源となっている。特に、毛包ではその再生と退縮を周期的に繰り返しながら構成細胞の新陳代謝が行われており、毛包内で毛に色素を供給している色素細胞も毛周期ごとに大部分の細胞が新しく入れ替わる。皮膚は、その外観から変化が容易に検出できる上、簡単にアクセスできる点で実験系としても大変優れている。特に、毛包においては幹細胞およびその居場所(ニッチ:生態的適所)を容易に可視化することもできる。私たちは、こういった利点を生かし、マウス成体皮膚における色素幹細胞を世界に先駆けて発見、同定している(Nishimura EK. et al., Nature, 2002.)(図)。さらに、毛包のない皮膚領域における幹細胞の同定などにも、現在取り組んでいる。これら皮膚の幹細胞システムを最大限に生かして、他のシステムでは知り得ていない幹細胞システムの動作原理を明らかにすべく研究を進めている。 2. 組織幹細胞の維持機構の解明 これまでの研究から、組織幹細胞の維持には、幹細胞自身に加えて、周囲の微小環境による制御が重要であることが複数の組織において明らかにされている。我々は、色素幹細胞の維持においては、色素細胞発生分化のマスター制御因子として知られるMITF転写因子および、その標的遺伝子であるBcl2が必須であり、その欠損により毛が白髪化することを既に明らかにしている (Nishimura EK. et al. Science 2005)。Bcl2とMitfのそれぞれが色素幹細胞維持のどのステップにおいて重要であるのか調べたところ、Bcl2欠損マウスにて詳細に解析したところ、発生をへてニッチに局在したメラノブラストが、色素幹細胞として休眠状態に入るその瞬間においてBcl2が生存に必須となることが判明した。幹細胞が休眠状態に入るタイミングを視覚的に捉えた初めての例であるといえる。さらに、加齢に伴いニッチにおいて色素幹細胞が“異所性に分化”する現象をはじめて発見し、これはMitf遺伝子の変異により有意に促進されることを示した。 次なる課題として、ニッチ由来の因子が色素幹細胞をいかにして維持するのかについて取り組んでいる。色素幹細胞システムにおいても、幹細胞の生態的適所であるニッチ(Niche)が色素幹細胞の維持に重要であり、色素幹細胞の運命を優勢に決定していることをこれまでに証明している(Nishimura EK. et al., Nature, 2002.)(図)。現在、機能的なニッチ細胞の同定と、ニッチ由来の因子の同定、さらに、いかにしてニッチ由来因子が色素幹細胞の運命を制御しているのか研究を進めている。  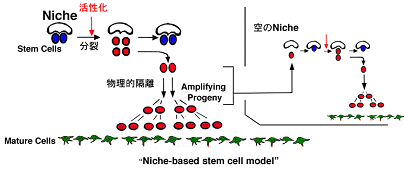 3. 白髪や脱毛などの老化形質の発現メカニズムの解明 加齢に伴い、多くの組織臓器で機能低下および器質的変化が見られるようになる。白髪は、最も身近な老化現象の一つでもある。我々は、加齢に伴ってマウスの髭毛包内で、色素幹細胞が異所性にニッチにおいてメラニン色素を持って樹状の形態をとるようになる(形態的には通常の分化に酷似する)ことを見いだし、これに次いで幹細胞の枯渇と白髪が起こることを見いだしている(Nishimura EK. et al. Science 2005)。さらに、ヒトの加齢に伴う生理的な白髪においても、同様の細胞が加齢に伴いニッチに現れ、未分化な色素細胞が枯渇してしまうこと、これについで白毛化が起こる。つまり、種をこえて色素幹細胞の維持不全により白髪がおこることがわかる。加齢に伴って、幹細胞が枯渇することによって老化形質を発現する例が実在することをはじめて明らかにしたことになる。 4. ゲノム損傷下における組織幹細胞の運命制御と組織老化形質の発現 加齢に伴う組織幹細胞の変化の実態はいったい何なのか? さらに加齢に伴ってなぜそのような変化がおこるのかについて、白髪をモデルとして研究を進めている。近年、遺伝性の早老症の原因遺伝子が明らかにされ、そのほとんどがゲノム損傷応答や修復に関わる遺伝子の変異に基づくこと、これらの疾患患者でゲノム不安定性が認められることが明らかにされている。早老症の多くで、早発性の白毛症(若白髪)が高頻度に見られることも知られており、我々は、ゲノム損傷によって誘発される色素幹細胞における変化と白髪との関連を明らかにすべく研究を進めている。 加齢に伴って、血液幹細胞においてγH2AXのフォーカス形成を認めるようになるという報告があり、加齢によって幹細胞にゲノム損傷が蓄積することが想像されている。しかし、実際に、ゲノム損傷が蓄積した細胞が本当にまだ幹細胞であると言えるのかどうか、ゲノム損傷が一定レベルを超えると、組織幹細胞はどのような運命を辿っているのかについて、in vivoでは明らかにされていない。その運命はアポトーシスや細胞老化であろうと一般に見なされていはいるが、我々が色素幹細胞システムで解析する限り、これをサポートするようなエビデンスは得られていない。我々は、色素幹細胞が一定以上のゲノム損傷を受けると、ニッチにおいて異所性に分化している可能性について検証した結果、大変興味深い知見を得ている。 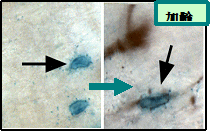 (最近の成果紹介: http://www.tmd.ac.jp/cmn/soumu/kouhou/news20090605.html) 5. 組織幹細胞をin vitroで制御する技術の開発 21世紀の新しい治療として再生医療が着目と期待を集めており、iPS細胞から目的の機能を持つ細胞を分化誘導して、これを再生医療に用いるなどの試みが盛んになされるようになった。iPS細胞作成時のリプログラミングや試験管内での維持に伴ってみられるゲノム損傷に抗して質の良い組織幹細胞を得ると同時に、移植後に組織幹細胞として正常な機能を果たす工夫が必要である。再生医療において、iPS細胞や組織幹細胞を長期にわたって安全に(癌化させることなく)維持制御するうえでも、上記1?4の取り組みから明らかになる基本原理が有効であると考えている。 6. 幹細胞システムにおける癌の発生機序の解明 癌は、加齢に伴ってその発生頻度が著しく増加する。幹細胞システムを形成する組織から、いかにして癌が発生するのか、その細胞の起源を知ることは、癌の発生機序を理解し応用する上でも重要である。マウス消化管粘膜の組織幹細胞が極めて高い頻度で癌の起始細胞となることが最近報告され、以前に増して、組織幹細胞が癌のオリジンとしても重要視されつつある。ヒトのがんのなかでも悪性黒色腫(メラノーマ)は、治療に最も苦渋する代表であり、放射線療法にも化学療法にも殆ど反応しない予後最悪の癌である。本来、色素幹細胞は、放射線に高感受性であることを見いだしているが、メラノーマは放射線や化学療法に耐性である。放射線や化学療法への耐性は、がん幹細胞の特徴としても知られ、発がんのどの段階から、どういった条件が揃った時に色素幹細胞ががん幹細胞の性質を獲得するのかを明らかにすることによって、新しい切り口からがん幹細胞の発生機序を解明したいと考えている。 2008-2009年 原著論文 1. Inomata K, Aoto T, Binh NT, Okamoto N, Tanimura S, Wakayama T, Iseki S, Hara E, Masunaga T, Shimizu H, Nishimura EK. Genotoxic stress abrogates renewal of melanocyte stem cells by triggering their differentiation. Cell. 137(6):1088-99, 2009 2. Yang G, Li Y, Nishimura EK, Xin H, Zhou A, Guo Y, Dong L, Denning MF, Nickoloff BJ, Cui R. Inhibition of PAX3 by TGF-beta modulates melanocyte viability. Mol Cell. 32(4):554-63, 2008 3. Sato-Jin K§, Nishimura E.K.§, Akasaka E, Huber W, Nakano H, Miller A, Du J, Wu M, Hanada K, Sawamura D, Fisher DE, and Imokawa G.. Epistatic Connections between MITF and Endothelin signaling in Waardenburg Syndrome and other pigmentary disorders. (§: co-first author) FASEB J. 22(4):1155-68, 2008 2008年 著書及び総説 1. 西村栄美:『色素幹細胞』 遺伝子医学Mook別册 進みつづける細胞移植治療の実際上巻 株式会社メディカルドゥ p110-114 2008 2. 西村栄美:「皮膚の幹細胞」実験医学, 最先端の幹細胞研究, 2008 増刊 p 107-112 2008年 国際学会発表 招待講演または招待シンポジウム 1. Nishimura, E.K.,Melanocyte stem cell maintenance and ageing.:International Symposium on Regenerative Medicine Tenth Anniversary of Institute for Frontier Medical Sciences.: (Kyoto) December 4th, 2008 2. Nishimura, E.K.:Hair graying,melanocyte stem cell and their niche.: 41st Annual Meeting for the Japanese Society of Developmental Biologists.: (Tokushima) May 30, 2008 3. Nishimura, E.K., Suzuki, M., Igras, V., Inomata, K., Widlund, H., Du, J., Beermann, F., Roes, J.. Miyachi, Y., Fisher, D.E.: Roles of transforming growth factor beta in melanocyte stem cell renewal.: Cojoint Meeting of XXth International Pigment Cell Conference (IPCC) & Vth International Melanoma Research Congress (IMRC), (Sapporo) May 8th, 2008 4. Nishimura, E.K.:Mechanisms of melanocyte stem cell maintenance by their niche.: International Investigative Dermatology 2008, Hair Research Symposium.: (Kyoto) May 13, 2008 2008年度 国内学会発表 招待講演または招待シンポジウム発表 1)西村栄美:ニッチによる色素幹細胞の維持機構:第7回日本再生医療学会総会 シンポジウム2(名古屋)2008年3月13日 2)西村栄美:メラノサイトの細胞生物学:第60回日本皮膚科学会西部支部学術大会 (福岡)2008年10月18日 その他 3)西村栄美:色素幹細胞の発生、維持と老化のメカニズム:第31回日本分子生物学会年会・第81回日本生化学会大会合同大会(神戸)2008年12月9日 4)西村栄美:色素幹細胞におけるステムセルエイジング:第8回日本再生医療学会総会 シンポジウム9(東京)2009年3月5日 5)Nishimura, E.K.,Identification of melanocyte stem cell niche and niche-derived factors:第8回日本再生医療学会総会 シンポジウム9(東京)2009年3月6日 6)青戸隆博:幹細胞シンポジウム(東京)2009年5月16日 2008年度 競争的研究経費取得 1) 西村栄美(代表):平成20年度科学研究費補助金 特定領域研究 『がん幹細胞の発生機序の解明とがん幹細胞ニッチの同定』 2) 西村栄美(代表):平成20年度科学研究費補助金 特定領域研究 『色素幹細胞運命決定における細胞外環境の役割とその分子基盤の解明』 3)西村栄美(代表):平成19-23年度 科学研究費補助金 若手研究(S) 『色素幹細胞の質的変化に着目した白髪発症機序の解明と老化解明へのアプローチ』 4) 西村栄美(分担):平成20年度 厚生労働省科学研究費 『固形がんにおけるがん性幹細胞の役割の究明とがん性幹細胞を標的とした治療法開発に関する研究』 5) 青戸隆博(代表):平成20年度科学研究費補助金 若手スタートアップ 『色素幹細胞のゲノム損傷応答から明らかにするメラノーマ発生機序の解明』 2008年度 特許出願 1. 海外特許出願 米国特許出願番号12/035,733 出願日:2008年2月22日 『Methods for inhibiting hair depigmentation and hair loss』 2. 国内特許出願 出願番号: PCT/JP2008/53210 出願日: 2008年2月25日 『脱毛の抑制方法および毛髪の脱色素化の抑制方法』 幹細胞 西村 東京医科歯科大学 老化 がん 白髪 幹細胞医学分野 業績 西村栄美 Cell CellStemCell |