研究開発内容
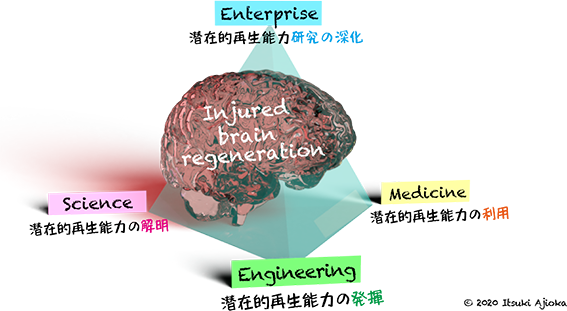
Science(理学):Project A「損傷脳の潜在的再生能力を知る」
発生期に脳などが作られる過程を研究する神経発生学や、脳神経疾患を研究する神経病理学には教科書があります。学問にも歴史があります。一方で、脳の潜在的再生能力を研究する神経再生学のような学問は萌芽期にあります。それではなぜ、脳の潜在的再生能力を知る研究が難しいのでしょうか。例えば、神経発生学であれば、形ができる前と後を比較する、神経病理学であれば、正常と病態を比較することで理解が深まります。しかしながら、脳の潜在的再生能力を研究するためには、何らかの方法で潜在的再生能力を発揮させる方法や技術が重要です。もしそれができれば、再生能力を発揮させる前と後で比較し、脳の潜在的再生能力の理解が深まります。つまり、脳の潜在的再生能力を知るためには、潜在的再生能力を発揮させる技術の発展を待つ、あるいは、自ら技術開発をする必要があります。私たちは技術の発展を待つのではなく、積極的に技術を開発し、脳の潜在的再生能力の解明に挑みます。
A1)血管新生と損傷脳再生
後述するように、私たちは東京農工大・村岡貴博先生などの協力を得て、血管新生促進因子を局所徐放する人工超分子ECM(JigSAP)を開発しました。この人工超分子ECMを亜急性期の脳梗塞マウスに投与すると、運動機能の回復が促進することを見出しました(Yaguchi et al., Nat Commun 2021, 17/999,313(米国)・EP21850578.2(欧州)・特願2022-539576(日本))。しかしながら、なぜ血管新生を促進させると損傷した脳が再生するのかに関しては、よくわかっていません。本プロジェクトでは生物学の常套的な研究アプローチでその謎を解明します。
A2)細胞周期とニューロンの細胞分裂
ニューロンは決して増殖しないと考えられてきましたが、私たちの研究によって、ニューロンにも潜在的な増殖能があることがわかってきました(Ajioka et al., Cell 2007; Oshikawa et al, Development 2013; Oshikawa et al, Development 2017)。しかしながら、そのメカニズムに関しては謎だらけです。本プロジェクトではその謎を1つずつ解明していきます。
発生期に脳などが作られる過程を研究する神経発生学や、脳神経疾患を研究する神経病理学には教科書があります。学問にも歴史があります。一方で、脳の潜在的再生能力を研究する神経再生学のような学問は萌芽期にあります。それではなぜ、脳の潜在的再生能力を知る研究が難しいのでしょうか。例えば、神経発生学であれば、形ができる前と後を比較する、神経病理学であれば、正常と病態を比較することで理解が深まります。しかしながら、脳の潜在的再生能力を研究するためには、何らかの方法で潜在的再生能力を発揮させる方法や技術が重要です。もしそれができれば、再生能力を発揮させる前と後で比較し、脳の潜在的再生能力の理解が深まります。つまり、脳の潜在的再生能力を知るためには、潜在的再生能力を発揮させる技術の発展を待つ、あるいは、自ら技術開発をする必要があります。私たちは技術の発展を待つのではなく、積極的に技術を開発し、脳の潜在的再生能力の解明に挑みます。
A1)血管新生と損傷脳再生
後述するように、私たちは東京農工大・村岡貴博先生などの協力を得て、血管新生促進因子を局所徐放する人工超分子ECM(JigSAP)を開発しました。この人工超分子ECMを亜急性期の脳梗塞マウスに投与すると、運動機能の回復が促進することを見出しました(Yaguchi et al., Nat Commun 2021, 17/999,313(米国)・EP21850578.2(欧州)・特願2022-539576(日本))。しかしながら、なぜ血管新生を促進させると損傷した脳が再生するのかに関しては、よくわかっていません。本プロジェクトでは生物学の常套的な研究アプローチでその謎を解明します。
A2)細胞周期とニューロンの細胞分裂
ニューロンは決して増殖しないと考えられてきましたが、私たちの研究によって、ニューロンにも潜在的な増殖能があることがわかってきました(Ajioka et al., Cell 2007; Oshikawa et al, Development 2013; Oshikawa et al, Development 2017)。しかしながら、そのメカニズムに関しては謎だらけです。本プロジェクトではその謎を1つずつ解明していきます。
Engineering(工学):Project B「分子を操り、潜在的再生能力を発揮させる」
共有結合で作られる高分子材料に比べ、超分子材料は低分子同士の非共有結合で作製するため、均一性をもたらします。また、私たちの体を構成する分子は高分子だけでなく超分子も多数あります。例えば、生物学の「アクチン重合」は化学用語の「重合」(共有結合)ではなく、「集合」(非共有結合による分子間結合)です。生物学分野では超分子という言葉をあまり耳にしませんが、実は超分子が多数存在します。超分子材料は物理・化学分野の発展に牽引されてスマートフォン液晶や有機半導体などの応用分野で進化を重ねています。しかしながら、超分子の生物学展開や超分子材料の再生医療・創薬応用は未踏の領域です。私たちは材料化学分野の研究者と力を合わせて、超分子生物学や超分子医療を開拓していきます。
B1)人工超分子ECM
細胞外マトリックス(ECM)は、タンパク質やその他の生体分子からなる複雑なネットワーク構造で、細胞の外から細胞増殖や細胞分化などを制御しています。ECMは、細胞の接着、増殖因子の局所作用、力学的強度の供与を担っており、正常発生や損傷組織の再生時に重要な役割を担っています。これまで様々な人工的な細胞足場材料が開発されてきましたが、多くの人工足場材料はECM機能の細胞接着のみを模倣して開発されてきました。そこで私たちは、東京農工大・村岡貴博先生と北里大・渡辺豪先生との共同研究で、生体ECMを模倣した超分子材料を開発してきました。具体的には、計算物理学を専門とする渡辺先生が分子動力学シミュレーションを駆使した超分子構造予測を担当し、合成化学を専門とする村岡先生が超分子材料の設計・合成・物性評価を担当し、私たちが生物学的な解析と材料設計へのフィードバックを担当してきました。この分野を超えた共同研究の結果、細胞接着能を持ち、様々な力学的強度を有する人工超分子ECM(JigSAP)を開発してきました(Ishida et al., Chem Eur J 2019; 特願2019-028845:PCT/JP2020/006745)。また最近、その2つの機能に加えて、増殖因子を局所徐放能を持つ人工超分子ECMの開発にも成功し、亜急性期の脳梗塞マウスモデルで運動機能回復の促進効果を持つ人工超分子ECMの開発にも成功しました(Yaguchi et al., Nat Commun 2021, 17/999,313(米国)・EP21850578.2(欧州)・特願2022-539576(日本))。本プロジェクトでは、物理・化学・生物学の叡智を結集して、細胞培養や組織再生に有用な人工超分子ECMの開発に挑戦します。
B2)光遺伝学材料
脳神経科学分野のパラダイムシフトを生み出すつつある革新的技術の1つに、光遺伝学(オプトジェネティクス)が挙げられます。光遺伝学は、光応答性タンパク質を神経細胞に発現させ、単一の神経細胞の機能(興奮や抑制など)を光で操作する技術です。しかしながら、光反応性タンパク質のほとんどが生体透過性の低い可視光応答性であり、個体レベルでの光遺伝学実験では光源を脳内に設置するため侵襲性が高くなります。そこで私たちは、合成化学を専門とする九州大学・楊井伸浩先生との共同研究で、生体透過性の高い近赤外光を青色光に変換する材料の応用に取り組んでいます。具体的には、楊井先生が九州大学・君塚信夫先生と長年開発を進めてきた「三重項-三重項消滅アップコンバージョン」材料を水中で機能するように改変し、細胞培養レベルでニューロンの光遺伝学操作を実現しました(Sasaki et al., Angew Chem Int Ed 2019)。本プロジェクトでは、楊井先生と力を合わせて、生体内での近赤外光オプトジェネティクス技術の開発を進めると共に、人工超分子ECMを近赤外光で操作する技術開発にも挑戦します。
共有結合で作られる高分子材料に比べ、超分子材料は低分子同士の非共有結合で作製するため、均一性をもたらします。また、私たちの体を構成する分子は高分子だけでなく超分子も多数あります。例えば、生物学の「アクチン重合」は化学用語の「重合」(共有結合)ではなく、「集合」(非共有結合による分子間結合)です。生物学分野では超分子という言葉をあまり耳にしませんが、実は超分子が多数存在します。超分子材料は物理・化学分野の発展に牽引されてスマートフォン液晶や有機半導体などの応用分野で進化を重ねています。しかしながら、超分子の生物学展開や超分子材料の再生医療・創薬応用は未踏の領域です。私たちは材料化学分野の研究者と力を合わせて、超分子生物学や超分子医療を開拓していきます。
B1)人工超分子ECM
細胞外マトリックス(ECM)は、タンパク質やその他の生体分子からなる複雑なネットワーク構造で、細胞の外から細胞増殖や細胞分化などを制御しています。ECMは、細胞の接着、増殖因子の局所作用、力学的強度の供与を担っており、正常発生や損傷組織の再生時に重要な役割を担っています。これまで様々な人工的な細胞足場材料が開発されてきましたが、多くの人工足場材料はECM機能の細胞接着のみを模倣して開発されてきました。そこで私たちは、東京農工大・村岡貴博先生と北里大・渡辺豪先生との共同研究で、生体ECMを模倣した超分子材料を開発してきました。具体的には、計算物理学を専門とする渡辺先生が分子動力学シミュレーションを駆使した超分子構造予測を担当し、合成化学を専門とする村岡先生が超分子材料の設計・合成・物性評価を担当し、私たちが生物学的な解析と材料設計へのフィードバックを担当してきました。この分野を超えた共同研究の結果、細胞接着能を持ち、様々な力学的強度を有する人工超分子ECM(JigSAP)を開発してきました(Ishida et al., Chem Eur J 2019; 特願2019-028845:PCT/JP2020/006745)。また最近、その2つの機能に加えて、増殖因子を局所徐放能を持つ人工超分子ECMの開発にも成功し、亜急性期の脳梗塞マウスモデルで運動機能回復の促進効果を持つ人工超分子ECMの開発にも成功しました(Yaguchi et al., Nat Commun 2021, 17/999,313(米国)・EP21850578.2(欧州)・特願2022-539576(日本))。本プロジェクトでは、物理・化学・生物学の叡智を結集して、細胞培養や組織再生に有用な人工超分子ECMの開発に挑戦します。
B2)光遺伝学材料
脳神経科学分野のパラダイムシフトを生み出すつつある革新的技術の1つに、光遺伝学(オプトジェネティクス)が挙げられます。光遺伝学は、光応答性タンパク質を神経細胞に発現させ、単一の神経細胞の機能(興奮や抑制など)を光で操作する技術です。しかしながら、光反応性タンパク質のほとんどが生体透過性の低い可視光応答性であり、個体レベルでの光遺伝学実験では光源を脳内に設置するため侵襲性が高くなります。そこで私たちは、合成化学を専門とする九州大学・楊井伸浩先生との共同研究で、生体透過性の高い近赤外光を青色光に変換する材料の応用に取り組んでいます。具体的には、楊井先生が九州大学・君塚信夫先生と長年開発を進めてきた「三重項-三重項消滅アップコンバージョン」材料を水中で機能するように改変し、細胞培養レベルでニューロンの光遺伝学操作を実現しました(Sasaki et al., Angew Chem Int Ed 2019)。本プロジェクトでは、楊井先生と力を合わせて、生体内での近赤外光オプトジェネティクス技術の開発を進めると共に、人工超分子ECMを近赤外光で操作する技術開発にも挑戦します。
Medicine(医学):Project C「潜在的再生能力を利用して、病態を改善する」
C1) 亜急性期脳梗塞患者の治療
私たちが開発した人工超分子ECM(VEGF-JigSAP)の投与で齧歯類の亜急性期脳梗塞モデルの治療効果を見出しましたが、この成果がすぐに患者さんに届くわけではありません。本プロジェクトでは、神戸医療産業都市推進機構・医療イノベーション推進センターなどとの共同研究で、人工超分子ECMの医療応用に向けて前進させていきます。最近、臨床応用を視野に入れた、安全性が高く製造費用を抑えた新しいJigSAP複合体の開発に成功しました(特願2023-192464)。現在、東京医科歯科大学病院・血管内治療科・壽美田教授などとの共同研究としてAMED橋渡し研究のサポートを受け、研究展開を図っています。
C1) 亜急性期脳梗塞患者の治療
私たちが開発した人工超分子ECM(VEGF-JigSAP)の投与で齧歯類の亜急性期脳梗塞モデルの治療効果を見出しましたが、この成果がすぐに患者さんに届くわけではありません。本プロジェクトでは、神戸医療産業都市推進機構・医療イノベーション推進センターなどとの共同研究で、人工超分子ECMの医療応用に向けて前進させていきます。最近、臨床応用を視野に入れた、安全性が高く製造費用を抑えた新しいJigSAP複合体の開発に成功しました(特願2023-192464)。現在、東京医科歯科大学病院・血管内治療科・壽美田教授などとの共同研究としてAMED橋渡し研究のサポートを受け、研究展開を図っています。
Enterprise(事業):Project X「基礎研究へ還元し、神経再生研究を深化させる」
X1)小規模ラボの研究成果を医薬品へと展開する仕組みの確立
薬の開発にかかる時間と費用は、10年1000億円と言われています。私たちの開発した技術が、齧歯類の脳梗塞モデルで治療効果があると言っても、薬を製造販売する大企業がすぐに興味を示すわけではありません。大企業に興味を持ってもらうデータを得るためには、誰かが開発を進めなければなりません。しかしながら、実用化に必要なデータを得ることは、大学の小規模ラボが独力でできる範疇をはるかに超えています。そこで経営学などのビジネスの専門家と協力し、小規模ラボの研究成果を医薬品へと展開する仕組みの確立に挑戦しています。本プロジェクトは神奈川県産業技術総合研究所(KISTEC)のサポートを得て進めています。
X2)公的研究費以外の研究開発費を得て、基礎研究へと還元する仕組みの確立
基礎研究の重要性が社会でも広く認識されつつありますが、実際私たちも科研費などの様々な公的研究費を得て、実用化研究へとつながる研究成果を得ることができました。しかしながら、右肩上がりの経済成長を終えた日本で、中国やインドのように莫大な研究費を基礎研究に投入するというのは難しいかもしれません。もし、私たちの研究成果が経済的な利益を生むことができれば、その利益をラボの基礎研究費に充て、基礎研究をさらに充実させることができるかもしれません。そこで本プロジェクトでは、経営学の専門家などと協力して、ラボのエコシステム構築に挑戦します。
X1)小規模ラボの研究成果を医薬品へと展開する仕組みの確立
薬の開発にかかる時間と費用は、10年1000億円と言われています。私たちの開発した技術が、齧歯類の脳梗塞モデルで治療効果があると言っても、薬を製造販売する大企業がすぐに興味を示すわけではありません。大企業に興味を持ってもらうデータを得るためには、誰かが開発を進めなければなりません。しかしながら、実用化に必要なデータを得ることは、大学の小規模ラボが独力でできる範疇をはるかに超えています。そこで経営学などのビジネスの専門家と協力し、小規模ラボの研究成果を医薬品へと展開する仕組みの確立に挑戦しています。本プロジェクトは神奈川県産業技術総合研究所(KISTEC)のサポートを得て進めています。
X2)公的研究費以外の研究開発費を得て、基礎研究へと還元する仕組みの確立
基礎研究の重要性が社会でも広く認識されつつありますが、実際私たちも科研費などの様々な公的研究費を得て、実用化研究へとつながる研究成果を得ることができました。しかしながら、右肩上がりの経済成長を終えた日本で、中国やインドのように莫大な研究費を基礎研究に投入するというのは難しいかもしれません。もし、私たちの研究成果が経済的な利益を生むことができれば、その利益をラボの基礎研究費に充て、基礎研究をさらに充実させることができるかもしれません。そこで本プロジェクトでは、経営学の専門家などと協力して、ラボのエコシステム構築に挑戦します。

