1.神経筋接合部 2.カルシウムイオンチャンネル 3.アセチルコリン受容体の構造 4.終板電位 関連するサイトとリンク(このページへ戻るときはブラウザーの戻るを選んでください) http://www.emory.edu/CHEMISTRY/justice/chem190j/の最初の2つ http://www.blackwellscience.com/matthews/index.html 更新日:2001年8月28日
前回までに述べたように、ニューロンは刺激を受けて興奮する。興奮とは活動電位を発生することである。ニューロンが発生する活動電位すなわちインパルスは、軸索を伝わって終板に達し、筋肉は収縮する。収縮がおこるのは、T管に生じた電気的変化によって電位依存型カルシウムチャンネルが開き、カルシウムイオンが筋小胞体から放出されるためである。
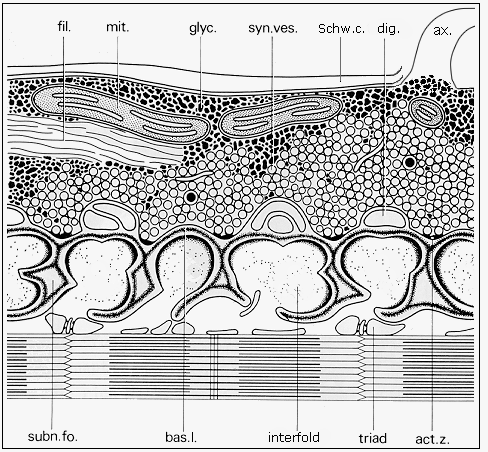
それでは、軸索の電気的な変化がどのようにして筋肉のT管の電気的な変化に伝えられるのであろうか。すでに簡単に述べたように、運動神経と筋肉の接合部は連続しているわけではなく、終板という構造が存在する。この部分は神経筋接合部( neuromuscular junction )とも呼ばれ、その構造は次のようなものである。
ax. - 軸索, fil. - ニューロフィラメント, mit. - ミトコンドリア, glyc. - グリコーゲン, syn. ves. - シナプス小胞, Schw. c. - シュワン細胞, dig. - シュワン細胞の突起, subn. fo. - シナプス後膜ののひだ, bas. l. - 基底層, act. z. - シナプス後膜アクティブゾーン
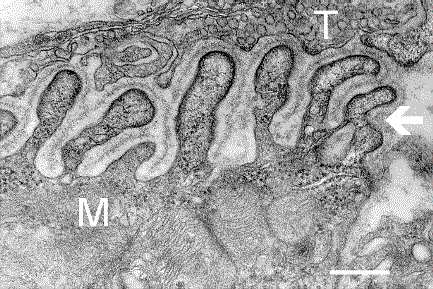
M:筋繊維、T:軸索末端
http://synapses.bu.edu/anatomy/nmj/nmj.stmより
中枢神経系にはいろいろな種類のたくさんのシナプスが存在するが、単一のシナプスを取り出して調べるわけにいかない。神経筋接合部はシナプスのよいモデルとなる。神経−筋標本(カエルの座骨神経−腓腸筋標本)を作り、神経を刺激して筋繊維から記録を取る、という方法でシナプスの機能がよく研究された。
上の図から分かるように、軸索末端にシナプス小胞が多数存在する。インパルスが到着すると、このシナプス小胞は軸索末端の細胞膜と融合し、中身を放出する。中身とはアセチルコリンという分子である。
アセチルコリンは、シナプス間隙を拡散し、シナプス後膜に達し、シナプス後膜に興奮を伝える。これを伝達(transmission)といい、アセチルコリンのように神経末端から放出される分子を神経伝達物質(neurotransmitter)と呼ぶ。
それでは、アセチルコリンがどうしてシナプス前膜の電気的信号をシナプス後膜へ伝えるのだろうか。
次の動画は全体を理解するのによい(このページへ戻るときはブラウザーの戻るを選んでください)
http://web.mit.edu/rujira/www/4.206/neuron/synapse.html
1)カルシウムイオンチャンネル
神経筋接合部に活動電位がくると、この電圧の変動によって、電位依存性カルシウムチャンネル(voltage-gated Ca2+ channel)が、前回述べた電位依存性ナトリウムチャンネルと全く同じようにして開き、細胞間液のCaイオンが流入する。このCaイオンが伝達物質の放出に働く。
これは次のような実験を行なって証明することができる。神経筋標本を培養し、培養液中のCaイオンを除くと、活動電位が来ても伝達物質の放出は起こらない。また、軸索末端の内部へ直接Caイオンを注入すると神経伝達物質の放出が起こる。
実際に流入するカルシウムイオンの量は、膜に大きな電位変化を起こすほどの量ではない。しかしながら、細胞内のカルシウムイオンは常に低く押えられているので(10-7 M)、この流入は濃度を10から100倍上げることになる。これが細胞内メッセンジャーとして働く。
流入したCaイオンは、すぐさまCa結合蛋白やストアサイトに取り込まれたり、Caポンプで細胞外へ排出され、濃度はすぐに下げられてしまう。
2)伝達物質の放出
軸索末端にはたくさんの大きさの均一な(40nm)シナプス小胞(synaptic vesicle)が存在し、このなかにアセチルコリンが含まれている。Caイオンの流入はこの小胞のシナプス前膜へ向かう移動、膜への融合、内容物の放出をおこす(開口分泌、exocytosis)。開口分泌が起こる場所は決っているらしく、その反対側、すなわちシナプス後膜側に受容体があり、拡散による時間のロスを最小にしている。融合した小胞のあまった膜は食細胞運動(endocytosis)によって取り込まれ、リサイクルされる。
3)アセチルコリン受容体が化学的信号を電気的信号に戻す
アセチルコリンはシナプス後膜に存在する受容体に結合し、受容体であるとともにナトリウムチャンネルでもある分子のコンフォメーションの変化を引き起こし、チャンネルを開かせる。そのためナトリウムイオンが流入し、電位変化が起こる。この電位変化が今度は電位依存型ナトリウムチャンネル(voltage-gated channels)を開くことになり、活動電位を引き起こす。
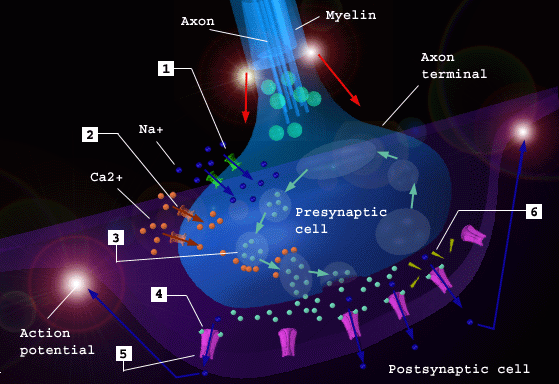
以上の1)から3)までの過程を示すと、上の図のようになる。全部で4種類6個のチャンネルが関係している。
●初めはすべてのチャンネルは閉じているが、軸索末端にインパルス(赤い矢印)が到着すると、電位依存性Naチャンネル(上の図1)が開いて電位が変化する。
●次に電位依存性のCaチャンネル(上の図2)が開きCaイオンが軸索末端へ流入する。
●これが刺激となって、シナプス小胞(上の図3)がシナプス前膜と融合してアセチルコリンが放出される。
●アセチルコリンがシナプス後膜の受容体(と同時にNaチャンネル)(上の図4)と結合すると、電気的変化が起こる。
●シナプス後膜の電位依存性のNaチャンネル(1と同じものだが上の図では省略)が開き、活動電位(青い矢印)が発生する。
●この活動電位がT管を伝わり、T管上のCaチャンネル(上の図では省略)を開き、最後に筋小胞体の別のCaチャンネル(上の図では省略)を開く。
●アセチルコリンはアセチルコリンエステラーゼ(上の図6)によって分解される。コリンはシナプス前膜によって取り込まれ再利用される。
以上を動画で示したものが、下のページにある。
http://www.blackwellscience.com/matthews/nmj.html
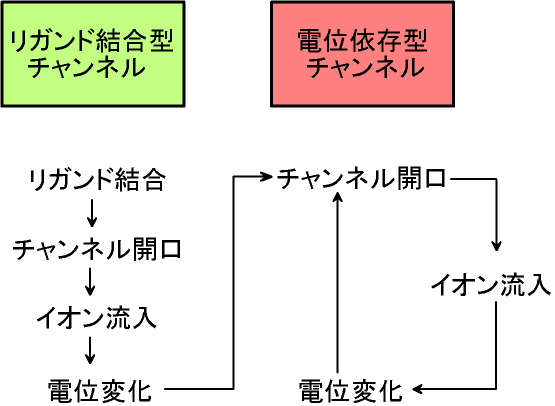
4)リガンド結合型チャンネルと電位依存型チャンネル
上に述べたアセチルコリン受容体のようなリガンド結合型チャンネルでは、受容体部に結合するリガンド(ligand)によって開口するので、電位依存型チャンネルと違って、電位変化には影響されにくい。したがって、全か無かの反応も起こさないし、自己増幅的興奮もしない。
そのかわり、刺激の強さと長さに応じた段階的(graded)な電位変化を示す。すなわち、伝達物質がどのくらいシナプス間隙に放出されたか、あるいはどのくらい残っているかに応じた変化をすることになる。この点が大変重要である。
リガンド結合型受容体には、さらにもう2つ重要な点がある。1つは受容体としての側面から生まれるリガンドに対する特異性である。もう1つはチャンネルとしての側面から生まれるイオンに対する選択性である。
あるものはKイオンだけを通し、あるものはClイオンだけを通す。あるいはカチオンは通すがアニオンは通さないチャンネルもある。このイオンの選択性がシナプス後膜の反応の性質を決定することになる。このことについては後で再び述べる。
5)アセチルコリンは分解され除かれる
信号はどこかでオフにならなければならない。すなわちシナプス間隙に出されたアセチルコリンはすぐさま除かれる必要がある。
1)拡散によって濃度が薄まる
2)はアセチルコリンエステラーゼ(acetylcholinesterase)(下の図)によって分解される
アセチルコリンエステラーゼは、筋肉細胞によって分泌され、コラーゲンに似た尾部で神経末端と筋肉細胞の間の基底層(basal lamina)に繋がれている。1ミリ秒当り10個のアセチルコリンを分解できるので、5000個のアセチルコリン分子も数100ミリ秒後にはシナプス間隙から無くなってしまう。
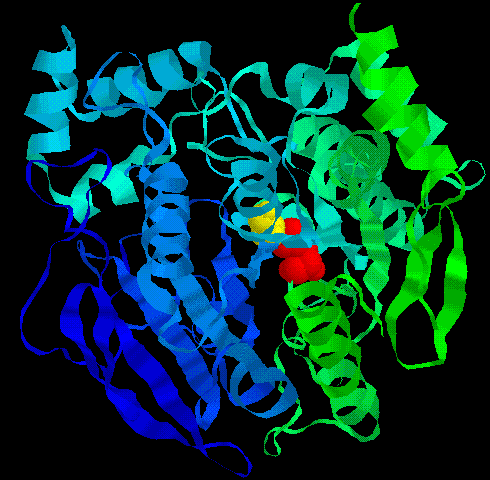
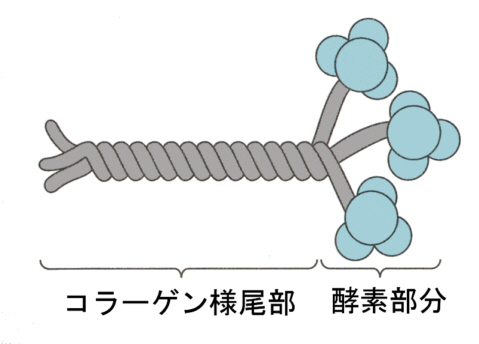
アセチルコリンエステラーゼの酵素部分
黄色と赤は活性中心を構成するセリンとヒスチジン
さらに学びたい人へ(プラグインchimeをインストールすること、登録ダウンロードとも無料)
http://srv2.lycoming.edu/‾newman/courses/bio43799/acetylcholinesterase/
次のページは全体を理解するのによい(このページへ戻るときはブラウザーの戻るを選んでください)
http://web.mit.edu/rujira/www/4.206/neuron/ach.html
アセチルコリン受容体の構造が解明されている。受容体は五量体(α2βγδ)で、細胞膜内に次の図のように埋まっていると考えられている。
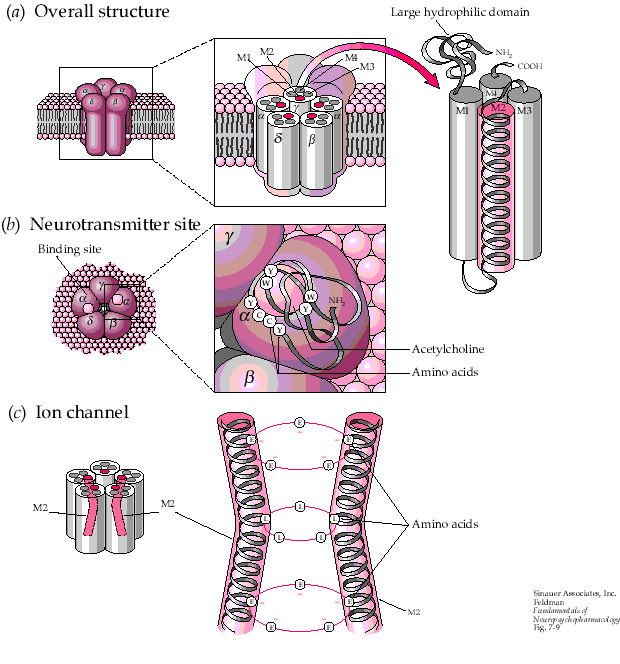
http://www.emory.edu/CHEMISTRY/justice/chem190j/nicotinic_receptors.htmより
γサブユニットのアミノ酸配列から得られる疎水性の度合いを、横軸をアミノ酸番号、縦軸を疎水性の度合いを示す指標でプロットしてみると、4つの部分が疎水性の強い部分が現れる(下の図M1−M4)。この部分が脂質の二重膜に埋まる部分で、N末端の部分は親水性の強い部分であることが分る。
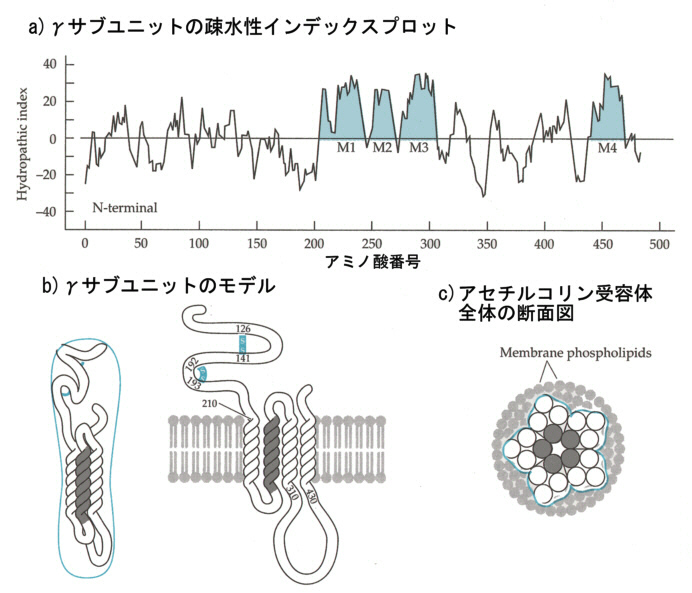
An Introduction to Molecular Neurobiology Z.W. Hall, Sinauer, 1992より
この事実からγサブユニットは上の図のb)ような構造であると推定されている。α、βも同じような構造を取り、これらが5つ集まったものが受容体となる。アセチルコリンはαサブユニットと結合するので、アセチルコリンは2分子、受容体に結合できる。
アセチルコリン受容体を含む細胞膜に、先の細いガラスピペットを押しつけ、陰圧にして吸着しちぎり取ることができる(パッチクランプ法、下の図上段左)。こうして一つの受容体を流れる電流を測定してみると、アセチルコリンが結合したときに、ほんのわずかな電流が流れることを測定することができる。
アセチルコリンが2個、結合すると、チャンネルは「開」である確立が高くなることがわかる。このような小さな電流が加算されて、上に述べたような爆発的な電流の変化になると考えられる。
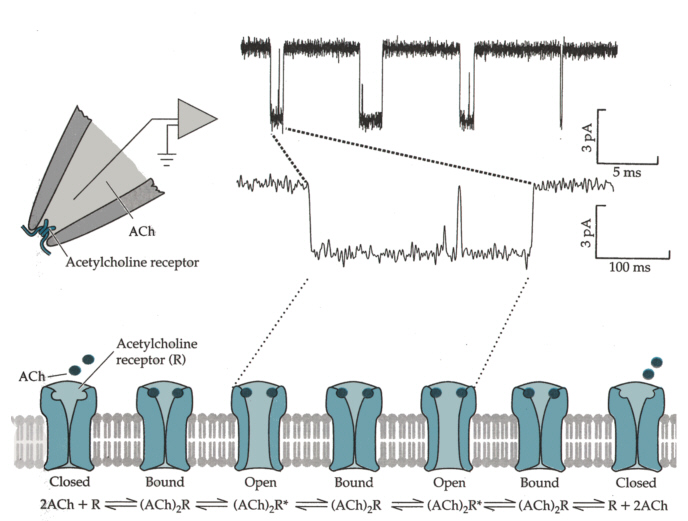
An Introduction to Molecular Neurobiology Z.W. Hall, Sinauer, 1992より
アセチルコリン受容体にアセチルコリンが結合して、チャンネルが開き、ナトリウムイオンが流入すれば電流が流れ、局所的に電位が脱分極に向かう。ガラス電極を終板のシナプス後膜側に刺入して、この電位変化を測定することができる。この電位を終板電位(endplate potential、EPP)という。
これまで述べたように、EPPは活動電位とは異なり、全か無かの法則にはしたがわない。多数のシナプス小胞がシナプス前膜と融合してたくさんのアセチルコリンが放出されれば、EPPは足し算され、閾電位を越えると活動電位が発生する。
終板以外でも、このようなシナプス後膜側の電位変化を測定することができる。シナプス後膜側における電位変化なので、シナプス後電位(postsynaptic potential、PSP)と呼ぶ。
アセチルコリン受容体のように、ナトリウムイオンを通すチャンネルが開く場合は、電位変化は脱分極側におこる。一方、塩素イオンのようなマイナスイオンを通すチャンネルの場合は、電位変化は過分局側に振れる。そこで、前者を興奮性シナプス後電位(excitatory postsynaptic potential、EPSP)と言い、後者を抑制性シナプス後電位(inhibitory postsynaptic potential、IPSP)と言う。
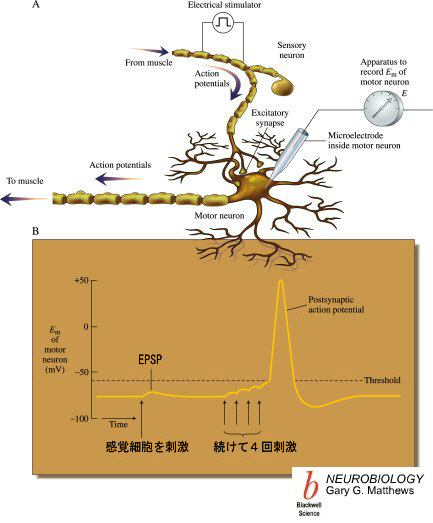
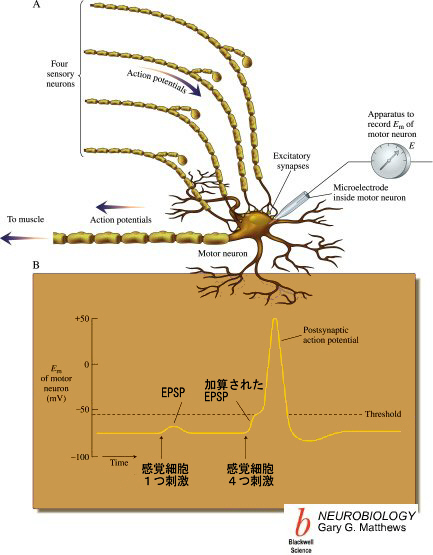
時間的加算(temporal summation)と空間的加算(spatial summation)
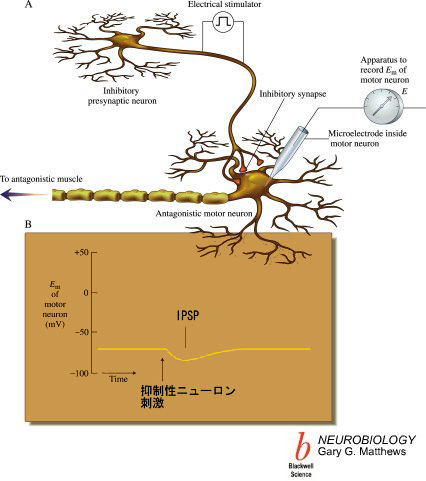

抑制性シナプス後電位と興奮性シナプス後電位の加算
関連するサイトとリンク(このページへ戻るときはブラウザーの戻るを選んでください)
http://www.zoology.ubc.ca/‾auld/bio350/index.html
![]() この章のpdfファイルをダウンロードするには、左のアイコンを右クリックしてください。
この章のpdfファイルをダウンロードするには、左のアイコンを右クリックしてください。